2. АТОМНО-КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
Металлические материалы. 83 из известных 112 химических элементов таблицы Менделеева Д. И. являются металлами. Они обладают рядом характерных свойств:
- высокой тепло- и электропроводностью;
- положительным коэффициентом электросопротивления (с повышением температуры электросопротивление растет);
- термоэлектронной эмиссией (испусканием электронов при нагреве);
- хорошей отражательной способностью (блеском);
- способностью к пластической деформации;
- полиморфизмом.
Наличие перечисленных свойств обусловлено металлическим состоянием вещества, главным из которых является наличие легкоподвижных коллективизированных электронов проводимости.
Металлическое состояние возникает в совокупности атомов, когда при их сближении внешние (валентные) электроны теряют связь с отдельными атомами, становятся общими и свободно перемещаются между положительно заряженными, периодически расположенными ионами. Силы притяжения (силы связи) в твердых телах существенно отличаются по своей природе. Обычно рассматривают четыре основных типа связей в твердых телах: ван-дер-ваальсовые, ковалентные, металлические, ионную.
Под атомно-кристаллической структурой понимают взаимное расположение атомов в кристалле. Кристалл состоит из атомов (ионов), расположенных в определенном порядке, который периодически повторяется в трех измерениях. Наименьший комплекс атомов, который при многократном повторении в пространстве позволяет воспроизвести пространственную кристаллическую решётку, называют элементарной ячейкой.
Для характеристики элементарной ячейки используют параметры кристаллической решётки: три ребра а, в, с, измеряемых в ангстремах (1Å = 1* 10-8см) или в килоиксах – kX (1kX = 1,00202 Å) и три угла a, b, g, а также компактность структуры h - отношение объема, занимаемого атомами, к объёму ячейки (для решётки ОЦК h = 64 %, для решётки ГЦК h = 74 %) и координационное числоК - число ближайших соседей данного атома: для решётки ОЦК это число равно 8, т.е. атомы, находящиеся в вершине, принадлежат восьми элементарным ячейкам (рис.2.1.а), для решётки ГЦК это число равно 12, т.е. атомы, находящиеся в вершине, принадлежат двенадцати элементарным ячейкам (рис. 2.1.б).
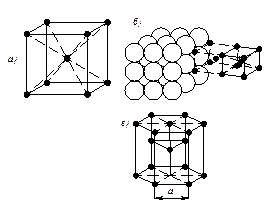
Рис.2.1. Схема определения координационного числа кристаллической решётки: а – ГЦК; б – ОЦК; в – ГПУ
Простейшим типом кристаллической ячейки является кубическая решётка. В простой кубической решётке атомы расположены (упакованы) недостаточно плотно.
Стремление атомов металла занять места, наиболее близкие друг к другу, приводит к образованию решеток других типов (рис. 2.2):
- объёмноцентрированной кубической решётки (ОЦК) (рис.2.2а) с параметром
а = 0,28 – 0,6мм = 2,8 – 6,0 Å
- гранецентрированной кубической решётки (ГЦК) (рис.2.2б) с параметром
а = 0,25мм
- гексагональной плотно упакованной решётки (ГПУ) (рис.2.2в) с параметром
с / а » 1,633

Рис. 2.2. Кристаллические решётки: а – гранецентрированный куб (ОЦК); б – объемноцентрированный куб (ГЦК); в- гексагональная плотно упакованная (ГПУ)
Узлы (положения атомов), направления в плоскости и в пространстве обозначаются с помощью так называемых индексов Миллера (рис. 2.3). Индексы узла записываются – (mnp), индексы направления - [mnp], индекс плоскости - (hk1).
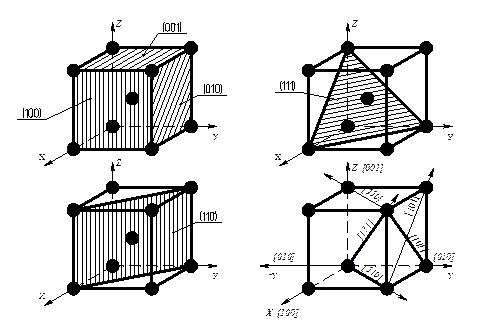
Рис. 2.3. Символы некоторых важнейших узлов, направлений и плоскостей в кубической решётке
Вследствие неодинаковой плотности атомов в различных плоскостях и направлениях решётки многие свойства отдельно взятого кристалла (химические, физические, механические) по данному направлению отличаются от свойств в другом направлении и, естественно, зависят от того, сколько атомов встречается в этом направлении. Различие свойств в зависимости от направления испытания носит название анизотропии. Все кристаллы анизотропны. Анизотропия – особенность любого кристалла, характерная для кристаллического строения.
Технические металлы являются поликристаллами, т.е. состоят из совокупности кристаллитов с различной ориентацией. При этом свойства во всех направлениях усредняются.
2.1. Строение реальных кристаллов
Реальный кристалл состоит из скопления большого числа мелких кристаллов неправильной формы, которые называются зернами или кристаллитами (рис. 2.4).

Рис. 2.4. Блочная структура кристалла: схема (а); реальная блочная структура в алюминии (б), наблюдаемая в электронном микроскопе на просвет, (х 35000)
Зерно не является монолитным кристаллом, построенным из строго параллельных атомных слоев. В действительности оно состоит как бы из мозаики отдельных блоков, кристаллографические плоскости в которых повернуты друг относительно друга на небольшой угол – порядка нескольких минут. Такое строение зерна носит название мозаичной структуры, а составляющие ее блоки называются блоками мозаики.
Часто блоки объединяются в более крупные агрегаты – так называемые фрагменты. Фрагменты в свою очередь разориентированы относительно друг друга в несколько градусов. Зерна ориентированы случайно по отношению друг к другу. Преимущественная ориентация зерен называется текстурой. Поверхность раздела зерен называется границей.
Технические металлы являются поликристаллами, т.е. состоят из совокупности кристаллитов с различной ориентацией, что приводит к изменению свойств металлов при различных процессах их обработки.
При определенных условиях, обычно при очень медленном контролируемом отводе тепла при кристаллизации, может быть получен кусок металла, представляющий собой один кристалл, который называют монокристаллом.
2.2. Дефекты кристаллического строения
Строение реальных кристаллов отличается от идеальных. Реальные кристаллы всегда содержат несовершенства (дефекты) кристаллического строения, которые нарушают связи между атомами и оказывают влияние на свойства металлов.
Дефекты в кристаллах принято классифицировать по характеру их измерения в пространстве:
1. Точечные. Точечными дефектами называются нарушения периодичности кристалла, размеры которых сопоставимы с размерами атома во всех измерениях.
К точечным дефектам относятся вакансии, межузельные атомы, примеси замещения, примеси чужеродных атомов внедрения (рис. 2.5).
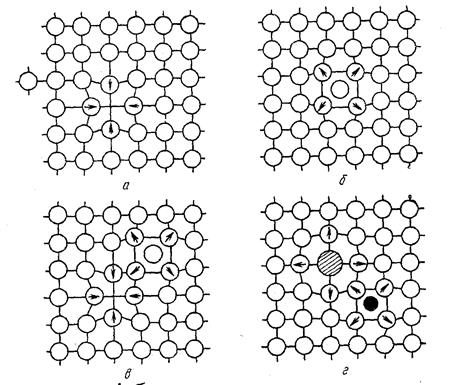
Рис. 2.5.Точечные дефекты в кристаллической решетке: а- вакансия;
б - межузельный атом; в- дефект Френкеля; г- примесные атомы замещения (большой) и внедрения (маленький).
Стрелками указаны направления смещений атомов в решетке.
Вакансии и межузельные атомы появляются в кристаллах при любой температуре выше абсолютного нуля из-за тепловых колебаний атомов. Каждой температуре соответствует равновесная концентрация вакансий, а также межузельных атомов. Например, в меди при температуре 20-25 оС содержится 10-13 ат. % вакансий, а вблизи точки плавления - уже 0,01 ат. % (одна вакансия приходится на 104 атомов).
Пересыщение точечными дефектами достигается при резком охлаждении после высокотемпературного нагрева, при пластическом деформировании и при облучении нейтронами. Чем выше температура, тем больше концентрация вакансий и тем чаще они переходят от узла к узлу. Вакансии являются самой важной разновидностью точечных дефектов; они ускоряют все процессы, связанные с перемещениями атомов: диффузию, спекание порошков и т. д.
2. Линейные. Линейные дефекты в кристаллах характеризуются тем, что их поперечные размеры не превышают нескольких межатомных расстояний, а длина может достигать размера кристалла. К линейным дефектам относятся дислокации – линии, вдоль и вблизи которых нарушено правильное периодическое расположение атомных плоскостей кристалла.
Важнейшие виды линейных несовершенств - краевые и винтовые дислокации (рис.2.6).
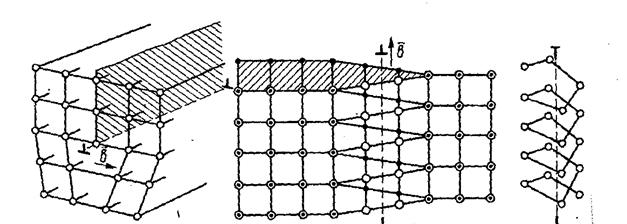
а б
Рис. 2.6. Схема дислокаций: а – краевая; б - винтовая
Краевая дислокация в сечении представляет собой край «лишней» полуплоскости в решетке (рис.2.7)
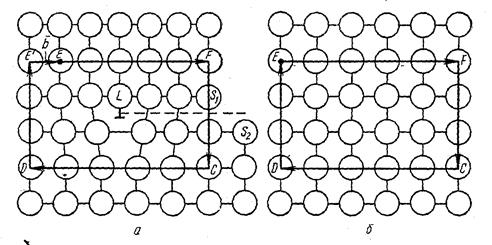
Рис. 2.7. Сечение простой кубической решетки: а - с краевой дислокацией; б - без дислокации.
Вокруг дислокаций решетка упруго искажена. Схема образования атмосферы Коттрелла в кристалле представлена на рисунке 2.8.

Рис. 2.8. Образование атмосферы Коттрелла: а – атомы примеси замещения (заштрихованы) и внедрения беспорядочно расположены в решетке; б, в – атомы примеси переместились к дислокации, в результате чего энергия решетки понизилась.
3. Поверхностные (двумерные). Под этими дефектами понимают нарушения, которые обладают большой протяженностью в двух измерениях и протяженностью лишь в несколько межатомных расстояний в третьем измерении.
К поверхностным дефектам относятся дефекты упаковки, двойниковые границы, границы зерен.
4. Объемные (трехмерные). Под ними понимают нарушения, которые в трех измерениях имеют неограниченные размеры. К таким нарушениям относят трещины, поры, усадочные раковины.
2.3. Превращения в твердом состоянии. Полиморфизм
Атомы данного элемента могут образовать, если исходить только из геометрических соображений, любую кристаллическую решетку. Однако устойчивым, а следовательно, реально существующим типом является решетка, обладающая наиболее низким запасом свободной энергии.
Так, разные металлы образуют разные виды кристаллической решетки:
- Li, Na, K, Mo, W – ОЦК;
- Al, Ca, Cu, Au, Pt – ГЦК;
- Mg, Zr, Hf, осмий – ГПУ.
Однако в ряде случаев при изменении температуры или давления может оказаться, что для одного и того же металла более устойчивой будет другая решетка, чем та, которая существует при данной температуре или давлении. Так, например, существует железо с решетками объемно-центрированного и гранецентрированного кубов, обнаружен кобальт с гранецентрированной и с гексагональной решетками.
Существование одного и того же металла (вещества) в нескольких кристаллических формах носит название полиморфизма или аллотропии. Различные кристаллические формы одного вещества называются полиморфными или аллотропическими модификациями (таблица 2.1).
Таблица 2.1
Аллотропические модификации металлов
| Металл | Группа | Модификация | Кристаллическая решетка | |||
| Кальций | II-A | Сaa до 450 Caab 450-851 | Кубическая гранецентрированная Гексагональная плотноупакованная | |||
| Галлий | III-B | Gaa Gab | Ромбическая Тетрагональная | |||
| Таллий | III-B | Tla до 262 Tlb 262-304 | Гексагональная плотноупакованная Кубическая объемноцентрированная | |||
| Титан | IV-A | Tia до 882 Tib 882-1725 | Гексагональная плотноупакованная Кубическая объемноцентрированная | |||
| Цирконий | IV-A | Zra до 862 Zrb 862-1830 | Гексагональная плотноупакованная Кубическая объемноцентрированная | |||
| Гафний | IV-A | Hfa до 1610 Hfb 1610-1952 | Гексагональная Кубическая объемноцентрированная | |||
| Олово | IV-B | Sna до 18` Snb 18-232 | Алмазная Тетрагональная объемноцентрированная | |||
| Вольфрам | VI-A | Wa до 650 Wb 650-3400 | Кубическая объемноцентрированная Сложная (нерасшифрованная) | |||
| Уран | VI-A | Ua до 660 Ub 660-770 Ug 770- 1133 | Ромбоэдрическая Тетрагональная Кубическая объемноцентрированная | |||
| Марганец | VII-A | Mna до 742 Mnb 742-1080 Mng 1080-1180 Mnd 1180-1242 | Кубическая сложная ««Тетрагональная гранецентрированная Неизвестна | |||
| Железо | VIII | Fea до 910 1401-1539 Feg 910-1401 | Кубическая объемноцентрированная Кубическая гранецентрированная | |||
| Кобальт | VIII | Coa до 477 Cob 477-1490 | Гексагональная плотноупакованная Кубическая гранецентрированная | |||
Аллотропические формы обозначаются греческими буквами a, b, g и т.д., которые в виде индексов добавляют к символу, обозначающему элемент. Аллотропическая форма при самой низкой температуре, обозначается буквой a, следующая - b и т. д.
Явление полиморфизма основано на едином законе об устойчивости состояния с наименьшим запасом энергии. Запас свободной энергии зависит от температуры. Поэтому в одном интервале температур более устойчивой является одна модификация, а в другом – другая. Температура, при которой осуществляется переход из одной модификации в другую, носит название температуры полиморфного (аллотропического) превращения.
Механизм роста кристаллов новой фазы может быть нормальным кристаллизационным и мартенситным. Нормальный механизм роста – это зарождение новой фазы на границах зерен, блоков, фрагментов при малых степенях переохлаждения (Sna «Snb).
Мартенситный механизм реализуется при низких температурах и большой степени переохлаждения, при малой диффузионной подвижности атомов путем их сдвига (смещения) по определенным кристаллографическим плоскостям и направлениям. Новая фаза имеет форму игл и растет очень быстро (Coa «Cob).
Аллотропическое превращение сопровождается изменением свойств, объема и появлением внутренних напряжений.