а). Простые вещества.
2KCN + H2SO4 ®2HCN + K2SO4 (МУ)
2K+ + 2CN- + 2H+ +SO42- ® 2HCN + 2K+ +SO42- (ИМУ)
CN- + H+ ® HCN (Кд HCN = 7,8•10-10) –ионно-молекулярное ур-е образования слабого электролита HCN.
б).Комплексные соединения.
ZnCl2 + 4NH3 ® [Zn (NH3)4]Cl2 (МУ)
Zn2+ + 2Cl- +4NH3 ® [ Zn (NH3)4]2+ + 2Cl- -(ИМУ)
Zn2++4NH3 ® [Zn(NH3)4]2+- краткое ионно-молекулярное уравнение образования комплексного катиона.
Встречаются процессы, при которых слабые электролиты или малорастворимые соединения входят в число исходных веществ и продуктов реакции. Равновесие в этом случае смещается в сторону образования веществ, имеющих наименьшую константу диссоциации или в сторону образования менее растворимого вещества:
А) NH4OH + HCl ® NH4Cl + H2O (МУ)
NH4OH + H+ + Cl- ® NH4+ + Cl- + H2O (ИМУ)
NH4OH + H+ ® NH4+ + + H2O (ИМУ)
Кд( NH4OH) =1,8× 10-5 > Кд( H2O) =1,8×10-16
Равновесие сдвинуто в сторону образования молекул воды.
Б) HCN + CH3COONa ® NaCN + CH3COOH (МУ)
HCN + CH3COO- + Na+ ® Na+ + CN- + CH3COOH (ИМУ)
HCN + CH3COO- ® CN- + CH3COOH
Kд( HCN)=7,9× 10-10 < Кд( CH3COOH) =1,8 ×10-5
Равновесие сдвинуто в сторону образования HCN.
В) AgCl¯ + NaI ®AgI¯ + NaCl (МУ)
AgCl¯ + Na+ +I- ®AgI¯+ Na+ +Cl- (ИМУ)
AgCl¯ + I- ®AgI¯ + Cl- ПР AgCl=1,78×10-10 > ПР AgI =8,3×10-17
Равновесие сдвинуто в сторону образования осадка AgI.
Г) Могут встречаться процессы, в уравнениях которых есть и малорастворимое соединение и слабый электролит
MnS¯ + 2HCl ® MnCl2 + H2S
MnS¯ + 2H+ +2Cl- ® Mn 2+ + 2Cl- + H2S
MnS¯ + 2 H+ ® Mn2+ + H2S
ПР MnS=2,5×10-10; [S-2]= 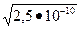 =1,58.10-5 моль/л
=1,58.10-5 моль/л
Kд H2S= K1×K2 = 6×10-22; [S2-] = 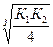 =5,4.10-8 моль/л
=5,4.10-8 моль/л
Связывание ионов S2- в молекулы H2S происходит полнее, чем в MnS, поэтому реакция протекает в прямом направлении.
Гидролиз солей.
Гидролиз является результатом поляризационного взаимодействия ионов соли с их гидратной оболочкой. Гидролиз - это обменная реакция в растворе между молекулами воды и ионами соли. В результате гидролиза, благодаря образованию слабого электролита (слабой кислоты или слабого основания), изменяется ионное равновесие Н2О ⇄ Н+ + ОН- из-за связывания Н+ или ОН- и изменяется рН-среды. Гидролизу подвергаются соли, в состав которых входят ионы слабой кислоты или слабого основания. Соли, образованные ионами сильной кислоты и сильного основания, гидролизу не подвергаются (NaCl, Na2SO4). Продуктами гидролиза могут быть слабые электролиты, малодиссоциирующие, труднорастворимые и летучие вещества. Гидролиз - стадийная реакция, в случае многозарядного иона число стадий равно его заряду. Гидролизу по катиону подвергаются соли, образованные анионами сильной кислоты и катионами слабого основания. Например, к слабым основаниям относятся гидроксиды p- и d-металлов (Кд £10-4), а также гидроксид аммония.
Хлорид цинка - соль, образованная слабым основанием Zn(OH)2 и сильной кислотой HCl. Катион цинка имеет заряд 2+, поэтому гидролиз будет проходить в две ступени: Zn2+ + HOH ⇄ ZnOH+ + H+ I ступень
ZnOH+ + HOH ⇄ Zn(OH)2 + H+ II ступень
В результате этого взаимодействия возникает избыток ионов Н+ ([Н+] > [ОН-]) , раствор подкисляется (рН<7).
Гидролиз по аниону. Данный тип гидролиза характерен для солей, образованных анионами слабой кислоты (Кд £10-3) и катионами сильного основания (Kд >10-3). Рассмотрим гидролиз карбоната калия - соли, образованной слабой угольной кислотой H2CO3 (KдI = 4,5. 10-7) и сильным основанием KOH, карбоксо-анион имеет заряд (2-). Гидролиз протекает в две ступени: CO32- + H2O ⇄ HCO3- + OH- I ступень
HCO3- + H2O ⇄ H2CO3 + OH- II ступень
В этом случае высвобождаются ионы ОН- ([Н+] < [ОН-]) - раствор подщелачивается (рН >7).
Необратимый гидролиз. Соли, образованные слабым основанием и слабой кислотой, гидролизуются по катиону и аниону. Результат гидролиза будет зависить от значения Кд основания и кислоты. Рассмотрим гидролиз фторида аммония - соли, образованной слабым
основанием NH4OH (Кд =1,8 . 10-5) и слабой кислотой HF (Кд = 6,8 .10-4):
NH4F + HOH ® NH4OH + HF
В этом случае Кд( NH4OH) < Кд( HF), следовательно гидролиз (в основном) пойдет по катиону и реакция среды будет слабокислой.
ЗАДАЧИ
Реакции ионного обмена
1. Можно ли приготовить раствор, содержащий одновременно следующие пары веществ: а) Cu(NO3)2 и NaCl; б) NaOH и HCl; в)BaCl2 и H2SO4? Составить молекулярные (МУ) и ионно-молекулярные уравнения возможных реакций (ИМУ).
2. Будут ли протекать реакции между растворами следующих электролитов: а)K2CO3 и HCl; б) KNO3 и Na2S; в) CdSO4 и NaOH? Написать молекулярные и ионно-молекулярные уравнения возможных реакций.
3. Написать ионно-молекулярные уравнения реакций между растворами
следующих солей: а) сульфатом меди и хлоридом бария; б)сульфатом натрия и нитратом свинца; в) сульфатом железа (II) и гидроксидом лития; г)нитратом серебра и хлоридом железа (III); д) сульфидом натрия и серной кислотой; е) нитратом свинца (II) и раствором сероводорода.
4. Составьте молекулярные и ионные уравнения следующих реакций и укажите в каждом отдельном случае причину, вызывающую смещение равновесия:
а) Pb(NO3)2 + KI = б) AlBr3 + AgNO3 = в) Cr2(SO4)3 + KOH=
г) Al(OH)3 + KOH = д) CaSO4 + BaCl2 = е) Pb(NO3)2 + H2S =
5. Написать молекулярные уравнения реакций, выраженных следующими молекулярно-ионными уравнениями:
а) Pb2+ + 2Cl- = PbCl2 б) CH3COO- + H+ = CH3COOH. в) Ba2+ + SO42- = BaSO4 г) CN- + H+ = HCN
д) Mn2+ + S2- = MnS е) Sn2+ + 2OH- = Sn(OH)2
6. С помощью молекулярных и ионно-молекулярных уравнений ответить на вопросы: а) растворы каких солей надо смешать для получения в осадке карбоната кальция? б) можно ли карбонат кальция перевести в сульфат кальция действием на него сульфата натрия (ПРCaSO4 = 2,5×10-5; ПРCaCO3 =3,8 10-9)?
7. Будут ли протекать реакции между растворами следующих электролитов: а)Ba(OH)2 и HNO3; б) (NH4)2SO4 и KOH; в) CuSO4 и NaOH? Написать молекулярные и ионно-молекулярные уравнения возможных реакций.
8. С помощью молекулярных и ионно-молекулярных уравнений ответить
на вопросы: а) растворы каких солей надо смешать для получения
в осадке сульфата бария? б) можно ли сульфат бария перевести в сульфат стронция действием на него хлорида стронция?
ПР BaSO4 = 1,1•10-10; ПР SrSO4=3,2• 10-7.
9. Написать молекулярные и ионно-молекулярные уравнения реакций между растворами следующих электролитов: а) сульфата натрия и серной кислоты; б) хлорида цинка и гидроксида калия; в) карбоната калия и соляной кислоты.
10. Смешивают попарно растворы: а) NaOH и KCl; б) K2SO3 и HCl;
в)CuCl2 и Ba(OH)2; г)H2SO4 и HCl. В каких случаях реакции идут до конца?
11. Написать в ионно-молекулярной форме уравнения реакций образования соединений, менее растворимых, чем исходные:
а) SrSO4 + BaCl2; б)AgCl +K2S; в) CaCl2 + Na3PO4.
12. Написать в молекулярной и ионно-молекулярной форме уравнения реакций, приводящих к образованию малодиссоциирующих соединений:
а) Na2S + H2SO4; б) NH4Cl + КOH; в) К2S + HCl.
13. Написать в молекулярной и ионно-молекулярной форме уравнения реакций нейтрализации и указать, какая из них протекает практически до конца. а) H2SO4 + NaOH; б) HCN + KOH; в) NH4OH + H2SO4.
14. Можно ли приготовить раствор, содержащий одновременно следующие пары веществ: а) NaOH и Ca(OH)2; б) Sn(OH)2 и NaOH; в) Sn(OH)2 и HNO3?
15. Написать в молекулярной и ионно-молекулярной форме уравнения реакций, приводящих к образованию малорастворимых соединений или
газов:
а) Pb(NO3)2 + KI; б) K2CO3 + HCl; в) NiCl2 + H2S.
16. Можно ли приготовить раствор, содержащий одновременно следующие пары веществ: а) CuSO4 и NaNO3; б) Na2CO3 и HCl; в) AgNO3 и NaCl? Ответ обосновать с помощью молекулярных и ионных уравнений.
17. Можно ли приготовить раствор, содержащий одновременно следующие пары веществ: а) Zn(OH)2 и KOH; б) Ba(OH)2 и HCl; в) Fe(OH)3 и NaOH Приведите возможные реакции в молекулярном и ионно-молекулярном виде.
18. С помощью молекулярных и ионно-молекулярных уравнений ответить на вопросы: а) растворы каких солей надо смешать для получения в осадке хлорида серебра?
б)можно ли хлорид серебра (I) перевести в сульфат серебра действием на него сульфата натрия (ПР AgCl= 1,79×10-10, ПР Ag2SO4 = 1,×10-5). Ответ обосновать.
19. Смешивают попарно растворы следующих электролитов:
а) Cu(NO3)2 и Na2SO4; б) BaCl2 и K2SO4; в) KNO3 и NaCl; г) AgNO3 и KCl. В каких из приведенных случаев реакция практически пойдет до конца? Составьте для этих реакций молекулярные и ионно-молекулярные уравнения.
20. Составьте молекулярные уравнения к каждому из ионно-молекулярных уравнений:
а) Сa2+ + CO32- =CaCO3¯; б) Fe3+ + 3OH- = Fe(OH)3¯.
21. Написать в молекулярной и ионно-молекулярной форме уравнения реакций между: а) сульфидом марганца (II) и серной кислотой; б) гидроксидом свинца (II) и гидроксидом калия; в) гидроксидом магния и раствором хлорида аммония; г) карбонатом кальция и соляной кислотой.
22. Написать молекулярные и ионно-молекуляpные уравнения реакций:
а) растворения карбоната кальция в соляной кислоте; б) взаимодействия растворов нитрата бария и сульфата натрия; в) взаимодействия растворов хлорида железа (III) и гидроксида аммония.
23. К каждому из веществ: AlCl3, H2SO4, Ba(OH)2, FeCl3 прибавили раствор гидроксида калия. В каких случаях произошли реакции? Выразить их молекулярными и ионно-молекулярными уравнениями.
24. Написать в молекулярной и ионной формах уравнения реакций между:м: а) уксусной кислотой и гидроксидом натрия; б) сероводородной кислотой и гидроксидом бария; в) фтористоводородной кислотой и гидроксидом натрия; г) азотной кислотой и гидроксидом аммония.
25. Написать в молекулярной и ионной форме уравнения реакций между: а) сульфидом цинка и соляной кислотой; в) сульфатом аммония и гидроксидом калия.
26. К каждому из веществ KHCO3, CH3COOH, BaCl2, Na2S прибавили раствор серной кислоты. В каких случаях произошли реакции? Выразить их молекулярными и ионно-молекулярными уравнениями.
27. К каждому из веществ Na2CO3, Fe(OH)3, NaNO3, KHS прибавили раствор соляной кислоты. В каких случаях произошли реакции? Выразить их молекулярными и ионно-молекулярными уравнениями.