8.1. Молекулярная диффузия
Процессы теплообмена в смеси часто сопровождаются переносом массы одного компонента относительно массы другого. Компонентами называют вещества, наименьшее число которых достаточно для образования всех фаз данной системы.
Перенос вещества в смеси, обусловленный тепловым движением микрочастиц, называют молекулярной диффузией. Это самопроизвольный процесс, приводящий к установлению внутри фаз равновесного распределения концентраций компонентов.
В однородной по температуре и давлениюсмеси процесс диффузии направлен к выравниванию концентраций,при этом происходит перенос компонента из области большей концентрации в область меньшей. Аналогично теплообмену диффузия (массообмен) может происходить как молекулярным (микроскопическим), так и молярным (макроскопическим) путем.
Диффузия характеризуется потоком массы вещества, то есть массой данного компонента смеси, проходящей в единицу времени через произвольную поверхность в направлении нормали к ней (J, кг/с). Поток массы, отнесенный к единице площади поверхности, называют плотностью потока массы (j, кг/(с∙м2)). Величины J и j – векторы.
 . .
| (8.1) |
Отсюда 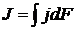 или при
или при  ,
,  .
.
Различают местную (локальную) и среднюю (осреднённую по поверхности) плотность потока массы.
В однородной по температуре и давлению макроскопически неподвижной двухкомпонентной смеси плотность потока массы одного из компонентов за счет молекулярной диффузии определяется законом Фика

| (8.2) |
или
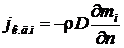
| (8.3) |
где r I – местная концентрация компонента, равная отношению его массы к соответствующему объёму смеси, кг/м3
mi = r i /r – относительная массовая концентрация i -го компонента;
r – плотность смеси, кг/м3
D – коэффициент молекулярной диффузии одного компонента смеси относительно другого (кратко – коэффициент диффузии), м2/с.
¶r i /¶ n и ¶ mi /¶ n – градиенты концентраций и относительной концентрации.
Коэффициент диффузии зависит от параметров состояния смеси. Он увеличивается с ростом температуры и уменьшается с ростом давления. В бинарной смеси коэффициент диффузии одинаков для обоих компонентов.
Градиент концентрации является движущей силой, вызывающей перенос компонента в смеси. Он направлен в сторону увеличения концентрации, а поток массы – в сторону уменьшения концентрации, чем и обусловлено наличие знака минус в уравнениях (8.2) и (8.3).
Математическая формулировка закона Фика аналогична формулировке закона Фурье (1.), при этом коэффициент диффузии D аналогичен коэффициенту теплопроводности l, а градиент концентрации ¶r i /¶ n – градиенту температуры ¶ t /¶ n. Диффузию, подчиняющуюся закону Фика, называют концентрационной диффузией.
Воспользовавшись уравнением состояния идеального газа, можно преобразовать уравнение (8.2) к виду

| (8.4) |
где рi – локальное парциальное давление i -го компонента, Па;
n – направление нормали к поверхности равных значений рi;
Dp,i = D/RiT –коэффициент диффузии, отнесенный к градиенту ¶ рi /¶ n.
В отличие от величины D коэффициент Dp,i различен для компонентов смеси ввиду различия их газовых постоянных; размерность Dp,i – секунда.
Если температура в разных частях объёма смеси различна, то возникает так называемая термическая диффузия (эффект Соре). При этом более тяжелые либо более крупные молекулы стремятся перейти в холодные области (а в ионизированном газе более тяжелые молекулы и ионы стремятся перейти в более теплые области). Термодиффузия приводит к образованию градиента концентраций, однако этому препятствует концентрационная диффузия.
Явление, обратное термодиффузии, называют диффузионным термоэффектом (эффектом Дюфо). Он представляет собой возникновение разности температур в результате диффузионного перемещения двух компонентов, первоначально имевших одинаковую температуру. При этом разность температур может достигать нескольких градусов. Возникающий при диффузионном термоэффекте градиент температур имеет такое направление, что вызванная им термодиффузия противоположна диффузии, благодаря которой появился этот градиент.
Если в смеси имеет место градиент полного давления, то может возникнуть диффузия за счет неоднородности давления – бародиффузия. При этом тяжёлые молекулы стремятся перейти в область повышенного давления, а легкие – в область пониженного. Такая диффузия наблюдается при вращении смеси газов, когда более тяжёлые молекулы под действием центробежных сил перемещаются в область, удаленную от центра вращения. Бародиффузия используется, в частности, при разделении изотопов урана с помощью центрифуг. Бародиффузии сопутствует и термоэффект, то есть возникает разность температур в различных частях смеси.
С учетом трех рассмотренных видов диффузии плотность потока массы i- го компонента за счет молекулярного переноса описывается уравнением
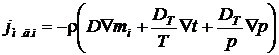 , ,
| (8.5) |
где DT = kTD – коэффициент термодиффузии, м2/с
Dб = kбD – коэффициент бародиффузии, м2/с
t и p – температура и давление смеси.
В этом уравнении первый член суммы учитывает концентрационную диффузию, второй – термодиффузию, третий – бародиффузию. При grad t = 0иgrad р =0уравнение (8.5) переходит в уравнение закона Фика (8.3).
Коэффициент kT называется термодиффузионным отношением, а kб – бародиффузионным отношением. Для бинарной смеси величина kT обычно не превышает 0,1, а величина kб определяется из соотношения
 , ,
| (8.6) |
где М 1, М 2 и М – молекулярные массы компонентов и смеси.
Бародиффузия проявляется при значительных перепадах давления, а при равенстве молекулярных масс компонентов отсутствует.
8.2. Конвективная диффузия
В движущейся смеси компоненты переносятся не только молекулярной диффузией, но и конвекцией. При перемещении объёма смеси 1м3 плотностью r со скоростью w плотности потока массы смеси и i- го компонента соответственно равны j = r w и j к. i = r iw.
Суммарная плотность потока массы i- го компонента за счет молекулярного и конвективного переноса равна
 . .
| (8.7) |
При этом вместе с массой переносится энтальпия jihi, где  – удельная энтальпия i- го компонента. Более того, если через выделенную в смеси поверхность нет потока массы, суммарный поток энтальпии может иметь место, так как в принципе h 1 ≠ h 2.
– удельная энтальпия i- го компонента. Более того, если через выделенную в смеси поверхность нет потока массы, суммарный поток энтальпии может иметь место, так как в принципе h 1 ≠ h 2.
Таким образом, суммарная плотность теплового потока в смеси описывается уравнением
 . .
| (8.8) |
Преобразовав второй член уравнения (8.8), можно представить его в виде
 . .
| (8.9) |
Первый член правой части уравнения (8.9) учитывает перенос теплоты теплопроводностью, второй – конвекцией, третий – молекулярной диффузией, то есть в смеси появляется диффузионная составляющая теплового потока.
Из уравнения (8.9) следует, что для определения полного теплового потока смеси надо знать поля температур, скоростей и потоков массы. Поэтому к системе дифференциальных уравнений, описывающих конвективный теплообмен, необходимо добавить дифференциальное уравнение массообмена. Для его вывода выделяют в смеси элементарный параллелепипед с ребрами dx, dy, dz и, считая D и r постоянными, записывают для него уравнение баланса массы. В итоге получают
 , ,
| (8.10) |
или в сокращенной форме
 . .
| (8.11) |
Уравнения массообмена (8.10) и (8.11) описывают распределение массы i -го компонента в движущейся смеси. Они представляют собой уравнения сохранения массы этого компонента.
Если wx = wy = wz = 0, уравнение массообмена принимает вид
 . .
| (8.12) |
В уравнении (8.12) учтен перенос массы только концентрационной диффузией. Это уравнение аналогично дифференциальному уравнению теплопроводности ¶ t /¶t = a Ñ2 t.
Диффузионный перенос теплоты в бинарной смеси диффундирующих друг в друга компонентов учитывает уравнение энергии
 . .
| (8.13) |
Согласно этому уравнению температурное поле движущейся смеси зависит как от составляющих скорости, входящих в выражение для dt/d τ так и от массовой концентрации.
Дифференциальные уравнения массообмена и энергии совместно с уравнениями движения и сплошности смеси дают полное математическое описание процесса конвективной диффузии. Естественно, для описания конкретного явления необходимо к системе дифференциальных уравнений добавлять условия однозначности. Из анализа системы уравнений методами теории подобия находят связь между переменными, характеризующими процесс массоотдачи, в виде уравнений подобия.
8.3 Тепло- и массоотдача
По аналогии с конвективным теплообменом перенос вещества в многокомпонентной среде, осуществляемый процессами молекулярной диффузии и конвекции, называют конвективным массообменом. Аналогично теплоотдаче конвективный массообмен между жидкой либо твёрдой поверхностью и окружающей средой называют массоотдачей.
В рассматриваемых случаях тепло- и массоотдача протекают одновременно. Процесс теплоотдачи описывает уравнение Ньютона-Рихмана
 . .
| (8.14) |
Для расчетов массоотдачи применяют уравнение
 , ,
| (8.15) |
где b – коэффициент массоотдачи, отнесенный к разности концентраций диффундирующего вещества, м/с;
r i ,c и r i ,0 – концентрация i -го компонента у поверхности раздела сред и вдали от неё.
Используя уравнение состояния идеального газа, можно преобразовать уравнение (8.15) к виду
 , ,
| (8.16) |
где b р = b/ RT – коэффициент массоотдачи, отнесенный к разности парциальных давлений, с/м.
Как видно из вышеизложенного, математические описания процессов теплообмена и массообмена идентичны. В этом состоит аналогия процессов теплообмена и массообмена, которую часто используют на практике. Как известно, при теплообмене (в условиях вынужденного движения жидкости) справедливо следующее уравнение подобия
 . .
| (8.17) |
Тогда по аналогии полагают, что при массообмене справедлива зависимость
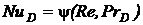 , ,
| (8.18) |
где функции y и f идентичны.
В уравнении (8.18) Nu D =b l / D – диффузионное число Нуссельта, а Pr D =n/ D – диффузионное число Прандтля. Эти числа являются аналогами чисел Nu и Pr.
Аналогия процессов тепло- и массообмена позволяет использовать большую информацию, накопленную в теории теплообмена, для расчета менее изученных процессов массообмена.
8.4. Тепло- и массообмен при фазовых переходах
Большой практический интерес представляют процессы тепло- и массообмена при испарении жидкости и конденсации пара. Испарение жидкости со свободной поверхности обусловлено тепловым движением молекул жидкости. Из общего количества молекул, вылетевших из жидкости, часть распространяется в окружающей парогазовой среде диффузией и конвекцией, а часть возвращается назад. Отношение числа молекул, окончательно потерянных жидкостью, к общему количеству вылетевших молекул называется коэффициентом испарения.
Если вдали от жидкости газ не насыщен паром, возникает поток вещества, направленный от поверхности испарения. Поток теплоты может быть направлен как от жидкости к парогазовой среде, так и в противоположном направлении в зависимости от соотношения температур поверхности жидкости и среды. На испарение жидкости затрачивается теплота r∙j п.пов, Вт/м2, где r – теплота испарения. Если к жидкости подводится меньше теплоты, чем затрачивается на испарение, происходит охлаждение жидкости.
Предположим, что при испарении жидкости из открытого теплоизолированного сосуда в ненасыщенную парогазовую смесь вначале температура поверхности жидкости выше температуры смеси. Вследствие теплоотдачи и испарения температура жидкости будет уменьшаться. Когда температура поверхности жидкости станет равной температуре парогазовой смеси, теплоотдача прекратится, но испарение продолжится, что приведёт дальнейшему снижению температуры жидкости. Вследствие этого жидкость начнёт получать теплоту от смеси, и при некоторой температуре жидкости t м установится динамическое равновесие между подводом теплоты конвективной теплоотдачей и отводом путём испарения и последующей диффузии.
Таким образом, дальнейшее испарение жидкости при t пов = t м происходит за счет теплоты, получаемой жидкостью путём теплоотдачи от парогазовой смеси. Температура t м –– предельная температура, ниже которой нельзя охладить жидкость при данных условиях. При этом справедливо равенство
 , ,
| (8.19) |
Процесс испарения, при котором вся теплота, передаваемая от парогазовой смеси к жидкости, затрачивается на испарение последней и возвращается к смеси в виде внутренней энергии пара, называют адиабатным испарением, а температуру t м – температурой мокрого термометра. Значение t м можно определить из соотношения (8.19) по формуле
 , ,
| (8.20) |
На практике встречаются и неадиабатные процессы испарения, когда испарившаяся жидкость восполняется такой же жидкостью, имеющей другую температуру (t ж2). Тогда испарение происходит не только за счет теплоты, переданной теплоотдачей от парогазовой смеси, но и за счет теплоты, вносимой дополнительной жидкостью и поступающей извне через ограждения. Для расчета теплоотдачи можно использовать уравнение
 , ,
| (8.21) |
где qT – теплопотери в окружающую среду (либо теплопритоки).
Во втором члене уравнения (8.21) знак плюс берётся при t ж2 < t пов, а знак минус – при t ж2 > t пов.
Рассмотрим процесс молекулярной диффузии при испарении жидкости в парогазовую среду (без учета термо- и бародиффузии). Относительная массовая концентрация пара изменяется от значения m п.с. на поверхности испаряющейся жидкости до значения m п.0. вдали от этой поверхности. Так как сумма относительных концентраций пара и газа равна единице, то справедливо равенство
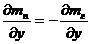 , ,
| (8.22) |
Следовательно, молекулы газа диффундируют в направлении, обратном направлению диффузии пара. Однако если пар свободно диффундирует в парогазовую среду, то для газа поверхность жидкости непроницаема. В случае стационарного тепло- влажностного режима распределение концентраций не изменяется во времени. Поэтому перемещение газа к поверхности должно компенсироваться конвективным потоком парогазовой смеси, направленным от жидкости. Этот поток называется стефановым потоком.

Рис. 8.1. Распределение концентрации пара и газа у поверхности испарения.
Плотность потока пара у поверхности жидкости (стенки) j п.с. равна сумме плотностей молекулярного и конвективного потоков
 , ,
| (8.23) |
где w с.п.с. – скорость стефанового потока у стенки.
Суммарный поток газа у поверхности жидкости равен нулю
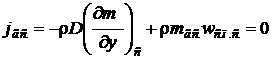 . .
| (8.24) |
Из этого уравнения с учетом соотношения (8.22) получим
 . .
| (8.25) |
Подставив значение w с.п.с в уравнение (8.23) получим окончательно
 . .
| (8.26) |
Уравнение Стефана (8.26) отличается от уравнения Фика (8.3), относящегося к условиям беспрепятственного распространения обоих компонентов смеси, множителем 1/ m г.с.. Он учитывает конвективный (стефанов) поток, вызванный непроницаемостью поверхности испарения жидкости для газа.
Плотность потока массы можно записать также через коэффициент массоотдачи
| (8.27) |
Из уравнения (8.27) можно определить коэффициент массоотдачи b, зная поле концентрации пара.
Рассмотренный процесс соответствует условию поверхности, проницаемой для пара и непроницаемой для газа. Такая же поверхность существует при конденсации пара из парогазовой смеси. При этом условии и стационарном процессе испарения жидкости стефанов поток компенсирует встречный поток газа и реально возникает лишь поток пара. Поэтому плотность теплового потока на границе раздела фаз равна

Рис. 8.2. Распределение концентраций и температуры при конденсации пара из парогазовой смеси.
 , ,
| (8.28) |
При конденсации пара из парогазовой смеси наличие неконденсирующегося газа затрудняет доступ пара к поверхности и уменьшает скорость конденсации. В процессе конденсации выделяется теплота фазового перехода
 . .
| (8.29) |
На поверхности теплообмена образуется плёнка конденсата. Пренебрегая переохлаждением конденсата, можно описать плотность теплового потока на этой поверхности уравнением
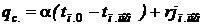 , ,
| (8.30) |
где a – коэффициент теплоотдачи от парогазовой смеси к плёнке конденсата.
Уравнение (8.30) можно представить в виде
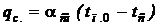 , ,
| (8.31) |
где aсм – коэффициент теплоотдачи, отнесенный к разности температур поверхности конденсации и парогазовой смеси вдали о поверхности.
Коэффициент aсм =1/S R учитывает сумму термических сопротивлений плёнки конденсата R к, фазового перехода R ф и подвода пара к поверхности (диффузионное термическое сопротивление R д). Этим термическим сопротивлениям соответствуют указанные на рис.8.2 разности температур D t к, D t ф и D t д. Из рисунка видно, что
 . .
| (8.32) |
Пренебрегая значением D t ф, можно рассматривать температуру поверхности конденсата t пов как температуру насыщения пара при давлении рп.пов..
Значение коэффициента теплоотдачи aсм зависит от интенсивности взаимосвязанных процессов тепло- и массообмена в парогазовой смеси и в плёнке. Поэтому для расчёта значения aсм необходимо предварительно определять диффузионное число Нуссельта Nu D =b l / D и на его основании – коэффициент массоотдачи b.
 .
.