Билет № 9
Общие правила работы с аптечными бюретками и пипетками
В аптеках выделяют фармацевта, контролирующего состояние и правильную эксплуатацию аптечных бюреток, пипеток и каплемеров в соответствии с Положением о ведомственном надзоре за измерительными приборами в системе МЗ РФ, положениями Инструкции по санитарному режиму аптек.
Перед сборкой все резиновые и стеклянные детали бюреток, пипеток и каплемеров тщательно моют и дезинфицируют в соответствии с требованиями действующей Инструкции.
Аптечные бюретки, пипетки и каплемеры моют по мере надобности, но не реже 1 раза в 10 дней. Для этого их освобождают от жидкостей, моют горячей водой (50 - 60° C), взвесью горчичного порошка или 3% раствором водорода перекиси с добавлением 0,5% моющих, дезинфицирующих и моюще-дезинфицирующих средств, разрешенных для применения в аптечной практике; промывают водой водопроводной и очищенной, с обязательным контролем на полноту смывания моющих средств (в соответствии с нормативной документацией).
Перед началом работы сливные краны, концы бюреток и пипеток очищают от налета солей, настоек, экстрактов и протирают спирто-эфирной смесью (1:1).
Заполняют питающие сосуды в бюреточной установке концентрированными растворами, настойками, экстрактами (концентратами), предназначенными для изготовления водных извлечений. Проверяют правильность их заполнения путем качественного химического анализа в соответствии с требованиями действующей Инструкции.
Малые объемы жидкостей отмеривают бюретками и пипетками с малым диаметром.
Уровень бесцветных жидкостей в бюретках и пипетках устанавливают по нижнему мениску, окрашенных - по верхнему.
Слив жидкостей из пипеток и бюреток производят полностью, после полного стекания жидкости выжидают еще 2 - 3 секунды.
Отмеривание жидкости по разности делений не допускается. Вязкие и летучие жидкости не отмеривают по объему во избежание большой ошибки дозирования.
Не разрешается использовать бюретки, пипетки и каплемеры с отломанными концами, а также с плохо смачивающейся внутренней поверхностью стенок.
Малые количества жидких лекарственных средств (менее 1 мл или 1 г) дозируют каплями. При отсутствии стандартного каплемера (ГФ) последний может быть заменен эмпирическим каплемером - пипеткой, откалиброванной путем пятикратного взвешивания 20 капель соответствующего жидкого лекарственного средства.
На этикетке штангласа (флакона) с прикрепленным каплемером следует указать наименование лекарственного средства, число капель в 1 мл или 1 г и соответствие 1 капли стандартного каплемера числу капель нестандартного.
2. Дать определение,выполнить расчеты и описать технологию изготовления, контроля и оформление следующей прописи:
Rp: Kalii bromidi 5.0
Natrii bromidi 4.0
Kalii iodidi 6.0
Tincturae Valerianae 10 ml
Aquae purificatae 200 ml
Misce. Da. Signa По 1 ctоловой ложке 3 раза в день
В рецепте выписана микстура, дозируемая ложками. Общий объем рассчитывается по сумме всех входящих в состав микстуры жидких ингредиентов. Лекарственные средства (сухие) используют в виде растворов-концентратов.
ППК (оборотная сторона):
V20% раствора концентрата калия бромида (1:5)=5,0*5=25 мл
V10% раствора концентрата натрия бромида (1:10) =4,0*10=40 мл
V20% раствора концентрата калия йодита (1:5) = 6,0*5=30 мл
Vнастойки валерианы =10 мл
Vводы очищенной = 200-25-40-30=105 мл
Vобщ =10+200=210мл
Технология: микстуру изготавливают во флаконе для отпуска. Отмеривают 105 мл воды очищенной, добавляют из бюреточной установки 25 мл 20% раствора калия бромида, 40 мл 10% раствора натрия бромида и 30 мл 20% раствора калия йодида, перемешивают и, если нет механических включений, добавляют 10 мл настойки валерианы. Оформляют к отпуску.
ППК (лицевая сторона):
Дата _____ № рецепта ____
Aquaepurificutaе 105 ml
Sol. Kalii bromidi 20% 25 ml
Sol. Natrii bromidi 10% 40 ml
Sol. Kalii iodidi 20% 30 ml
Tincturae Valerianae 10 ml
Vo6щ = 210 мл
Приготовил: (подпись)
Проверил: (подпись)
Методы количественного анализа лекарственных средств. Бромометрия и броматометрия. Химизм, индикаторы, конкретные примеры
Броматометрический метод основан на окислении восстановителей броматом калия в кислой среде. При восстановлении бромат переходит в бромид:
ВrО-3 + 6Н+ + 6ē →Вr- + 3Н2О.
Стандартным раствором служит 0,1 н. раствор бромата калия. Этот раствор готовят по точной навеске чистого, перекристаллизованного бромата калия и высушенного при 150 °С бромата калия. Как видно из уравнения, фактор эквивалентности (f экв) равен 1/6, тогда его молярная масса эквивалента равна 1/6 молярной массы:
М(1/6КВrО3) = 167,00 / 6 =27,83 г/моль.
Водные растворы бромата калия устойчивы, они не изменяют свою концентрацию в течение длительного времени (около 6 мес). Для проверки концентрации приготовленного раствора бромата калия используют метод йодометрии. С этой целью к раствору приливают раствор йодида калия и выделившийся йод титруют тиосульфатом натрия.
При титровании броматом калия первая лишняя капля бромата вступает в реакцию с образующимся в растворе бромидом. Выделяется свободный бром, который может быть обнаружен по появлению желтой окраски:
BrO-3 + 5Вr- + 6Н+ → 3Вr2 + 3Н2О.
Однако без использования индикаторов эквивалентную точку нельзя зафиксировать достаточно точно. Поэтому для определения конца титрования применяют азоиндикаторы, например метиловый красный или метиловый оранжевый. При достижении эквивалентной точки эти индикаторы окисляются выделившимся бромом и разрушаются: цвет раствора из красного переходит в бледно-желтый. Переход окраски связан с разрушением индикатора, поэтому этот процесс необратим. При быстром добавлении бромата калия окраска может исчезнуть раньше достижения точки эквивалентности. В этом случае рекомендуется к концу титрования добавлять еще несколько капель индикатора и проводить осторожное добавление окислителя.
Для увеличения скорости реакции титрование броматом проводят при нагревании раствора до 80 °С.
Броматометрию применяют для определения мышьяка (III), сурьмы (III), железа (III), пероксида водорода и др. Броматометрию используют также в анализе органических соединений. Броматом можно непосредственно титровать тиомочевину, тиоэфиры, щавелевую кислоту и другие соединения.
Бромометрия, или бромат - бромидный метод основан на окислении восстановителей свободным бромом:
Вr2 + 2ē ↔ 2Вr -.
Некоторые вещества непосредственно не реагируют с броматом, но количественно реагируют с бромом. При добавлении избытка бромида и кислоты к определенному количеству раствора бромата калия с точно известной концентрацией выделяется эквивалентное количество брома:
КВrО3 + 5КВг + 6НС1 = ЗВг2 + 6КС1 + ЗН2О.
Таким образом может быть получен раствор брома точно определенной концентрации. Выделившийся бром вступает в реакцию бромирования со многими органическими веществами, особенно с теми, которые содержат в своем составе одну или несколько фенольных групп: фенол, резорцин, тимол, салициловая кислота и др. Например, при бромировании фенола количественно образуется трибромфенол и бромоводородная кислота:
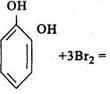
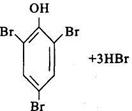
При бромометрическом определении применяют различные способы титрования: прямое, косвенное и обратное.
В случае определения фенола к анализируемому раствору добавляют бромид калия и хлороводородную кислоту и титруют 0,1000 н. раствором бромата калия в присутствии метилового оранжевого. Для определения фенола и резорцина в фармацевтическом анализе используется метод заместительного титрования. К раствору анализируемого вещества добавляется определенный объем раствора КВrО3, КВr и НСl. Смесь оставляют на 10 мин. За это время происходит реакция бромирования вещества выделившимся свободным бромом. Избыток не прореагировавшего брома определяют, добавляя к смеси раствор KI. Бром количественно вытесняет йод из KI. Выделившийся йод титруют раствором Na2S2O3.
Таким образом, при определении фенолов (например, резорцина) протекают четыре химические реакции:
1) КВrО3 + 5КВr + 6НСl = 3Вr2 + 6Сl + 3H2O
2)
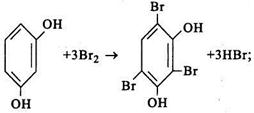
3) 2KI + Вr2 = I2 + 2КВr;
4) I2 + 2Na2S2O3 = 2NaI + Na2S4O6.
Метод используется также для определения многих ионов металлов (магния, алюминия, меди, кадмия) в присутствии 8-оксихинолина.