Лабораторная работа № 3
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ВИТАМИНА С.
Качественная реакция на витамин С.
Витамин С существует в окисленной (L–дегидроаскорбиновая кислота) и восстановленной (L–аскорбиновая кислота) формах. Несмотря на это, его называют аскорбиновой кислотой. Обе формы витамина С обладают биологической активностью, участвуют в ферментативных окислительно-восстановительных реакциях, в частности, в окислении молочной, лимонной и других оксикислот; в гидроксилировании остатков пролина и лизина в молекуле проколлагена с образованием гидроксипролина и гидроксилизина в молекулах коллагена и эластина. Биохимическая функция аскорбиновой кислоты окончательно не известна.
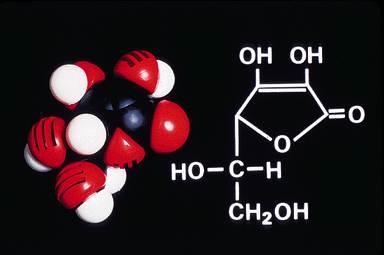
Человек, приматы и морские свинки не способны синтезировать аскорбиновую кислоту и должны получать ее с пищей. Большинство других видов животных и, вероятно, все растения могут синтезировать это соединение из глюкозы. Микроорганизмы не содержат аскорбиновой кислоты и не нуждаются в ней.
Источником витамина С для человека служат самые разнообразные продукты растительного происхождения. Особенно много ее содержат черная смородина, плоды шиповника, хвоя ели и сосны, капуста, картофель, облепиха, рябина, красный перец, лимоны, черемша и др.
Определение витамина С основано на его способности легко вступать в окислительно-восстановительные реакции, восстанавливать, например, метиленовую синь, 2,6-дихлофенолиндофенол натрия (краску Тильманса), гексациано-(III)-феррат калия, нитрат серебра, йод и др.
ХОД РАБОТЫ. В три пробирки вносят по 10 капель дистиллированной воды и по 3 капли: в первую и третью – раствора 2,6-дихлорфенолиндофенола (индофенолового реактива), во вторую – раствора Люголя. Затем в первую пробирку добавляют 5 капель вытяжки хвои, во вторую – 5 капель 0,5% раствора аскорбиновой кислоты, в третью – воды (контроль). В пробирках с вытяжкой хвои и аскорбиновой кислоты растворы индофенолового реактива и Люголя обесцвечиваются.
Определение содержания витамина С в растительном материале.
Берут навеску исследуемого материала 5-20 г (в зависимости от предполагаемого содержания аскорбиновой кислоты), нарезают мелкими кусочками (картофель, морковь, яблоки и т.п.), тщательно растирают в ступке со щепоткой стекла или кварцевого песка, добавляют порциями по 4-5 мл раствора (с массовой долей соляной кислоты 2 %) до получения однородной жидкой кашицы. Смесь из ступки количественно, с помощью раствора используемой при растирании кислоты, переносят в мерную колбу вместимостью 100 мл и общий объем экстракта доводят до метки тем же раствором кислоты. Содержимое хорошо перемешивают, настаивают 5-7 мин и фильтруют через бумажный фильтр. Полученный фильтрат должен быть совершенно прозрачным.
Используемые для экстракции кислоты (соляная, метафосфорная, щавелевая) извлекают из исследуемого материала как свободную, так и связанную аскорбиновую кислоту, а также способствуют устойчивости аскорбиновой кислоты в экстрактах.
Берут две конические колбочки вместимостью 100-150 мл и в одну пипеткой вносят 20 мл полученного фильтрата, в другую – 20 мл раствора кислоты, используемой для растирания исследуемого материала. Содержимое колбочек титруют индофеноловым реактивом до слабо-розового цвета, удерживающегося 30 секунд. Результаты записывают, и титрование повторяют с новыми порциями того же фильтрата. На основании средней величины, полученной из 2-3 определений, рассчитывают содержание аскорбиновой кислоты по формуле:
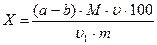 ,
,
где Х – содержание аскорбиновой кислоты в материале, мг/100г продукта;
(a-b) – разность между объемами индофенолового реактива, пошедшими на титрование опытной (а) и контрольной (b) проб, мл;
М – масса аскорбиновой кислоты, соответствующая 1 мл индофенолового реактива, мг;
u - общий объем экстракта, мл;
u1 – объем фильтрата, взятого для титрования, мл;
m – масса исследуемого материала, г,
100 – пересчет на 100г материала.
В растительных тканях в некоторых количествах содержатся и другие редуцирующие вещества, восстанавливающие 2,6-дихлорфенолиндофенол, поэтому при необходимости проведения особо точного анализа следует принять это в расчет. Для этого к двум другим порциям по 10-20 мл исследуемой вытяжки прибавляют по 0,1 или 0,2 мл 10 % раствора сернокислой меди и нагревают в термостате или сушильном шкафу 10 мин при температуре 110 ˚С. Охлаждают и титруют индофеноловым реактивом. В присутствии солей меди и при нагревании аскорбиновая кислота разрушается полностью. Полученную поправку вычитают из данных титрования опытных проб.
При анализе многих плодов и ягод, некоторых овощей получают окрашенные экстракты, что затрудняет определение аскорбиновой кислоты. Для определения аскорбиновой кислоты, окрашенную вытяжку переносят в широкую пробирку, приливают 2-5 мл дихлорэтана или хлороформа и титруют при взбалтывании раствором индофенолового реактива до появления в слое дихлорэтана (или хлороформа) розового окрашивания, неисчезающего 30 сек.
При определении необходимо учитывать редуцирующую способность применяемых для экстракции кислот (смесь 20 мл 1 % соляной кислоты и 80 мл 2 % метафосфорной или 1 % щавелевой кислоты). Для этого две порции смеси кислот по 10 мл титруют индофеноловым реактивом до розового окрашивания. Полученную поправку (обычно не превышающую 0,08-0,10 мл раствора краски) вычитают из данных титрования опытных растворов.