Задание
Рассчитайте и постройте график ТКТ, определите по нему оптимальный индикатор и индикаторную погрешность при титровании:
| ↓ | KOH |
| C6H5COOH |
Кд(C6H5COOH) = 6,3·10-5
Анализ задания
Определяемым веществом в данном титровании является слабая одноосновная бензойная кислота C6H5COOH, а веществом титранта – гидроксид калия, являющийся сильным основанием. Следовательно, данная ТКТ относится к типу протолитических.
Бензойная кислота диссоциирует в одну ступень.
C6H5COOH = C6H5COO- + Н+ Кд(C6H5COOH) = 6,3·10-5
Для простоты расчета ТКТ примем, что на титрование взято 100 см3 раствора C6H5COOH и с(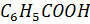 ) = с(КОН) = 0,1 моль/дм3.
) = с(КОН) = 0,1 моль/дм3.
РЕШЕНИЕ
1) До начала титрования в титруемом растворе только слабая бензойная кислота, рН титруемого раствора определяется как
[H+] = 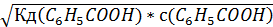 =
= 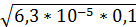 = 2,51*10-3 моль/л
= 2,51*10-3 моль/л
pH = -lg[H+] = 2,6
2) Для случая добавления 10 см3 (10%) титранта:
[Н+] = Кд (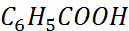 )*
)* 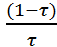
τ = 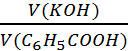
τ = 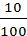 = 0,1
= 0,1
[H+] = 6,3*10-5 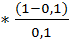 = 5,67*10-4 моль/л
= 5,67*10-4 моль/л
pH = 3,3
τ = 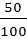 = 0,5
= 0,5
[H+] = 6,3*10-5* 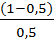 = 6,3*10-5моль/л
= 6,3*10-5моль/л
pH = 4,2
τ = 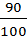 = 0,9
= 0,9
[H+] = 6,3*10-5* 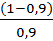 = 6,9*10-6 моль/л
= 6,9*10-6 моль/л
pH = 5,2
τ = 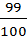 = 0,99
= 0,99
[H+] = 6,3*10-5* 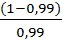 = 6,36*10-7 моль/л
= 6,36*10-7 моль/л
pH = 6,2
τ = 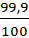 = 0,999
= 0,999
[H+] = 6,3*10-5* 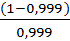 = 6,3*10-8 моль/л
= 6,3*10-8 моль/л
pH = 7,2
3) При добавлении 100 см3 (100 %) раствора титранта наступает момент эквивалентности. В этот момент рН титруемого раствора определяется концентрацией образовавшейся из бензойной кислоты соли C6H5COOK. Эта соль, как соль сильного основания и слабой кислоты, подвергается гидролизу, что приводит к щелочной среде титруемого раствора:
C6H5COOK + H2O = KOH + C6H5COOH
Для соли C6H5COOK
[H+] = 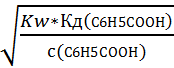 =
= 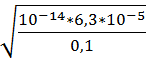 2,5*10-9 моль/л
2,5*10-9 моль/л
pH = 8,6
4) При титровании после ТЭ титруемый раствор будет содержать соль C6H5COOK и избыток добавленного титранта КОН. Как более сильный электролит КОН подавляет диссоциацию C6H5COOK, поэтому после ТЭ рН титруемого раствора определяется только концентрацией избыточного количества КОН. Поскольку среда раствора после ТЭ щелочная, то
[H+] = 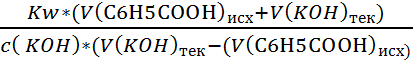
[H+] = 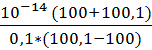 = 2*10-10 моль/л
= 2*10-10 моль/л
pH = 9,7
[H+] = 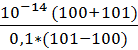 = 2,01*10-11 моль/л
= 2,01*10-11 моль/л
pH = 10,7
[H+] = 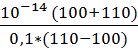 = 2,1*10-12 моль/л
= 2,1*10-12 моль/л
pH = 11,67
[H+] = 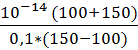 = 5*10-13 моль/л
= 5*10-13 моль/л
pH = 12,3
[H+] = 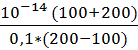 = 3*10-13 моль/л
= 3*10-13 моль/л
pH = 12,57
СВОДНАЯ ТАБЛИЦА РЕЗУЛЬТАТОВ РАСЧЕТА ТКТ
| № точки ТКТ | Добавлено титранта, % | Остаток титруемого р-ра, % | Расчет Н+ моль/л | рН |
| 1 | 0 | 100 | 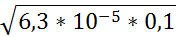 = 2,51*10-3 = 2,51*10-3
| 2,6 |
| 2 | 10 | 90 | 6,3*10-5 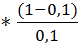 = 5,67*10-4 = 5,67*10-4
| 3,3 |
| 3 | 50 | 50 | 6,3*10-5* 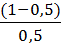 = 6,3*10-5 = 6,3*10-5
| 4,2 |
| 4 | 90 | 10 | 6,3*10-5* 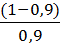 = 6,9*10-6 = 6,9*10-6
| 5,2 |
| 5 | 99 | 1 | 6,3*10-5* 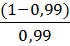 = 6,36*10-7 = 6,36*10-7
| 6,2 |
| 6 | 99,9 | 0,1 | 6,3*10-5* 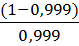 = 6,3*10-8 = 6,3*10-8
| 7,2 |
| 7 | 100 | 0 | 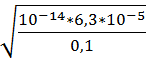 2,5*10-9 2,5*10-9
| 8,6 |
| 8 | 100,1 | 0 | 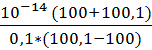 = 2*10-10 = 2*10-10
| 9,7 |
| 9 | 101 | 0 | 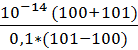 = 2,01*10-11 = 2,01*10-11
| 10,7 |
| 10 | 110 | 0 | 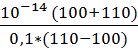 = 2,1*10-12 = 2,1*10-12
| 11,67 |
| 11 | 150 | 0 | 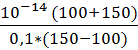 = 5*10-13 = 5*10-13
| 12,3 |
| 12 | 200 | 0 | 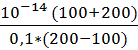 = 3*10-13 = 3*10-13
| 12,57 |
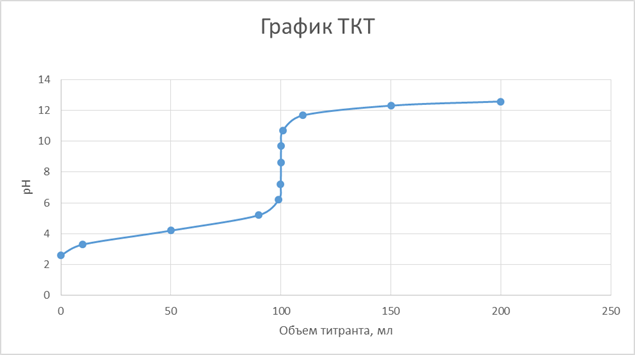
ВЫБОР ИНДИКАТОРА
В соответствии с правилами подбора кислотно-основных индикаторов для регистрации КТТ слабой кислоты подходят индикаторы, изменяющие окраску в щелочной среде и при рН возможно более близком к значению рН в ТЭ. Для слабой кислоты C6H5COOH с рНТЭ = 8,63 по справочнику находим, что в качестве таких индикаторов могут быть использованы:
1) фенолфталеин, рТ=9; рН1...рН2=8,0...10,0; переход окраски от малиновой в щелочной среде до бесцветной в кислой.
2) тимоловый синий, рТ=8,8, рН1...рН2 = 8,0...9,6; переход окраски от синей в щелочной среде до желтой в кислой. 10
3) α-нафтолфталеин, рТ=8, рН1...рН2 = 7,4...8,6; переход окраски индикатора от розовой в кислой среде до зеленой в щелочной среде.
РАСЧЕТ ИНДИКАТОРНОЙ ПОГРЕШНОСТИ
1) для фенолфталеина
Тип индикаторной погрешности определим из графической схемы титрования:

Из графической схемы титрования следует, что использование фенолфталеина приведет к перетитрованию бензойной к-ты сильным основанием КОН и накоплению в титруемом растворе в КТТ ионов ОН-. Это обусловливает гидроксильную индикаторную погрешность. Для этой погрешности:
ΔOH = 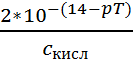 *100 =
*100 = 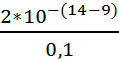 = +0,02%
= +0,02%
Знак "+" у индикаторной погрешности берем, вследствие перетитрования с фенолфталеином.
2) для тимолового синего
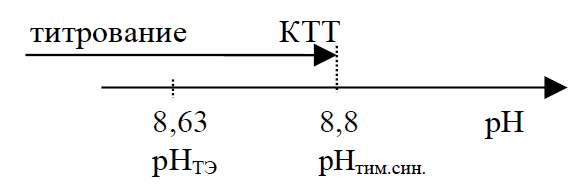
Следовательно, индикаторная погрешность - гидроксильная.
ΔOH = 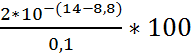 = +0,01%
= +0,01%
3) для α-нафтолфталеин 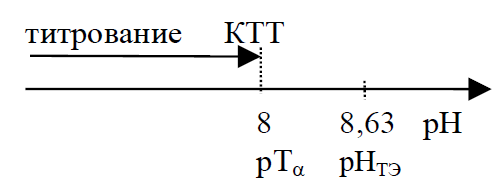 Из схемы следует, что применение α-нафтолфталеина приведет к недотитрованию слабой кислоты и к накоплению ее молекул в титруемом растворе в КТТ. Это обусловливает кислотную индикаторную погрешность:
Из схемы следует, что применение α-нафтолфталеина приведет к недотитрованию слабой кислоты и к накоплению ее молекул в титруемом растворе в КТТ. Это обусловливает кислотную индикаторную погрешность:
ΔН = 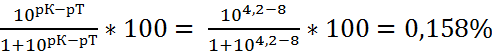
ВЫВОД
1) На графике ТКТ имеется достаточно большой скачок титрования, следовательно, титрование щавелевой кислоты гидроксидом калия возможно при данных концентрациях реагентов.
2) Титрование рекомендуется вести с фенолфталеином, тимоловым синим и
α-нафтолофталеином в качестве индикаторов. Индикаторная погрешность у каждого из них меньше допустимой 0,1%.
3) Оптимальным индикатором является α-нафтолофталеин, т.к. у него наименьшая индикаторная погрешность 0,0158%.