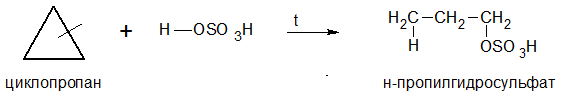Строение, получение и свойства циклоалканов
Циклоалканы (циклопарафины) – органические насыщенные соединения, атомы углерода в молекулах которых, соединяясь, образуют циклы. Общая формула – CnH2n (n≥3). Строение, получение и свойства циклоалканов отличаются от свойств нормальных алканов с тем же числом углеродных атомов.
Строение циклоалканов
В молекулах циклоалканов углеродные атомы связаны между собой σ – связями. Устойчивость циклопарафинов, т.е. прочность С-С связей возрастает с увеличением количества атомов углерода, образующих цикл. Циклы делят на малые (С3, С4) и обычные (C5 – С7).
В качестве представителя малого цикла рассмотрим циклопропан:
· Молекула циклопропана представляет собой плоский цикл, образованный тремя атомами углерода; атомы водорода при этом расположены вне его плоскости и занимают энергетически невыгодное («заслонённое») положение, что способствует увеличению «напряжённости» цикла и его неустойчивости.
· Валентные углы в плоском равностороннем треугольнике принимают значение равное 60°. А для sp3-гибридизованного атома углерода это значение соответствует 109,5°. В случае молекулы циклопропана sp3-гибридизованные орбитали атомов углерода перекрываются между собой вне прямой, соединяющей ядра атомов. Образующиеся σ-связи с подобным способом перекрывания называют «банановыми». Их свойства обладают сходными чертами с π-связями, например, вступают в реакции присоединения.
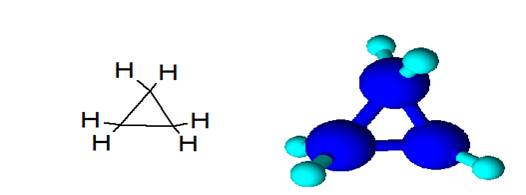
В отличие от трехчленных циклов, устойчивость пяти- и шестичленных циклических алканов настолько высока, что они не способны к разрыву.
В качестве представителя обычного цикла рассмотрим циклогексан.
|
|
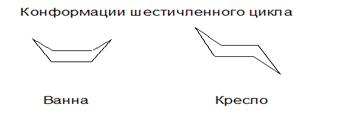
Для молекулы циклогексана не характерно плоское строение, напротив,ей присуще несколько форм — конформаций. Наиболее выгодной с энергетической точки зрения являются конформации кресла (более устойчива) и ванны. Валентные углы, образованные гибридными орбиталями атомов углерода в цикле, равны 109,5°, атомы водорода у соседних атомов углерода расположены относительно друг друга в положении энергетически выгодном.
Тетраэдрическое расположение связей вокруг каждого атома углерода способствует большей устойчивости обычных циклов по сравнению с малыми. Для них возможны реакции замещения и невозможны реакции присоединения.
Физические свойства циклоалканов
При обычных условиях циклоалканы закипают и плавятся при более высоких температурах по сравнению с соответствующими алканами. С увеличением размера цикла температуры кипения и плавления растут. Циклоалканы С3 — С4 представляют собой газы, С5 — С16 — жидкости, C17 и более — твёрдые вещества. Растворимость циклических алканов в воде очень низка.
Получение циклоалканов
· Переработка нефти (получают циклогексан и его производные)
· Реакция отщепления
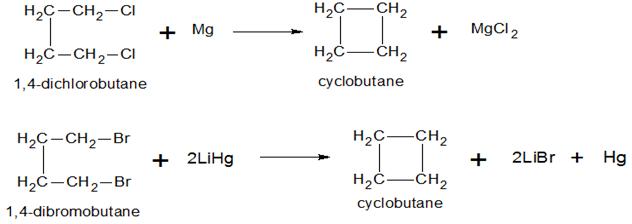
При отщеплении от дигалогенпроизводныхалканов двух атомов галогена получают трёх- и четырёхчленные циклоалканы:
· Реакция гидрирования ароматических углеводородов в присутствии катализатора
При нагревании бензола или его гомологов и водорода в присутствии никелиевого катализатора получают циклогексан или его производные: С6Н6 + 3Н2 → С6Н12 (циклогексан)
Химические свойства циклоалканов
|
|
Устойчивость, а, следовательно, и реакционная активность малых и обычных циклов сильно различаются.
Малые циклы, такие как циклопропан и циклобутан проявляют склонность к реакциям присоединения, тогда как для обычных циклов (циклопентан и циклогексан) более характерны реакции замещения.
Реакции присоединения
· Галогенирование:
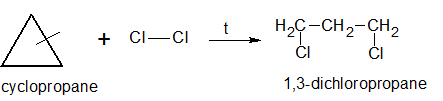
· Гидрогалогенирование:
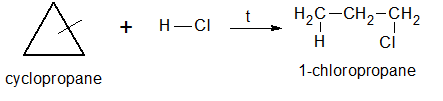
· Гидрирование:
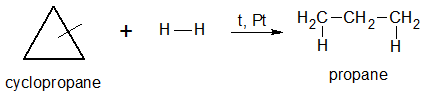
· Расщепление серной кислотой: