Для азотсодержащих гетероциклических соединений с азотом пиридинового типа п-электронная плотность максимальна именно на атоме азота. В качестве иллюстрации можно привести расчётную п-электронную плотность для пиридина:
| Положение атома | Электронная плотность |
| 1 (N) | 1.43 |
| 2 (α) | 0.84 |
| 3 (β) | 1.01 |
| 4 (γ) | 0.87 |
Соответственно, атаки электрофилов в этом случае направляются на пиридиновый атом азота. В качестве электрофилов могут выступать разнообразные алкилирующие и ацилирующие агенты (реакция кватернизиции с образованием соответствующих четвертичных солей) и пероксикислоты (с образованием N-оксидов).
Атом азота пиррольного типа значительно менее нуклеофилен — алкилирование N-замещенных имидазолов идёт преимущественно по азоту пиридинового типа, однако, при депротонировании незамещённого пиррольного азота направление замещения обращается. Так, 4-нитроимидазол при метилировании в нейтральных условиях даёт в основном 1-метил-5-нитроимидазол, а в щелочных растворах (где субстратом является его депротонированная форма) главным продуктом реакции оказывается 1-метил-4-нитроимидазол.
Такое повышение нуклеофильности азота пиррольного типа при депротонировании типично для всех гетероароматических соединений, однако направление атаки электрофила зависит от степени диссоциации образующегося аниона: если индолил- и пирролилмагнийгалогениды подвергаются электрофильной атаке преимущественно по углероду, то соответствующие соли щелочных металлов реагируют в основном по атому азота. Подтверждением влияния диссоциации комплекса N-анион — металл на направление реакции является обращения направления электрофильной атаки при реакции индолилмагнийгалогенидов с метилйодидом в ГМФТАвследствие промотируемой растворителем диссоциации магниевого комплекса.
Электрофильность
Электрофильность гетероароматических соединений растёт при падении п-электронной плотности, то есть при увеличении числа гетероатомов и, при их равном числе, выше для шестичленных, по сравнению с пятичленными, гетероциклами. Так, для пирролов и индолов реакции нуклеофильного замещения атипичны, пиридин и бензимидазол аминируются амидом натрия, а 1,3,5-триазин быстро гидролизуется до формиата аммония уже в водном растворе.
Реакционная способность заместителей и боковых цепей
Реакционная способность неароматических гетероциклических близка к таковой их ациклических аналогов с поправкой на стерические эффекты.
В случае гетероароматических соединений на реакционную способность боковых цепей существенно влияют мезомерные эффекты. Кислотность метиленовых водородов в 2- и 4-замещённых пиридинах существенно повышена: так, альдольная конденсация 2-метилпиридина (α-пиколина) с формальдегидом с образованием 2-этоксиэтил-2-пиридина с последующей его дегидратацией служит промышленным методом синтеза 2-винилпиридина.
Строение и номенклатура
Ароматические гетероциклы представляют собой плоские циклические системы, содержащие вместо одного или нескольких атомов углерода атомы кислорода, серы, азота. Ароматическими их называют вследствие того, что они удовлетворяют всем критериям, присущим любой ароматической системе, а именно:
• система является циклической;
• цикл является плоским;
• имеется сопряжение по всему циклу, то есть возможность беспрепятственной делокализации любого из p-электронов по всей системе, благодаря наличию негибридизованных р-орбиталей;
• число делокализованных p-электронов, участвующих в сопряжении, отвечает, согласно правилу Хюккеля, проявлению ароматических свойств, а именно, равно 4n+2, где n – любое натуральное число, включая 0.
Среди ароматических гетероциклических соединений наиболее широко распространены и, соответственно, представляют наибольший интерес 5- и 6-членные гетероциклы, имеющие в своем составе азот, серу и кислород, а также эти же системы, конденсированные с бензольным кольцом.
К пятичленным циклическим системам с одним гетероатомом относятся пиррол, фуран и тиофен:

Из пятичленных гетероциклов с двумя гетероатомами наибольший практический интерес представляет имидазол.
К конденсированным с бензольным кольцом пятичленным гетероциклам относятся 2,3-бензопиррол (индол, I), 3,4-бензопиррол (изоиндол, II), бензимидазол (III), бензофуран (IV) и 2,3-бензотиофен (V):

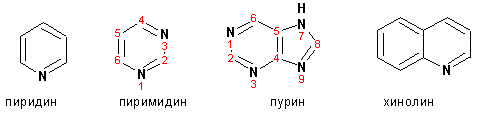
Наиболее важными из шестичленных гетероциклов являются пиридин, пиримидин, хинолин (бензопиридин) и пурин:
Биологическое значение
Гетероциклические соединения широко распространены в живой природе и имеют важное значение в химии природных соединений и биохимии. Функции, выполняемые этими соединениями весьма широки — от структурообразующих полимеров (производные целлюлозы и других циклических полисахаридов) до коферментов и алкалоидов.