Кроме металлов для изготовления различных технических изделий в настоящее время используют разные не металлические материалы:
· Полимеры
· Неорганическое стекло
· Ситалл
· Керамика: углеродная, графитовая, сверхтвердая, пористая, порошковая
· Композиционные материалы и др.
Полимеры - высокомолекулярные вещества с очень большой молекулярной массой (105 – 107)
Основа структуры полимеров – макромолекулы.
Молекула – наименьшая частица вещества, обладающая его основными химическими свойствами и состоит из атомов, соединённых между собой химическими связями.
Число атомов в молекулах – от 2 до 100 и до 1000. Наиболее общие характеристики молекул – молекулярная масса, состав и структурная формула, которая указывает последовательность химических связей.
Макромолекула (молекулярный полимер вещества) – состоит из 1000 и более повторяющихся единиц (одинаковые или близкие по строению группы атомов)
Химическое строение макромолекулы практически соответствует химическому строению структурной единицы.
Элементы макромолекулы – основная цепь, составное звено, боковые группы.
Основная цепь полимера – последовательность химически связанных атомов, длина которой значительно превосходит длину боковых групп.
Составное звено – выделяемая группа атомов, с помощью которой можно описывать строение всей цепи макромолекул. Если число составных звеньев в макромолекулы ПМ:
| число составных звеньев в макромолекулы ПМ | |||
| 1500-2000 | 200 000-300 000 | ||
| Полиэтилен (ПЭ) | Густая жидкость | Твердый, но эластичный | Твердое вещество в стеклообразном состоянии |
Боковые группы (радикалы)
· Могут быть атомы (водород, галогены);
· Группы атомов (-ОН; -СN; - С6Н5 и т.д.);
· Отрезки полимерных молекул, разной длины
Боковые группы могут располагаться вдоль основной цепи беспорядочно или иметь упорядоченную расстановку. Таки полимеры называются регулярными.
Полимер- вещество, которое характеризуется многократным повторением одного или более составных звеньев, которые соединены между собой в количестве достаточном для проявления комплекса свойств, который остается практически неизменным при добавлении или удалении одного, или нескольких составных звеньев.
Схема №1. Строение полимерной макромолекулы полимера.
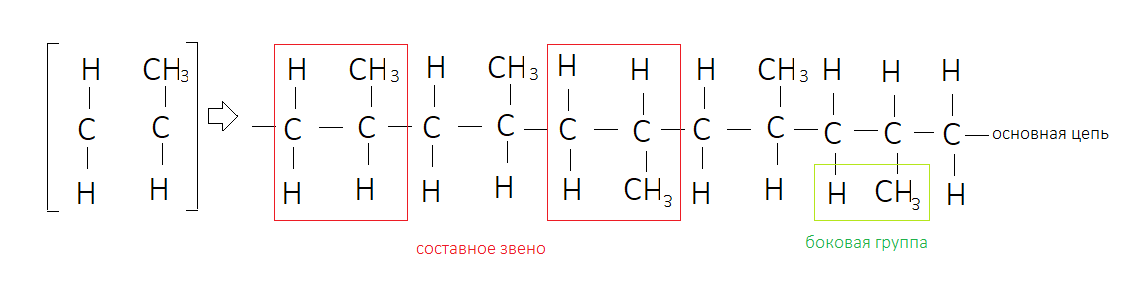
По химическому составу основной цепи полимеры делят на:
· Органические
· Элементорганические
· Неорганические
В органических полимерах (карбоцетных), например, каучуках, основная цепь образованна углеродными атомами. Кроме –С, в ней могут быть атомы: -О, -Р, -F, -Сl, -S.
Атомы –О – способствуют гибкости цепи.
-Р, -Сl – повышают огнестойкость.
-F – высокая химическая стойкость.
-S – предаёт газонепроницаемость.
Элементоорганические (гетероцепные) полимеры, кроме –С содержат в основной цепи атомы не органических элементов (кремний, титан, алюминий и т.д.), которые сочетаются с органическими радикалами: - СН3, - С6Н5, - СН2. И т.д. Неорганические атомы в основной цепи существенно влияют на свойства полимеров: увеличивают теплостойкость и т.д. Органические радикалы в таких элементах придают материалу прочность и эластичность. В природе элементорганические полимеры не встречаются – их получают искусственным путём (пример: кремнийорганические соединения).
Неорганические полимеры - полимеры, в основной цепи которых нет атомов –С, а также они не имеют боковых органических групп. Их основная цепь состоит из оксидов кремния, алюминия, магния, кальция и т.д. Исключение – некоторые модификации –С, которые представляют собой карбоцетные неорганические полимеры (графит). Неорганические полимеры имеют большую плотность и высокую длительную теплостойкость. Не существуют в высокоэластичном состоянии. Хрупкие, плохо переносят динамические нагрузки. Могут иметь природное происхождение (асбест) или искусственное (керамика).
Макромолекулы могут быть построены из одинаковых по хим. Составу составных звеньев – мономеры. Или разных – сополимеры. Для многих синтетических сополимеров характерно случайное распределение звеньев.
ВНУТРИ- И МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ В ПОЛИМЕРАХ.
Способность элемента к образованию полимеров связанна с его положением в периодической таблице и зависит от величины энергии связи между атомами данного химического элемента.
Если энергия связи будет меньше 155 кДж/моль – полимер не образуется. Так как макромолекулы разрушаются при комнатной температуре в результате термической деструкции. Гомоцентные полимеры, состоящие из однотипных звеньев, могут образовывать химические элементы, которые находятся в периодической системе между металлами и низкомолекулярными веществами. Это бор, углерод, кремний, фосфор, сера, германий, мышьяк, селен, олово, сурьма, теллур, висмут, полоний.
Таблица № 1 Энергии связей одинаковых химических элементов
| связь | С-С | S-S | P-P | Se-Se | Te-Te | Si-Si | Ge-Ge | As-As |
| Энергия связи, кДж/моль |
С увеличением энергии связи возрастает способность к образованию больших макромолекул. Поэтому (С-С имеет набольшую связь) карбоцетные полимеры составляют наиболее многочисленный класс высокомолекулярных соединений. В таких полимерах основная цепь макромолекулы состоит из –С, которые связаны ковалентными связями.
По строению основного звена макромолекул, карбоцетные полимеры делят на:
1. Полимеры с линейными звеньями. Их рассматривают как производные макромолекул с полиметильной цепью: -СН2-СН2-… К ним относятся:
1. Полиэтилен (ПЭ) -СН2-СН2-…;
2. Поливинилхлорид (ПВХ) -СН2-CH-Cl-…;
3. Полистирол …-СН2-CH(C6H5)-… и др.
2. Полимеры с циклами в звеньях (циклоцепные):
1. с циклами в звене (бензольными и т.д.);
2. с конденсированными звеньями лестничной структуры.
Конденсированные звенья – звенья, в которых 2 и более колец имеют общие атомы.
3. с конденсируемыми звеньями паркетной структуры.
 Рис. 1 Строение циклоцентных полимеров.
Рис. 1 Строение циклоцентных полимеров.
В гетероцентных полимерах энергия связи между атомами разных химических элементов во многих случаях больше, чем между атомами одного элемента.
Таблица №2 Энергия связи между разными химическими элементами.
| Связь | B-N | B-O | Si-O | C-O | C-N | Al-C | Si-S |
| Энергия связи, кДж/ моль |
Гетероцентные полимеры- в основной цепи содержат атомы –О, -N, и др. Стабильность связи в полимерах с неорганическими цепями макромолекул тем выше, чем меньше ионность таких связей. Ионность связи можно определить по данным элекроотрицательности элементов. Если разность в электроотрицательности составит 1,9, то такая связь на 50% имеет ионный характер. Если разность меньше 1,9, то связь преимущественно ковалентная.
По строению основного звена макромолекул гетероцентных полимеров так же делят на полимеры с линейными звеньями и включенные циклы в звене
В макромолекулах реализуются следующие виды связей
1) ковалентная и водородная между атомами основной цепи
2) Вандерваальсное соединение или же силами Ван-дер-Ваальса – между атомами основной цепи и боковыми группами; между макромолекулами в целом.
Межмолекулярное взаимодействие
Между макромолекулами действуют более слабые силы, межмолекулярные не химические взаимодействия (силы Ван-дер-Ваальса). Суммарная энергия такого взаимодействия складывается из энергии дисперсного ориентационного и индукционного взаимодействия.
Величина энергии связи (Есв) составляет 42;21;2,1 кДЖ/моль, т.е. значительно меньше энергии ковалентной (Еков) связей, действующих в основной цепи макромолекул.
Вклад каждого вида взаимодействия в суммарную величину сил Ван-дер-Ваальса зависит от природы полимера. У полимера со слабыми полярными макромолекулами основными силами будут силы дисперсного взаимодействия.
С увеличением полярности макромолекул все больше значения преобладает силы ориентационного взаимодействия. В ряде полимеров: целлюлоза, полиамиды и т.д. могут образовываться водородные связи между двумя электроотрицательными атомами (N,O,F) и возникают через водородный атом.
Есв водорода 17:- 50 кДж/моль
Она больше сил Ван-дер-Ваальса.
Поэтому полимеры с Н-Н (водородной связью) имеют более высокие физические свойства. Меры интенсивности межмолекулярного взаимодействия полимеров определяется плотностью энергии Когезии: Дж/см3. Она равна работе удаления взаимодействующих молекул на бесконечно большое расстояние друг от друга. В зависимости от интенсивности межмолекулярного взаимодействия и гибкости макромолекул, все полимеры делятся на эластомеры, пластические массы, волокна.
Эластомеры - это полимеры со слабым межмолекулярным взаимодействием и плотностью энергии Когезии менее 320 Дж/см3
Пластические массы - это полимеры с межмолекулярным взаимодействием с плотностью энергии Когезии менее 320:- 420 Дж/см3
Волокна - это полимеры с плотностью энергии Когезии менее 480:-1000 Дж/см3
Некоторые полимеры занимают промежуточное положение и могут использоваться как пластические массы и волокна, или эластомеры и пластические массы.
Таблица № 3 Виды материалов на основе разных полимеров
| Эластомеры | Пластические массы | Волокна |
| Величина плотности энергии Когезии Дж/см3 | ||
| До 320 | 320-400 | 480-1000 |
| Полиизопрен Полибутадиен | ПЭ (полиэтилен) ПММА(полиметилметакрилат) | Полиакрилонитрил |
| Полиуретан ПВХ (Поливинилхлорид) | ||
| Полиамиды, Полиэфиры Производные целлюлозы |
Полимеры, из статистического характера большинства процессов их синтеза, состоят из макромолекул разной длины и с разной молекулярной связью. Т.Е. являются веществами полимолекулярными, полидисперсными. Полидисперсные полимеры описываются в функциях молекулярно-массового распределения, т.е. чем сильнее различаются по молекулярной массе отдельные макромолекулы полимера, тем больше его полидисперсность и шире молекулярно-массовое распределение.
В зависимости от типа полимера, условий его использования, его эксплуатации – изменяют широту молекулярно-массового распределения.
Пример: эластомеры – стремятся получить широкое распределение
Волокна- более узкое.
ЛЕКЦИЯ II.