Первая группа катионов
К первой аналитической группе относят катионы Na+, K+ и NH4+.
Соответствующие первым двум катионам элементы Na и К находятся в главной подгруппе первой группы периодической системы Д. И. Менделеева и являются s1 - элементами. Все s1 элементы - сильные восстановители, легко от- дают электрон, образуя катионы с зарядом + 1 и оболочкой инертного газа.
Катион NH4+ сложный ион, свойства его сходны со свойствами катиона К+, что объясняется зарядом ионов и близким значением их ионных радиусов. Сходные свойства приводят к одинаковому действию некоторых реактивов на эти ионы.
Соединения катионов Na+, K+, NH4+, как правило, характеризуются хорошей растворимостью в воде и других полярных растворителях. Именно поэтому группа не имеет группового реактива. Только с крупными анионами катионы I группы дают труднорастворимые соединения, например, КНС4Н4О6, Na3[Со(NO2)6], K[Sb(OH)6]. Поэтому реактивы, содержащие подобные анионы, служат для обнаружения катионов I группы.
Гидроксиды калия и натрия - сильные щелочи, раствор аммиака в воде (гидроксид аммония NH4OH) - слабое основание.
Ионы Na+ и К+ гидролизу не подвергаются, поэтому соли этих катионов и сильных кислот имеют нейтральную реакцию раствора, а соли слабых кислот -
NH4 + + Н2О = NH4OH + Н+.
Следовательно, его соли, образованные сильными кислотами, имеют кислую реакцию раствора, а соли слабых кислот - нейтральную, слабокислую или слабощелочную, в зависимости от константы диссоциации слабой кислоты.
Катионы К+, Na+, NH4+ в растворе бесцветны и большинство их соединений также бесцветны, окрашенными являются соли, например, К2СrO4 (анион СrO 2- имеет желтую окраску), КМпО4 (анион МпО4 - имеет фиолетовую окраску).
Катионы I группы не проявляют способности к комплексообразованию, но могут входить во внешнюю сферу комплексных соединений.
Ионы Na+ и К+ имеют постоянную, устойчивую степень окисления и не участвуют в окислительно-восстановительных реакциях. Катион NH4+ может быть окислен только
очень сильными окислителями (хлорная вода, царская водка и другие) до свободного азота. Характерными реакциями этих ионов являются реакции обмена.
Соединения катионов I группы склонны к образованию пересыщенных растворов, поэтому при выполнении аналитических реакций, сопровождающихся образованием осадков, требуется тщательное перемешивание реакционной смеси. Как правило, осадки медленно кристаллизуются и имеют характерную форму кристаллов, что позволяет открывать эти ионы микрокристаллоскопическими реакциями. Для обнаружения катионов Na+ и К+ широко используют метод окрашивания пламени.
Реакции катиона калия К+
1. Гидротартрат натрия NaHC4H4O6 (кислая соль винной кислоты) об- разует с растворами солей калия белый кристаллический осадок:
КСl + NaHC4H4O6 = КНС4Н4О6↓ + NaCl,
К+ + НС4Н4О6 - = КНС4Н4О6 ↓.
4 4 6 4 4 6
Осадок растворим в минеральных кислотах и щелочах (образование средних солей). Составьте и запишите соответствующие уравнения реакций.
Опыт. В пробирку налить 4 - 5 капель раствора соли калия (КСl, KNO3, K2SO4), прибавить равный объем гидротартрата натрия. Перемешать реакционную смесь стеклянной палочкой (если осадок не выпадает, слегка потереть ею о стенки пробирки) и охладить раствор под струей водопроводной воды. Чтобы убедиться в том, что осадок кристаллический, следует, закрыв про- бирку, сильно наклонить ее и рассмотреть прилипшие к стенкам и ко дну кристаллы КНС4Н4О6 (при подобном испытании аморфные и мелкокристаллические осадки легко отстают от стенок пробирки).
Испытать действие кислот и щелочей на осадок. Для этого, взмутив раствор, разделить его на три пробы. К первой добавить 1 - 2 капли сильной кислоты, ко второй - щелочи. К содержимому третьей пробы прибавить 2 капли дистиллированной воды и нагреть на водяной бане, осадок растворится. Он также растворяется при добавлении холодной воды. Реакция эта сравнительно малочувствительна (предельное разбавление 1:1000). На основании вышеизложенного можно сделать заключение об условиях проведения реакции. Реакцию необходимо проводить в нейтральной среде, при охлаждении и при достаточно большой концентрации ионов калия (разбавленные растворы можно предварительно упарить). Открытию катиона К+ мешают ионы NH4+, образующие с реактивом аналогичный осадок.
2. Гексанитрокобальтат(III) натрия Na3[Co(NO2)6] образует с катионом К+ кристаллический желтый осадок комплексной соли гексанитро(III)кобальтата натрия-калия:
2КС1 + Na3[Co(NO2)6] = K2Na[Co(NO2)6] ↓+ 2NaCl,
2К+ + Na+ + [Co(NO2)6]3- = K2Na[Co(NO2)6] ↓.
Осадок растворим в сильных кислотах (образование нестойкой кислоты Н3[Со(NO)2)6]). Присутствие щелочей мешает реакции, так как щелочь разлагая реактив, образует темно-бурый осадок Со(ОН)3.
Опыт. В пробирку налить 1 - 2 капли раствора КС1, прибавить 1 - 2 капли раствора реактива. Если осадок не выпадает, потереть стеклянной палочкой о стенки пробирки. Убедиться в том, что осадок кристаллический. Разделить осадок на две части. К первой добавить сильную кислоту до растворения осадка, ко второй - 4-5 капель уксусной кислоты СН3СООН (осадок не растворяется). Следовательно, реакцию необходимо проводить в нейтральной или слабокислой среде. Кроме того, следует учесть, что реактив должен быть свежеприготовленным, т. к. он сравнительно быстро разлагается и его бурая окраска переходит в розовую. Катион NH4+ мешает обнаружению иона К+. Реакция более чувствительная, чем первая (предельное разбавление составляет 1: 13000).
3. Гексанитрокупрат (II) натрия-свинца Na2Pb[Cu(NO2)6] образует с катионами К+ черные или коричневые кристаллы кубической формы:
2КС1 + Na2Pb[Cu(NO2)6] = K2Pb[Cu(NO2)6]↓ + 2NaCl,
2К+ + Рb2+ + [Cu(NО2)6]2- = K2Pb[Cu(N02)6]↓.
Опыт А) В пробирку налить 2-3 капли раствора КС1, прибавить равный объем реактива, дать постоять и рассмотреть образовавшийся осадок.
Б) Реакцию можно выполнять микрокристаллоскопическим методом. На чистое, сухое предметное стекло нанести каплю раствора соли калия, выпарить досуха, охладить и обработать каплей реактива. Через минуту рассмотреть образовавшиеся кристаллы под микроскопом (рис. 1).
Условия проведения реакции - в слабокислой или нейтральной среде (рН = 6 ÷ 7). Реакция достаточно чувствительная, обнаруживаемый минимум 7,5 мкг.
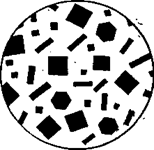 |
Рис. 1. Кристаллы K2Pb[Cu(NO2)6]
2. Окрашивание пламени. Ионы К+ окрашивают пламя в бледно- фиолетовый цвет.
Опыт. Платиновую или нихромовую проволочку тщательно очистить, для чего смочить ее в растворе НС1 и прокалить в пламени горелки до полного исчезновения окраски пламени. Ушком раскаленной проволочки при- коснуться к кристаллам соли калия и внести его в пламя горелки. Фиолетовое окрашивание пламени лучше наблюдать через синее стекло или флакон с раствором индиго.
Реакции катиона натрия Na+
1. Гексагидроксостибат (V) калия K[Sb(OH)6] образует с катионом Na+ белый кристаллический осадок Na[Sb(OH)6]:
NaCl + K[Sb(OH)6] = Na[Sb(OH)6]↓ + KC1, Na+ + [Sb(OH)6]- = Na[Sb(OH)6]↓.
Осадок растворим в щелочи:
Na[Sb(OH)6] + 2NaOH = Na3SbO4 + 4H2O.
Кислоты разлагают реактив с образованием аморфного осадка метасурьмяной кислоты HSbO3:
К [Sb(OH)6] + HC1 = HSbO3↓+ КС1 + ЗН2О.
Опыт. В пробирку налить 2 - 3 капли раствора соли NaCl, прибавить равный объем реактива, перемешать стеклянной палочкой и, если осадок не выпадает, потереть ею о стенки пробирки и охладить. Убедиться в том, что осадок кристаллический. Реакция малочувствительная, обнаруживаемый минимум - 0,3 мг.
2. Окрашивание пламени. Соли натрия окрашивают пламя в желтый цвет. Окраска устойчивая, не исчезает в течение нескольких секунд. Реакция очень чувствительная; предел обнаружения этой реакции составляет 3 ∙ 10-4 мкг, поэтому с ее помощью можно открывать ион Na+ как примесь в реактивах. Вывод о присутствии натрия надо делать с большой осторожностью, только при очень яркой окраске пламени.
Опыт. Реакция проводится так же, как и на ион К+.
Реакции катиона аммония NH4+
1. Щелочи NaOH и КОН при нагревании разлагают соли аммония с вы- делением газообразного аммиака:
NH4C1 + NaOH = NH3↑ + Н2О + NaCl.
Опыт. В пробирку поместить 2 - 3 капли соли аммония, прибавить 1 - 2 капли раствора щелочи (не касаясь края пробирки) и нагреть. Выделение аммиака можно обнаружить по характерному запаху (специфическая реакция) или по изменению окраски влажной индикаторной бумаги, поднесенной к отверстию пробирки. Красная лакмусовая бумага синеет.
Реакция чувствительная, обнаруживаемый минимум - 0,01 мкг.
2. Реактив Несслера - раствор тетраиодомерурат (II) калия K2[HgJ4] и КОН образует с солями аммония красно-бурый аморфный осадок иодида оксодимеркурат (II) аммония [NH2Hg2O]J:

Опыт. К капле разбавленного раствора соли аммония на предметном стекле (или в пробирке) добавить 1-2 капли реактива Несслера. Наблюдать выпадение осадка.
Реакция очень чувствительная (обнаруживаемый минимум - 0,25 мкг).
Условия проведения опыта: при выполнении опыта необходимо брать избыток реактива Несслера, так как осадок растворим в солях аммония; открытию катиона NH4 + мешают катионы Fe3+, Cr3+, Co2+, Ni2+ и другие, образующие окрашенные осадки с КОН.
В табл.1 представлены результаты действия некоторых реагентов на катионы I группы.
Таблица 1