Контрольная работа
Вариант 0.
1. Определите сумму коэффициентов в молекулярном уравнении ОВР:
KBrO3+F2+KOH→KBrO4+
а) 7 б) 23 в) 8 г) 12
2. Определите равновесный потенциал электрода, на котором протекает реакция
ClO4- + 2H+ + 2e ÛClO3− + 2H2O
Стандартный потенциал равен + 1,19 В, активности ионов ClO3- и ClO4- соответственно 0,75 и 1,55 моль/л, рН = 4.5, Т =298 К
3. Какая из восстановленных форм
а) H2S б) Mn2+ в) Cu
является более активным восстановителем:
1) S+2H++2e=H2S φ0=0,17В
2) MnO4-+8H++5e=Mn2++4H2O φ0=1,51В
3) Cu++e=Cu φ0=0,52В
4. Используя табличные значения, определите, какой наиболее вероятный продукт образуется при окислении хлорид-ионов в нейтральной среде под действием перманганат-ионов, если концентрации веществ в растворе равны 1 моль/л.
1) MnO4-+4H++3e=MnO2+2H2O φ0=1,67В
2)2Cl-=Cl2+2e φ0=1,36В
3) Cl-+H2O=HClO+H++2e φ0=1,49В
4) Cl-+3H2O=ClO3-+6e+6H+ φ0=1,45В
а) HClO б) Cl2 в) ClO3-
5. Установите, в каком направлении возможно самопроизвольное протекание реакции
2NaCl+Fe2(SO4)3=2FeSO4+Cl2+Na2SO4
1) Cl2+2e=2Cl- φ0=1,36В
2) Fe3++e=Fe2+ φ0=0,77В
а) слева направо б) справа налево в) обратима
→ ← ↔
6. Вычислите константу равновесия системы:
2CoCl3=2CoCl2+Cl2
а) 2 б) 1·1016 в) 2·1016 г) 16
7. Решите задачу, используя закон эквивалентов.
Определить массу выделившегося йода при взаимодействии 0,5 л 15%-ного раствора иодида калия (плотность - 1,12 г/мл) в кислой среде с избытком перекиси водорода.
Примеры решения некоторых задач
Окислительно-восстановительными называются реакции, сопровождающиеся изменением степени окисления элементов.
Степень окисления равняется условному заряду атома элемента, определенному исходя из предположения, что молекула состоит только из ионов.
При определении степени окисления атомов в соединениях следует знать:
1. Степень окисления атомов входящих в состав молекул простых веществ  , равна нулю, так как ни частичный, ни полный переход электронов одного атома к такому же другому невозможен.
, равна нулю, так как ни частичный, ни полный переход электронов одного атома к такому же другому невозможен.
2. Некоторые элементы во всех сложных веществах имеют постоянную степень окисления:
а) Щелочные металлы (Li, Na, K, Rb, Cs, Fr) имеют степень окисления +1
б) Элементы II группы (кроме Hg)
Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd имеют степень окисления +2
в) Алюминий Al имеет степень окисления +3
г) Фтор F имеет степень окисления –1
д) Водород(H) имеет степень окисления равную +1, во всех соединениях,
кроме гидридов, которые он образует со щелочными и щелочноземельными металлами. В гидридах степень окисления водорода равна -1 (NaH, AlH3, BaH2).
е) Степень окисления кислорода(O) равняется – 2.
Исключение составляют пероксиды, надпероксиды и супероксиды. Например, в  степень окисления кислорода составляет соответственно – 1, –1/2 и –1/3, а во фториде кислорода ОF2 степень окисления равна +2.
степень окисления кислорода составляет соответственно – 1, –1/2 и –1/3, а во фториде кислорода ОF2 степень окисления равна +2.
4. Степень окисления атома в сложном соединение может быть определена, если известны степени окисления атомов других элементов, входящих в соединение, исходя из того, что алгебраическая сумма степеней окисления, всех атомов составляющих молекулу, равна нулю. В случае иона алгебраическая сумма степеней окисления составляющих этот ион атомов, равняется заряду иона.
Например, даны  . Для определения степени окисления серы и азота составим уравнение: (+1)∙2 + х + (-2) ∙ 4 = 0; х = 6, степень окисления S = 6
. Для определения степени окисления серы и азота составим уравнение: (+1)∙2 + х + (-2) ∙ 4 = 0; х = 6, степень окисления S = 6
y + (-2) ∙ 3 = -1; у = +5, степень окисления N = 5
Не следует отождествлять степень окисления с валентностью элемента, даже если их абсолютное значение совпадают. Валентность атома определяется числом химических связей, и не имеет знака.
Например, во всех соединениях  валентность углерода равна 4, а степень окисления составляет соответственно -4, -2, 0, +1.
валентность углерода равна 4, а степень окисления составляет соответственно -4, -2, 0, +1.
Принято считать, что изменение степеней окисления атомов в результате окислительно-восстановительной реакции связано с переходом электронов от одного атома к другому.
Процесс отдачи электронов называться окислением. Вещество, атомы которого отдают электроны, называется восстановителем. Восстановитель в результате реакции окисляется, степень окисления его повышается, соответственно числу отданных электронов.
Процесс присоединение электронов называется восстановлением. Вещество, атомы которого принимают электроны, называется окислителем. Окислитель в результате реакции восстанавливается, степень окисления его понижается соответственно числу принятых электронов.
Так, в реакции 
восстановителем является хлорид олова (II). Степень окисления иона олова увеличивается от +2 до +4.
Степень окисления иона железа в ходе реакции понижается от +3 до +2, хлорид (III) является окислителем.
Каждая окислительно-восстановительная реакция представляет собой единство двух противоположных одновременно протекающих процессов: окисления и восстановления.
Пример. Расставьте коэффициенты, укажите: окислитель и восстановитель, что окисляется, что восстанавливается:
Решение.
1) Определяем степени окисления элементов, окислитель и восстановитель:

в-ль, т.к. о-ль, т.к. понижает
повышает степ. окисления
степ. окисл.
2) Записываем уравнение электронного баланса.
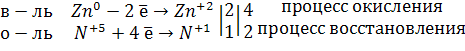
не можем поставить у N2O коэффициент 1, поэтому умножаем все коэффициенты на 2.
Часть атомов азота в HNO3 проявляет свойства окислителя, а часть выполняет роль кислой среды, поэтому коэффициент у HNO3 определяется суммой двух составляющих/


При определении продуктов окислительно-восстановительной реакции надо вспомнить, что
Только восстановительными свойствами обладают:
- все металлы; наиболее активными восстановителями являются металлы S-электронного семейства;
- вещества, в которых атомы элементов проявляют свою низшую степень окисления, имея завершенный слой ns2np6, (низшая степень окисления неметаллов = №группы – 8) эти атомы могут только отдавать электроны, например:  .
.
Только окислительными свойствами обладают:
-  (самый электроотрицательный элемент)
(самый электроотрицательный элемент)
- вещества, в которых атомы элементов находятся в высшей степени окисления (высшая степень окисления, как правило, равняется номеру группы периодической системы, к которой относится данный элемент). Например, в молекулах
 , внешний электронный слой атомов в высшей степени окисления имеет конфигурацию ns0np0, т.е полностью лишен электронов.
, внешний электронный слой атомов в высшей степени окисления имеет конфигурацию ns0np0, т.е полностью лишен электронов.
Двойственными окислительными и восстановительными свойствами обладает вещества, содержащие атомы в промежуточной степени окисления, которую они могут повышать, окисляясь и проявляя при этом восстановительные свойства, а также понижать, восстанавливаясь и проявляя окислительные свойства. Это все неметаллы, кроме  ,а также сложные вещества:
,а также сложные вещества:
 и др.
и др.
Характер взаимодействия между одними и теми же веществами может изменяться в зависимости от pH среды. Это наглядно проявляется в реакциях восстановления перманганата калия одним и тем же восстановителем, например, сульфитом натрия.
окисленная форма восстановленная форма
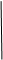
 кислая среда, pH<7
кислая среда, pH<7  Бесцветный раствор
Бесцветный раствор



|


| |||
 | |||
Влияние концентрации реагентов и температуры четко прослеживается при взаимодействии металлов с серной кислотой. Так, при растворении цинка в разбавленной кислоте, в качестве окислителя выступает ион водорода:

 В концентрированной же кислоте окислительные свойства проявляет сера со степенью окисления +6:
В концентрированной же кислоте окислительные свойства проявляет сера со степенью окисления +6:

Во многих случаях продукты окислительно-восстановительных процессов можно определить экспериментально по наблюдениям, если продукты реакции имеют характерную окраску, выпадают в осадок, выделяются в виде газа, имеют специфический запах. В тех случаях, когда реакция не сопровождается видимыми изменениями, необходимо прибегнуть к логическому рассуждению.
В этом случае может быть полезна таблица. В левой графе даны окислители, стрелкой показано, какой продукт получается из данного окислителя при восстановлении. В правой графе приведены восстановители и продукты их окисления. В таблице также учтено влияние концентрации кислоты и характера среды.
Таблица 1
Наиболее часто применяемые восстановители и окислители, и продукты реакции
| Окислители | Восстановители |
| Соединения серы | |



| 


|
| Соединения азота | |


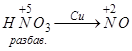


| 

|
| Соединения хрома | |

| 
|
| Соединения марганца | |




| 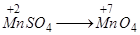
|
Количественной характеристикой самопроизвольного протекания окислительно – восстановительной реакции является расчетное значение ∆φ о реакции, которое определяется как разность между потенциалами окислителя и восстановителя. Окислительно – восстановительная реакция протекает самопроизвольно, если разность потенциалов является положительной величиной. Сущность этого заключается в следующем: если мысленно обособить процессы окисления и восстановления, т.е. “составить” гальванический элемент, то в нем будет совершаться электрическая работа за счет протекания химической реакции. Для обратимого процесса справедливо: А (максимально полезная)=А (электрическая), но
А (электрическая) = n F Ео, где Ео - стандартная ЭДС, В;
Ео (∆φ о) = φ оокислителя - φ о восстановителя,
(рассчитываем для той реакции, которая протекает самопроизвольно, т.е. при расчете А-работы ЭДС должна быть положительно).
Из термодинамики известно, что А = - ∆ Gо, отсюда n F Ео = - ∆ Gо
Таким образом, изменение энергии Гиббса будет отрицательной величиной, а значит, реакция будет протекать самопроизвольно, при положительном значении разности потенциалов.
Константу равновесия редокс-процесса можно рассчитать, исходя из соотношения:
 ;
;
 ;
;  .
.
Примеры решения заданий варианта контрольной работы
1. Определите сумму коэффициентов в молекулярном уравнении ОВР:
KBrO3 + F2 + KOH → KBrO4 +
Решение:
Т.к. Br в реакции повышает степень окисления с +5 до +7, то он является восстановителем. Окислителем в данной реакции может быть F2 , способный только понижать высшую степень окисления 0 до -1. В щелочной среде фторид-ион образует соль KF.
Br+5 - 2е = Br+7 │ 1 в-ль ок-ся
F2 + 2∙1е = 2 F- │ 1 о-ль вос- ся
KBrO3 + F2 + 2KOH → KBrO4 + 2KF + H2O
Сумма коэффициентов равна 8.
2. Определите равновесный потенциал электрода, на котором протекает реакция
ClO4- + 2H+ + 2e ÛClO3− + 2H2O
Стандартный потенциал равен + 1,19 В, активности ионов ClO3- и ClO4- соответственно 0,75 и 1,55 моль/л, рН = 4.5, Т =298 К
Решение:
Равновесный потенциал электрода, на котором протекает реакция с участием электронов и протонов определяется по уравнению Нернста-Петерса для окислительно-восстановительных процессов II типа:
0,059 [окисленной формы][ H+ ]m
φ = φ о + ------- lg ------------------------------- =
z [восстановленной формы ]
0,059 [окисленной формы][ 10-рН]m
= φ о + ------- lg -----------------------------------
z [восстановленной формы ]
φ — равновесный потенциал, В
φ о --- стандартный потенциал, В
z ---- число электронов, передаваемых в данной реакции
m ---- число H+, передаваемых в данной реакции
[ H+ ] = 10-рН ,моль/л
[ ] ---- активности или концентрации ионов, моль/л
Для данной реакции: φ о = 1,19В; [окисленной формы] = [ClO4-] = 1,55 моль/л;
[восстановленной формы ] = [ClO3-] = 0,75 моль/л;
[ H+ ] = 10-4,5 моль/л; m = 2; z = 2
0,059 1,55∙ (10-4,5)2
φ = 1,19 + ------- lg ---------------- = 1,19 + 0,0295 lg(2,0667∙ 10-9) =
2 0,75
= 1,19 + 0,0295∙(0,315 – 9) = 1,19 + 0,0295∙ (- 8,685) = 1,19 – 0,256 = 0,934В
3а. Какая из восстановленных форм
а) H2S б) Mn2+ в) Cu
является более активным восстановителем:
1) S+2H++2e=H2S φ0=0,17В
2) MnO4-+8H++5e=Mn2++4H2O φ0=1,51В
3) Cu++e=Cu φ0=0,52В
Чем меньше потенциал φ0 , тем более активным восстановителем будет восстановленная форма.
Ответ: а) H2S
3б. Какая из восстановленных форм
а) H2S б) Mn2+ в) Cu
является менее активным восстановителем:
1) S+2H++2e=H2S φ0=0,17В
2) MnO4-+8H++5e=Mn2++4H2O φ0=1,51В
3) Cu++e=Cu φ0=0,52В
Чем больше потенциал φ0 , тем менее активным восстановителем будет восстановленная форма.
Ответ: б) Mn2+
3в. Какая из окисленных форм
а) MnO4- б) Cu+ в) S
является менее активным окислителем:
1) S+2H++2e=H2S φ0=0,17В
2) MnO4-+8H++5e=Mn2++4H2O φ0=1,51В
3) Cu++e=Cu φ0=0,52В
Чем меньше потенциал φ0 , тем менее активным окислителем будет окисленная форма.
Ответ: в) S
3г. Какая из окисленных форм
а) MnO4- б) Cu+ в) Cu+
является более активным окислителем:
1) S+2H++2e=H2S φ0=0,17В
2) MnO4-+8H++5e=Mn2++4H2O φ0=1,51В
3) Cu++e=Cu φ0=0,52В
Чем больше потенциал φ0 , тем более активным окислителем будет окисленная форма.
Ответ: а) MnO4-
4. Используя табличные значения, определите, какой наиболее вероятный продукт образуется при окислении хлорид-ионов в нейтральной среде под действием перманганат-ионов, если концентрации веществ в растворе равны 1 моль/л.
1) MnO4-+4H++3e=MnO2+2H2O φ0=1,67В
2)2Cl-=Cl2+2e φ0=1,36В
3) Cl-+H2O=HClO+H++2e φ0=1,49В
4) Cl-+3H2O=ClO3-+6e+6H+ φ0=1,45В
а) HClO б) Cl2 в) ClO3-
Решение:
Чем больше Ео (∆φ о) = φ оокислителя - φ о восстановителя, тем наиболее вероятный продукт образуется.
Окислитель: MnO4- Восстановитель: Cl-
∆φ о 1-2 = 1,67 – 1,36 = 0,31В (продукт Cl2)
∆φ о 1-3 = 1,67 - 1,49 =0,18 В (продукт HClO)
∆φ о 1-3 = 1,67 - 1,45 =0,22 В (продукт ClO3-)
Ответ: наиболее вероятный продукт: б) Cl2
5. Установите, в каком направлении возможно самопроизвольное протекание реакции
2NaCl + Fe2(SO4)3 = 2FeSO4 + Cl2 + Na2SO4
1) Cl2+2e=2Cl- φ0=1,36В
2) Fe3++e= Fe2+ φ0=0,77В
а) слева направо б) справа налево в) обратима
→ ← ↔
Решение:
Если ∆φ о >0, то протекает прямая реакция, т.е. слева направо (→)
Если ∆φ о < 0, то протекает обратная реакция, т.е. справа налево (←)
∆φ о = φ оокислителя - φ о восстановителя,
Окислитель --- Fe2(SO4)3,т.к. Fe3+ переходит в Fe2+;
Восстановитель – NaCl,т.к. Cl- переходит в Cl0
∆φ о = 0,77 – 1,36 = - 0,59< 0,т.е ответ: б) справа налево
6. Вычислите константу равновесия системы:
2CoCl3=2CoCl2+Cl2
а) 2 б) 1·1016 в) 2·1016 г) 16
Решение:
Константу равновесия редокс-процесса можно рассчитать, исходя из соотношения:
 . n--- наименьшее общее кратное передаваемых электронов
. n--- наименьшее общее кратное передаваемых электронов
F = 96500 Кл /моль (постоянная Фарадея), Кл = Дж/В
Е0 = ∆φ о = φ оокислителя - φ о восстановителя, В
R = 8,314 Дж/К∙ моль (универсальная газовая постоянная)
n∙∆φ о
lg K = -------------.
0,059
Co3+ + 1e = Co2+ │ 1 2 2
2Cl- - 2∙ 1e = Cl2 │ 2 1
n = 2
Из таблицы: φ оокислителя = φ о(Co3+ /Co2+ ) = 1,84В
φ о восстановителя= φ о (Cl2/ 2Cl-) = 1,36В
∆φ о = 1,84 -1,36 = 0,48В
2∙ 0,48
lg K = ------------- = 16,27; К = 1016,27 = 100,27 ∙ 1016 = 1,9∙ 1016 = 2∙ 1016
0,059
Ответ: в) 2·1016
7. Решите задачу, используя закон эквивалентов.
Определить массу выделившегося йода при взаимодействии 0,5 л 15%-ного раствора иодида калия (плотность - 1,12 г/мл) в кислой среде с избытком перекиси водорода.
Закон эквивалентов: количества вещества эквивалентов всех участвующих в реакции веществ равны,т. е.
νэкв(X) = νэкв(Y) (1)
а так как

то з акон эквивалентов можно записать следующими формулами:
СН(Х)∙ V(Х) = СН(Y) ∙V(Y) (2)
Или
M(X) m(Y)
------------ = -------------- (3)
M(1/zX) M(1/zY)
(возможны комбинации между формулами 1, 2, 3)
Решение:
Закон эквивалентов для данной реакции:
νэкв(I2) = νэкв(KI)
νэкв(KI) = m(KI)∙z ; νэкв(I2) = m(I2)∙z ; m(I2) = νэкв(I2)∙M(I2) / z
M(KI) M(I2)
z в окислительно-восстановительных реакциях равно числу электронов, передаваемых атомом окислителя или восстановителя в данной реакции.
2I- - 2∙1e → I2 z(KI) = 1
I2 + 2∙1e → 2I- z(I2) = 2
 .
.
 = 500∙1,12 = 560 г
= 500∙1,12 = 560 г
 = 84 г
= 84 г
νэкв(KI) = 84∙1 / 166 = 0,506 моль
νэкв(I2) = 0,506 моль
m(I2) = 0,506∙254 / 2 = 64,262 г
Ответ: m(I2) =64,262 г