Государственное образовательное учреждение высшего профессионального образования
Ростовский государственный строительный университет
Утверждено на заседании
кафедры химии 10.01.2005 г.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
по теме: «МЕТОДЫЗАЩИТЫМЕТАЛЛОВ ОТ КОРРОЗИИ»
Ростов-на-Дону
УДК 541.2
Методические указания по теме «Методы защиты металлов от коррозии».- Ростов-н∕Д: Рост. гос., строит. ун-т. 2005 - 8 с.
Рассмотрены контроль коррозионного процесса, методы защиты металлов и принцип их выбора. В экспериментальной части дана методика выполнения лабораторной работы.
Составитель: доц. Л.М. Астахова
Редактор Н.Е. Гладких
Темплан 2005 г., поз. 168
Подписано в печать 11.05.05
Формат 60х84/16. Бумага писчая. Ризограф.
Уч.-изд.л. 0,5. Тираж 100 экз. Заказ
Редакционно-издательский центр
Ростовского государственного строительного университета
344022, Ростов-на-Дону, ул. Социалистическая, 162
© Ростовский государственный
строительный университет, 2005
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Каждая шестая доменная печь работает на коррозию - таков итог действия коррозии, приводящей к разрушению конструкций, понижению качества продук ции, а также к авариям и несчастным случаям на производстве. Это наносит на-родному хозяйству огромный ущерб.
Любой метод защиты изменяет ход коррозионного процесса, уменьшая его скорость. Однако, выбирая способ защиты металла, необходимо учитывать кон-роль коррозионного процесса.
Разрушение металла - совместное протекание двух процессов: окисления (анодный процесс) и восстановления (катодный процесс) и общая скорость кор-розии определяется скоростью более медленнотекущего процесса (медленно текущая реакция называется л и м и т и р у ю щ е й). Катодный контроль коррозионного процесса имеет место, если лимитирующей является катодная реакция. Анодный контроль - если лимитирующей является анодная реак-ция. При выборе метода защиты это необходимо учитывать. Если разрушение металла протекает с анодным контролем, необходимо подобрать метод защиты усиливающий анодную поляризацию. Если разрушение металла протекает с ка-тодным контролем - метод усиливающий катодную поляризацию. Напомним, что п о л я р и з а ц и е й называется смещение потенциала электрода при протекании через систему электрического тока. Анодная поляризация - сме- щение потенциала в положительную сторону. Нижеприведенные иаграммы ил-люстрируют снижение скорости коррозии при усилении анодной (рис. 1) и катодной (рис. 2) поляризации.
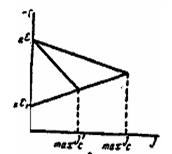

Рис. 1. Анодный контроль Рис. 2. Катодный контроль
Все методы защиты условно делятся на четыре группы:
1) электрохимические методы;
2) методы, связанные с изменением свойств корродирующего металла;
3) методы, связанные с изменением свойств коррозионной среды;
4) комбинированные методы.
Электрохимические методы защиты основаны на изменении электрохимических свойств металла под действием поляризующего тока. Катодная защита применяется для повышения коррозионной стойкости металлов в условиях почвенной, морской коррозии, при контакте металла с агрессивными химическими средами. Защита обеспечивается в этом случае наложением тока от внешнего источника питания (защищаемая поверхность соединяется с отрица-тельным полюсом этого источника) - на защищаемой поверхности протекают только восстановительные процессы. Протекторная защита (частный случай катодной защиты) - создание макрогальванической пары с менее благород-ным металлом-протектором. П р о т е к т о р играет роль анода и растворяется со скоростью, достаточной для создания в системе тока необходимой силы. В качестве протектора могут быть использованы цинк, алюминий, магний и их сплавы. Анодная защита применима к металлам и сплавам, способных пасси-вироваться при смещении их электродного потенциала в положительную сторо-ну и достижения состояния полной пассивации (здесь защищаемая поверхность соединяется с положительным полюсом внешнего источника питания). Элек-трохимические методы защиты можно использовать только в хорошо проводи- мой среде - в морской воде, почве, растворах электролитов.
Группа методов защиты,основанная на изменении свойств металлов,
осу ществляется либо специальной обработкой их поверхности, либо легированием. Легированием называ-ется введение в защищаемый металллегирующих эле-ментов, повышающих термодинамическую устойчивость анодной фазы (напри-мер: легирование стали – никелем, никеля – медью, меди – золотом и т. д.), либо содействующих пассивированию анодной фазы (легирование сталей хро-мом или кремнием, никеля – хромом). Кроме того, для увеличения коррозион-
ной стойкости металлов широко используются различные покрытия. Предназ
начение защитного покрытия - создание барьерного слоя, препятствующе-го проникновению коррозионной среды к поверхности металла. Материал пок-рытия прежде всего должен обладать высокой химической устойчивостью, сла- бой проницаемостью для воды, газов, агрессивных ионов (Cl-, SO4-2), хорошей адгезией к металлу, механической прочностью и др. Покрытия делятся на две группы: металлические и неметаллические. Неметаллические покрытия, в свою очередь,бывают неорганические (оксидные, солевые, силикатные, асбоце-
ментные и др.) и органические (лакокрасочные, битумные, резиновые, поли-мерные). Металлические покрытиябывают анодными и катодными. Анодное металлическое покрытие имеет место в случае нанесения на защищаемый металл другого металла с более отрицательным электродным потенциалом, например, железо (-0,44 В), покрытое цинком (-0,76 В). Катодное металли-ческое покрытие - на защищаемый металл наносят другой металл с более положительным электродным потенциалом, например, железо (-0,44 В), покры-
тое медью (+0,345 В). Если нарушается целостность защитного металлического покрытия в процессе эксплуатации, начинают работать гальванопары. В случае анодного покрытия - разрушается металл покрытия (анод), защищаемый металл (катод) остается без изменения. В случае катодного покрытия – разрушается защищаемый металл (анод, т.к. его электродный потенциал отрицательнее по-тенциала покрытия), металл покрытия (катод) не изменяется.
Для повышения защитного эффекта часто используют системы из не-скольких покрытий: фосфатное покрытие перед нанесением лакокрасочного, цинковое покрытие с последующим фосфатированием и нанесением лака, мно- гослойные металлические покрытия, лакокрасочные покрытия с наполнителем из металлического порошка и др.
Скорость коррозии можно уменьшить также изменением свойств корро-зионной среды, в результате которой уменьшается ее агрессивность, или введением в коррозионную среду небольших добавок замедлителей коррозии - ингибиторов. Обработка среды заключается в уменьшении влажности и запы-ленности воздуха производственного помещения, деаэрировании (уменьше-
нии концентрации кислорода) жидких сред и т. д. Ингибиторы коррозии в зависимости от условий их применения делят на летучие и жидкостные, кото-рые, в свою очередь, бывают кислотные, щелочные и нейтральные (замедля-ющие скорость коррозии соответственно в кислых, щелочных или нейтраль-ных средах). Ингибиторы широко исполь-зуются для защиты от разрушений внешних и внутренних поверхностей труб и аппаратов, в циркуляционных охла-дительных системах, коммуникационных системах, в различных емкостях для хранения жидких продуктов и др.Их большое преимущество состоит в том, что они пригодны при защите уже пораженных коррозией систем без замены мате-риала или конструкции. Механизм действия ингибиторов обусловлен их ад-сорбцией на границе раздела «металл – коррозионная среда». Защитное дейст-вие ингибитора тем больше, чем больше размер ингибирующей молекулы. Кро-ме того, защитный эффект наступает при более низких концентрациях, если мо-лекулы ингибитора полярны, чем в случае неполярных молекул. Здесь, при растворении ингибитора образуются положительно заряженные ионы. При рас-творении металла его положительно заряженные ионы переходят в раствор, а на поверхности металла скапливается избыток отрицательных зарядов. Отрица-тельно заряженная поверхность металла притягивает положительные ионы ингибитора, которые адсорбируясь блокируют дальнейшее его растворение. В настоящее время в качестве ингибиторов используются глицерин
(СН2ОН-СНОН- СН2ОН), ацетальдегид (СН3СОН), анилин (С6Н6NН2), уротропин и многие другие.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ