Параграф №№ 1 - 17
. Вы сказали, что вещества записываются при помощи формул. Выполните следующее задание
Задание: №1 а) что означают следующие записи
4N2 3H2O 4S P2O5 2Fe 3CuO 4O3 3NH3
б) подчеркните формулы сложных веществ.
Следующее задание. Вы говорили, что химия изучает вещества, из которых состоят все окружающие нас тела. Если тела имеют массу, то и вещества должны иметь массу. И такая масса называется относительная молекулярная.
Для вычисления относительной молекулярной массы необходимо суммировать относительные атомные массы элементов образующих соединение.
Мr = n1 *Аr1 + n2* Ar2 + n3* Ar3 (1)
. Массовая доля элемента в данном веществе (w) – отношение относительной атомной массы данного элемента, умноженной на число его атомов в молекуле к относительной молекулярной массе вещества:
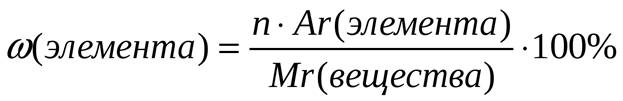 (2)
(2)
где w – массовая доля элемента в веществе;
Ar– относительная атомная масса;
n– индекс в химической формуле;
Mr– относительная молекулярная масса вещества.
Массовые доли выражают в процентах или в долях:
w (элемента) = 20% или 0,2.
Задание: №2 Определите, в каком веществе массовая доля кислорода больше в FeO или Fe2 O3?
Вы справились с заданием. А теперь посмотрите на две эти формулы, в их состав входят одинаковые элементы, но количество их разное. Почему? Какое свойство лежит в основе составления формул? (Ответ: валентность.). А что такое валентность?
Задание №3:
а).Пользуясь таблицей Д И Менделеева, составьте формулы веществ по валентности:

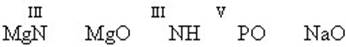
б). Определите валентность второго элемента по формуле, если известно, что сера во всех веществах двухвалентна:
Al2S3 CS2 K2S MgS H2S
Мы можем провести аналогию химии с русским языком. В русском языке существуют буквы, из букв, складываются слова, а из слов предложения. Так и в химии, атомы химического элемента обозначаются знаками, из знаков, как слова складываются формулы, а что же в химии является предложением? Правильно – химические уравнения.
Итак. Что называется химическим уравнением? Какие типы химических реакций вы знаете?
Задание №4: Расставьте коэффициенты и укажите тип реакции.
Mg + O2 = MgO
H2O = H2 + O2
Zn + HCl = ZnCl2 + H2
P + O2 = P2O5
HCl = H2 + Cl2
Fe2O3 + H2 = Fe + H2O
Заключительный этап повторения. Химия – наука экспериментальная. Но, чтобы проводить эксперимент, необходимо знать количества веществ, их массу или объем. Основной количественной характеристикой вещества является понятие «количество вещества». Что такое «количество вещества»? Какие формулы используют для расчета количества вещества.

 Решите задачу. Дано 2 моль кислорода. Рассчитайте массу, и число молекул кислорода. (Помните! Формула кислорода – О2).
Решите задачу. Дано 2 моль кислорода. Рассчитайте массу, и число молекул кислорода. (Помните! Формула кислорода – О2).
Домашнее задание:
· подготовится к контрольной работе.
· повторить параграфы №№ 1 – 17
· вопросы для повторения: (устно)
- что изучает химия?
- что называется веществом?
- чем отличаются чистые вещества от смесей?
- какие смеси называются однородными? какие – неоднородными?
- какие способы разделение смесей вам известны?
- чем физические явления отличаются от химических явлений?
- что такое атомы, молекулы?
- чем отличаются простые вещества от сложных веществ?
- что называется химическим элементом?
- что показывает относительная атомная масса?
- что называется химической формулой?
- что показывает относительная молекулярная масса?
- что называется валентностью? определение валентности по формулам их соединений. Составление химических формул по валентности.
- типы химических реакций
- закон сохранения массы веществ и составление уравнений химических реакций.
-находить по формулам: массу вещества, количество вещества и молярную массу.