Нитраты спиртов, или нитроэфиры, составляют основу бездымных порохов и твердых ракетных топлив, а также входят в состав многих промышленных взрывчатых веществ (динамитов, победитов, некоторых аммонитов и др.) [1]. Ассортимент используемых для вооружения и промышленных целей нитроэфиров, который долгое время ограничивался нитроглицерином и пироксилином, все время расширяется. Широкому применению нитроэфиров в технике, несмотря на их высокую чувствительность к механическим воздействиям и относительно низкую стойкость, способствует легкость получения, доступность исходных материалов и высокие взрывчатые свойства. Многие нитроэфиры способны пластифицировать высокомолекулярный нитроэфир — нитроцеллюлозу. Такая пластификация, приводящая к образованию эластичных масс с хорошими физико-механическими показателями, используется при производстве высокоэнергетического баллиститного пороха.
Некоторые нитроэфиры, например тетранитрат пентаэритрита (тэн), благодаря высокой чувствительности к детонационному импульсу и малому критическому диаметру детонации, используют для снаряжения капсюлей-детонаторов, детонирующих шнуров и детонаторов.
По свойствам нитроэфиры резко отличаются от нитросоединений и нитраминов, вследствие того, что нитрогруппа связана с углеродом через кислород —С—О—NO2. Эту группировку атомов называют нитратной, а нитроэфиры рассматривают как О-нитросоединения.
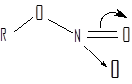 Атомы С, О и N нитратной группировки лежат в одной плоскости, и кратность связи нитрогруппы с кислородом несколько больше единицы, о чем говорит высокий барьер вращения (~ 10ккал/моль) вокруг этой связи:
Атомы С, О и N нитратной группировки лежат в одной плоскости, и кратность связи нитрогруппы с кислородом несколько больше единицы, о чем говорит высокий барьер вращения (~ 10ккал/моль) вокруг этой связи:
Спектроскопические исследования различных Нитроэфиров подтверждают симметричность структуры нитратной группировки. Длины связей и углы между ними следующие:
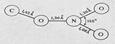
Доказательством связи нитрогруппы с кислородом является реакция восстановления нитроэфиров, приводящая к образованию исходного спирта и аммиака:
RON02  ROH + NH3
ROH + NH3
При восстановлении же нитросоединений образуется амин. Структура группы N02 в нитроэфирах та же, что и в нитросоединениях.
ПОЛУЧЕНИЕ
Нитроэфиры могут быть получены при взаимодействии галогеналкилов с нитратом серебра:
R3CX+AgNO3  R3CONO2+AgX
R3CONO2+AgX
где Х – Cl, Br, I; R – H, Alk.
Более удобным и широко распространенным способом получения нитроэфиров, особенно в заводской практике, является этерификация спиртов азотной кислотой или серно-азотной кислотной смесью.
Согласно современным взглядам, механизм этерификации спиртов азотной кислотой или серно-азотной кислотной смесью аналогичен механизму образования нитросоединений.
Ингольд этерификацию спиртов рассматривает как O-нитрование. Точнее, он считает, что происходит электрофильное замещение водорода гидроксила на нитрогруппу. Процесс идет в две стадии:
1) присоединение 

2) отрыв протона

Первая стадия протекает медленно, вторая — быстро.
Образование активного этерифицирующего агента идет по схеме:
2HNO3 
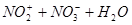
HNO3+2H2SO4 

H2O+H2SO4 

Промежуточный комплекс может распадаться как на конечный, так и на исходный продукт, потому что константы K1 и K2 по величине довольно близки и процесс этерификации является обратимым. Чтобы реакция протекала в нужном направлении, необходим активный акцептор протонов, например 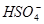 или
или 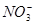 .
.
Спирт атакует положительно заряженный азот и образует с ним связь за счет свободной электронной пары кислорода гидроксила. Реакция будет идти тем быстрее, чем больше частичный положительный заряд на азоте. Таким зарядом обладает катион нитрония  . Это делает концентрированную серно-азотную кислотную смесь более сильным этерифицирующим агентом, чем чистая азотная кислота.
. Это делает концентрированную серно-азотную кислотную смесь более сильным этерифицирующим агентом, чем чистая азотная кислота.
Теоретическое объяснение этого факта впервые было дано Сапожниковым, полагавшим, что этерифицирующим агентом в серно-азотной кислотной смеси является молекула азотной кислоты, не связанная с Н20 в гидраты благодаря наличию серной кислоты. Некоторым продолжением исследований и развитием взглядов Сапожникова является работа Еременко, который считает, что механизм О-нитрования Ингольда недостаточно полно отражает процесс и не объясняет многих его явлений.
На основании калориметрических исследований реакции О-нитрования метанола, этиленгликоля, метриола, глицерина, мезоэритрита, пентаэритрита и других спиртов было показано, что О-нитрование одной азотной кислотой прекращается, если в ней воды становится более 40%. Таким образом, даже разбавленная азотная кислота, не содержащая катион нитрония, обладает этерифицирующим
действием.
Кинетические исследования О-нитрования спиртов непрерывным автоматическим методом по выделению реакционного тепла, а также О-нитрования меченого мезоэритрита (180) азотной кислотой позволили предположить, что О-нитрующим агентом является свободная неионизированная азотная кислота. Механизм складывается из следующих реакций:



(медленно)
 (быстро)
(быстро)
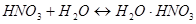 (быстро)
(быстро)
Реакционная способность спиртов различна, при электрофильном замещении Н на N02 она определяется электронной плотностью атома кислорода гидроксила, усиленной или ослабленной индукционным эффектом, распространяемым по цепи атомов, из которых состоит молекула.
Первичные спирты этерифицируются азотной кислотой легче, чем вторичные. Это различие используют в практике при получении неполных эфиров многоатомных спиртов. В многоатомных спиртах α-гидроксильные группы более реакционноспособны, чем β-гидроксильные группы. Поэтому для получения тринитрата глицерина используют безводные серно-азотные кислотные смеси, в то время как динитрат глицерина получают с использованием чистой азотной кислоты.
Повышение содержания азотной кислоты в отработанной кислоте увеличивает выход нитроэфира, а повышение содержания воды, наоборот, влечет за собой уменьшение выхода нитроэфира, вследствие его гидролиза.
При выборе состава кислотной смеси необходимо помнить также, что серная кислота не только ускоряет этерификацию, но при определенном избытке разлагает продукты этерификации. При этом эфиры азотной кислоты могут переходить в эфиры серной кислоты:
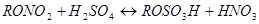
Для этерификации спиртов можно применять в качестве водоотнимающего средства уксусный ангидрид или его смесь с ледяной уксусной кислотой. В этом случае, по сравнению с этерификацией в присутствии серной кислоты, исключается образование сульфатов, наличие которых во взрывчатых азотнокислых эфирах нежелательно, так как они понижают стойкость нитроэфиров и затрудняют стабилизацию.
Нитроэфиры получают при определенной, обычно невысокой, температуре, поскольку повышение температуры увеличивает скорость не только этерификации, но и обратной реакции омыления, а также процессов окисления. Окислительные процессы снижают выход нитроэфиров и увеличивают опасность их производства. Повышение температуры выше определенного предела может привести к загоранию массы, вследствие прогрессивно увеличивающихся скоростей реакций этерификации и окисления. Из-за большого теплового эффекта окисления охлаждающая поверхность аппаратуры не сможет обеспечить полный отвод выделившегося тепла, температура реакционной массы будет прогрессивно расти может достичь температуры воспламенения спирта и нитрата, что повлечет за собой взрыв.
Повышение температуры при этерификации особенно опасно для некоторых эфиров азотной кислоты, обладающих низкой стойкостью в неочищенном состоянии. Оно может вызвать саморазложение полученного продукта, которое часто ускоряется окислами азота. Саморазложение нитроэфиров, как правило, остановить охлаждением не удается, и оно оканчивается загоранием или даже взрывом.
ХИМИЧЕСКИЕ СВОЙСТВА.
1) Гидролиз
Характерным свойством нитроэфиров является их способность к гидролизу как в щелочной, так и в кислой среде:
RONO2+H2O  ROH+HNO3
ROH+HNO3
Гидролиз сопровождается образованием, наряду с основными продуктами (спирт и кислота), ряда побочных продуктов: альдегидов кетонов карбоновых кислот, ненасыщенных соединении, азотной кислоты и т.
2) Восстановление
Восстановление нитроэфиров приводит, как правило, к образованию исходного спирта и аммиака. В некоторых случаях, в зависимости от природы восстанавливающего агента, продуктами реакции могут быть N2, NO, а также вместо спирта эфир той кислоты, в которой проводили восстановление.
3) Переэтирификация
Специфичной для нитроэфиров является реакция переэтерификации. В частности, взаимодействие их с серной кислотой приводит к замене нитрогруппы сульфогруппой:
RONO2+H2SO4  ROSO3H+HNO3
ROSO3H+HNO3
При нагревании нитроэфиров в уксусной кислоте, содержащей серную кислоту, кроме переэтерификации может протекать реакция, приводящая к образованию альдегидов.
4) Нитрование
Благодаря подвижности нитрогруппы, нитроэфиры способны нитровать различные органические соединения в кислой и щелочной средах Например, пиррол и индол легко нитруются этилнитратом:

5) Интересным свойством нитроэфиров является их способность катализировать реакции полимеризации.
Например, нитроглицерин инициирует полимеризацию стирола и метилметакрилата.