d lnР + γ d lnV =0. (8)
Если показатель адиабаты принять постоянным, то дифференциальное уравнение (8) в следующее:
d(ln (РV γ) = 0
Интегрируя это уравнение, получим:
ln (РV γ) = ln const
или
РV γ = const; (9)
для любой массы вещества объемом V уравнение (9) имеет вид
РV γ = const.
Уравнение (9) называется уравнением адиабаты или уравнением Пуассона и справедливо и для газа, и для жидкости, и для твердого тела. Если показатель адиабаты изменяется с изменением состояния системы, то можно использовать среднее значение показателя γср.
Реальные газы в области умеренных давлений по своим свойствам приближаются к идеальным газам и для них можно применять соотношения для идеальных газов. Для идеального газа показатель адиабаты с учетом соотношения (7) определяется по формуле:
γ = ср/сv = Cp/Cv = 1+R/Cv 
Приборы, необходимые для выполнения работы
Прибор Клемана – Дезорма, с помощью которого можно определить величину  (рис.1). Он представляет собой баллон A с воздухом, накачиваемым компрессором K, до некоторого давления P, избыток которого D Р = Р – Р 0 над атмосферным р0 определяется по водяному манометру, соединённому с баллоном шлангом,
(рис.1). Он представляет собой баллон A с воздухом, накачиваемым компрессором K, до некоторого давления P, избыток которого D Р = Р – Р 0 над атмосферным р0 определяется по водяному манометру, соединённому с баллоном шлангом,
D Р = r g h
Для осуществления быстрого (адиабатного) расширения воздуха из баллона в атмосферу служит ручной клапан Кл.
Выделим (мысленно) внутри воздуха, находящегося в баллоне А, некоторую массу газа m и проследим за изменением её состояния во время опыта при одновременном изменении давления Р и температуры Т.
Если клапан Кл открыт, то давление в сосуде равно атмосферному Р 0; температура воздуха в сосуде равна T0 – температуре окружающей среды. Тогда параметрами мысленно выделенной массы воздуха будут V 0, P 0, T 0, где V 0 – объём рассматриваемой массы воздуха при давлении P 0 и температуре T 0.
Если теперь закрыть клапан Кл и накачать с помощью компрессора в сосуд некоторое количество воздуха, то рассматриваемая нами масса воздуха сожмётся, а температура и давление её повысятся. Через некоторое время, вследствие теплообмена с окружающей средой, температура воздуха в сосуде станет равной T 0. Давление же будет равно:
P 1 = P 0 + rg h 1, (10)
где h 1 – окончательная (после установления теплового равновесия с окружающей средой) разность уровней жидкости в манометре.
Состояние рассматриваемой массы воздуха определяется теперь параметрами V 1, P 1, T 0 – это 1-ое состояние выделенной массы воздуха; V 1 – объём рассматриваемой массы воздуха при давлении P 1 и температуре T 0.
 Е сли на короткое время (~ 1÷2 с) открыть клапан Кл (рис. 1), то воздух, находящийся в баллоне, быстро (адиабатно) расширится и вследствие этого охладиться. В конце этого малого промежутка времени, в течение которого клапан Кл открыт и баллон сообщается с атмосферой, давление воздуха внутри сосуда станет равным давлению атмосферы P0, и состояние рассматриваемой массы воздуха будет определяться в этот момент следующими параметрами:
Е сли на короткое время (~ 1÷2 с) открыть клапан Кл (рис. 1), то воздух, находящийся в баллоне, быстро (адиабатно) расширится и вследствие этого охладиться. В конце этого малого промежутка времени, в течение которого клапан Кл открыт и баллон сообщается с атмосферой, давление воздуха внутри сосуда станет равным давлению атмосферы P0, и состояние рассматриваемой массы воздуха будет определяться в этот момент следующими параметрами:
V2, P0, T1 – 2-ое состояние выделенной массы воздуха, где V2 – объём выделенной массы воздуха. При этом T1 < T0.  Когда давление в сосуде А сделается равным давлению атмосферы (~ 1÷2 с) клапан Кл закрывают. Воздух, находящийся в баллоне, начнёт нагреваться от T 1 до T 0 вследствие получения тепла от окружающей среды, давление в сосуде начнёт повышаться и станет равным:
Когда давление в сосуде А сделается равным давлению атмосферы (~ 1÷2 с) клапан Кл закрывают. Воздух, находящийся в баллоне, начнёт нагреваться от T 1 до T 0 вследствие получения тепла от окружающей среды, давление в сосуде начнёт повышаться и станет равным:
P 2 = P 0 + rg h 2, (11)
где h 2 – разность уровней жидкости в манометре после того, как температура газа в баллоне станет равной температуре окружающей среды.
Рассматриваемая масса воздуха теперь характеризуется параметрами V 2, P 2, T 0 – это 3-е состояние рассматриваемой массы воздуха.
Итак, рассматриваемая масса воздуха во время опыта находилась последовательно в трёх состояниях:
1. V 1, P 1, T 0 2. V 2, P 0, T 1 3. V 2, P 2, T 0
Переход из первого состояния во второе происходит адиабатно, а точки состояний 2 и 3 лежат на изохоре. На рис.2 изображены графики процессов: кривая 1-2 – адиабата, кривая 2-3 – изохора, кривая 1-3 – изотерма. Газ в состояниях 1-3 имеет одинаковую температуру T 0.
Переход из состояния 1 в состояние 2 описывается уравнением Пуассона:
 . (12)
. (12)
Параметры 1-го и 3-го состояний удовлетворяют закону Бойля – Мариотта:
P 1 V 1 = P 2 V 2. (13)
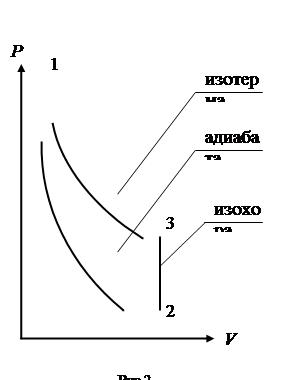 Возведя уравнение (13) в степень γ и разделив его почленно на (12), получим
Возведя уравнение (13) в степень γ и разделив его почленно на (12), получим
 ,
,
отсюда
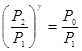 . (14)
. (14)
Учитывая равенства (9) и (10), получаем, что
P 0 = P 1 – rg h 1, P 2 = P 1 – rg(h 1 - h 2)
и подставляя их в равенство (14), имеем
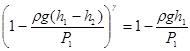 . (15)
. (15)
Так как rg(h 1 – h 2) << P 1, то разложив левую часть (15) в ряд и ограничившись первым членом разложения, получим
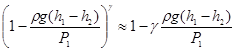 . (16)
. (16)
Приравняв правые части (14) и (15), получим следующую формулу:
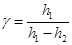 ,
,
которая используется в этой работе для экспериментального определения γ.