Лекция «Механизм антиоксидантного действия»
Схема ингибирования радикально-цепного окисления, приведена и рассмотрена в предыдущей лекции.

Ингибирование цепной вырожденно-разветвленной реакции. Если окисление протекает без инициатора, т. е. в режиме автоокисления, то оно идет с автоускорением из-за нарастающей в ходе реакции скорости инициирования (накопление гидропероксида). Темп ускорения зависит от скорости цепного окисления, т. е. существует положительная обратная связь между процессами автоинициирования и цепного окисления RH. Эта связь проявляется и в ингибированном окислении органических соединений.
Если в цепной инициированной реакции, когда Vi = const, период индукции (время торможения реакции) не зависит от эффективности тормозящего действия ингибитора, а определяется его концентрацией, то при автоокислении чем эффективнее ингибитор обрывает цепи, тем он медленнее расходуется. Обусловлено это тем, что в присутствии ингибитора медленнее накапливается ROOH, а следовательно, и увеличивается период торможения. Кроме того, если инициированное окисление углеводородов тормозят соединения, обрывающие цепи, то автоокисление тормозят и такие соединения, которые разрушают гидропероксиды. Такой распад, если он не сопровождается образованием свободных радикалов, снижает концентрацию накапливающегося гидропероксида, а, следовательно, и скорость автоинициирования.
Для ингибированного автоокисления часто характерны критические явления, причиной которых является автокаталитический характер реакции и упоминавшаяся выше обратная связь. Поскольку гидропероксид в ходе окисления распадается, возникают два разных режима ингибированного окисления: нестационарный и квазистационарный по гидропероксиду.
Рассмотрим более детально группы ингибиторов окисления.
Фенолы и ароматические амины - эффективные ингибиторы окислительных реакций
Наиболее распространенными и эффективными ингибиторами окисления являются ингибиторы окисления первой группы - фенолы и ароматические амины. Главным действующим началом антиоксидантов этой группы, обеспечивающим их способность тормозить окисление, является гидроксильная или аминогруппа группа у ароматического ядра. Энергии связей O-H и NH в фенолах и ароматических аминах относительно низкие, поэтому, образующиеся в ходе окисления радикалы RO2• насыщают свою свободную валентность путем взаимодействия с молекулой ингибитора. В результате на смену активным пероксирадикалам приходят малоактивные радикалы ингибитора, не способные, в общем случае, вести цепной процесс. Следствием этого является замедление или полное прекращение (если ингибитор перехватывает алкисльные радикалы R•) процесса окисления. После израсходования всего ингибитора заканчивается период индукции, и реакция окисления развивается практически с той же скоростью, что и без ингибитора.
Важной особенностью электронного строения антиоксидантов фенольного типа является сопряжение π-электронов ароматической системы с р-электронами неподеленной пары электронов атома кислорода. В наибольшей степени сопряжение проявляется, когда гидроксильная группа компланарна с плоскостью ароматического кольца. о-Алкильное замещение вызывает некоторое нарушение компланарности, что приводит к существенным изменениям физико-химических свойств фенолов. Прочность связи О-Н (DOH) для различных фенолов можно найти в справочниках. При сравнении значений DOH для замещенных в кольце фенолов - фенола (370 кДж⋅моль-1), 2,6-диметилфенола (354 кДж⋅моль-1), 2,6-дитретбутилфенола (343 кДж⋅моль-1) видно, что особенно сильные изменения в молекуле наблюдаются, когда орто -положения замещены объемными трет-алкильными группами. Нарушение компланарности приводит к некоторому изменению связи О-Н и, как следствие, к снижению ее прочности.
Влияние природы заместителей на реакционную способность фенолов и соответствующих радикалов будет двояким: с одной стороны – увеличение объема о-алкильных заместителей снижает прочность О-Н связи, что увеличивает активность фенола в реакции с пероксирадикалом. С другой - экранирование реакционного центра объемными заместителями создает стерические препятствия для подобных реакций.
Другой важный фактор, от которого зависят свойства фенолов, в том числе их реакционная способность - распределение электронной плотности. Оно в значительной степени определяется электронодонорной (электроноакцепторной) способностью заместителей. Электронодонорные заместители увеличивают антиоксидантную активность фенольных соединений, электроноакцепторные заместители снижают.
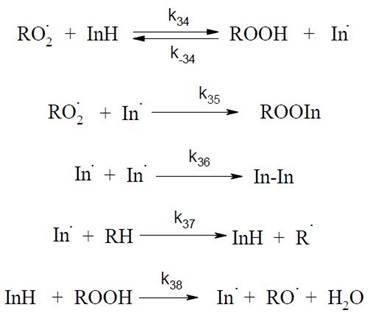
Реакция (k34) - ключевая в ингибированном окислении, она определяет саму способность ароматических аминов и фенолов тормозить цепное окисление органических веществ. В результате этой реакции в окисляющейся системе снижается концентрация RO2• и, следовательно, скорость реакции продолжения цепи. Константы скорости большого числа фенолов и ароматических аминов с различными пероксидными радикалами лежат в интервале 104-106 л/моль.
В процессе ингибированного окисления органических веществ из ингибитора образуются свободные радикалы In•. Феноксильные радикалы многих фенолов сравнительно устойчивы, что позволяет изучать их свойства и определять строение образующихся из них продуктов. При больших концентрациях радикалов RO2• в системе продуктами рекомбинации являются, главным образом, соединения ROOIn - хинолидные пероксиды были выделены при ингибировании процессов окисления углеводородов 2,4,6 - триалкилфенолами. Выход хинолидных пероксидов при окислении низкомолекулярных углеводородов в присутствии пространственно - затрудненных фенолов достигает 100%.
Эффективность ингибитора в общем случае определяется величиной константы скорости реакции RO2• + InH. Однако, если отрыв атома водорода протекает слишком легко, то это может привести к прямому взаимодействию ингибитора с кислородом, что снижает его эффективность и увеличивает вероятность дополнительных реакций радикалообразования.