БОЛЕВОЙ АНАЛИЗАТОР
Болевой анализатор построен по общему принципу, его активация сопровождается возникновением боли.
Боль – это неприятные в виде страданий ощущения, возникающие всякий раз, когда сверхсильные механические, термические раздражители, действуя на ткани организма, разрушают или создают угрозу разрушения целостности их защитных покровных оболочек. Одной из причин боли является нарушение процессов тканевого дыхания. Например, боль всегда сопровождает ишемию, при этом она тем сильнее, чем выше уровень функциональной активности ткани. Так, в сокращающихся скелетных мышцах верхних конечностей при пережатии их артериальных сосудов манжеткой боль появляется через 15-25 с. В отсутствии сокращений боль появляется через 3-4 мин. Возникновение боли при остром нарушении кровообращения является следствием расстройства микроциркуляции, кислородного голодания клеток, активации анаэробного дыхания, накопления в межклеточном пространстве органических кислот, разрушения клеток, появления в межклеточном пространстве протеолитических ферментов, биологически активных веществ тканевого или плазменного происхождения. Многие химические вещества, постепенно накапливающиеся в тканях при кислородном голодании, оказывают прямое раздражающее влияние на нервные элементы, вызывая у человека отчетливые изменения в работе вегетативных эффекторов. К ним следует отнести перестройки в работе желез внутренней секреции (гипофиза, надпочечников), изменения в работе аппарата внешнего дыхания, ускорение свертывания крови, повышение ее фагоцитарной активности, лейкоцитоз, усиление выработки антител, системное усиление кровотока, местное расширение сосудов в болевом очаге, улучшающее трофику тканей, доставку клеткам кислорода.
Кроме вегетативных в целостной картине боли дополнительно можно выделить еще ряд относительно самостоятельных компонентов (Р. Шмидт, Л. В. Калюжный). Прежде всего, это – сенсорный компонент, отражающий возникновение ощущения боли; далее – негативно-эмоциональный компонент в виде характерных тягостных переживаний; наконец, двигательный компонент (поведенческий акт, щащение поврежденного органа), направленный на устранение причины, вызвавшей боль.
Типы болей и их характеристика
По месту возникновения боль разделяют на соматическую и висцеральную. Примером соматической боли является боль, вызываемая введением инъекционной иглы под кожу человека. В чувственной картине такой боли выделяют два компонента. Первый – «быстрый», непродолжительный, легко локализуемый компонент, отражающий ощущение четкой, яркой боли, возникающей с латентным периодом порядка 0,1 с. Это соматическая поверхностная боль. Второй – «медленный», поздний, плохо локализуемый компонент, отражающий ощущение тупой боли, возникающей с латентным периодом порядка 1 с и более, постепенно увеличивающейся по выраженности в течение нескольких секунд или минут. Это соматическая глубокая боль.
Соматическая глубокая боль возникает в мышцах, суставах, суставных связках, костных образованиях. Типичным примером такой боли является зубная (дентальная) боль. Глубокая боль почти всегда плохо локализуется. Так, зубная боль, вызванная развитием воспалительного процесса в пульпе зубе, может обнаружить себя первично в различных участках лица, шеи, головы.
Висцеральная боль по своим качественным характеристикам во многом совпадает с глубокой соматической болью. Основные причины ее возникновения: 1) ишемия тканей, приводящая к накоплению метаболитов и нарушению тканевого дыхания; 2)выход содержимого полых органов при повреждении целостности их стенок (например, выход содержимого аппендикса в брюшную полость при его воспалении и разрыве); 3) cильные тонические сокращения или растяжения мышц желудка, желчного пузыря, кишечника, мочевого пузыря, мочеточников.
По продолжительности различают боль острую, подострую и хроническую.
Острая – внезапно возникающая боль. В практике врача-стоматолога острую боль можно вызвать у больного в ходе обследования кариозной полости пораженного зуба зондом. Острая боль обычно имеет предупредительное, т. е. сигнальное значение.
Хроническая – длительная, долго сохраняющаяся или регулярно повторяющаяся боль разной интенсивности. Примером такой боли могут служить определенного вида головные боли, боли в спине при остеохондрозе, при опухолях на поздних стадиях их развития.
Подострая боль – занимает промежуточное положение по своим характеристикам между острой и хронической видами боли.
Здесь же отметим мгновенную, приступообразную, непрерывную, пульсирующую виды боли, отражающие субъективное качественное восприятие интенсивности боли в пределах некоторого временного интервала.
По отношению боли к причинам ее возникновения различают боль физическую и психогенную.
Физическая боль возникает в результате действия на тканевые структуры организма различных раздражителей. Психогенная боль является следствием нарушения психических функций человека.
Болевой анализатор, как и все другие, имеет три отдела.
Периферический отдел болевого анализатора. Локализация ноцицепторов.
Представления о том, что боль возникает при «чрезмерном раздражении любых сенсорных рецепторов», в настоящий момент практически оставлены, т. к. получены убедительные доказательства того, что боль возникает в результате воздействия раздражителей на специализированные высокопороговые болевые рецепторы, или ноцицепторы (от латинского nocere - разрушать).
Гистологически ноцицепторы кожи, слизистых, фасций, сухожилий, скелетных мышц, надкостницы, суставных поверхностей, адвентициальной оболочки мелких кровеностных и лимфатических сосудов (близ просвета), эндоневрия нервных стволов, мозговых оболочек, тканей внутренних органов представляют собой свободные – неинкапсулированные окончания нервных волокон, имеющие разнообразную форму волосков, сплетений, спиралей, пластинок.
Большое число ноцицепторов – «болевых точек» можно насчитать на поверхности кожи. Оно намного превышает число рецепторов прикосновения, тепла, холода. Наибольшая плотность кожных ноцицепторов у человека отмечается в паховой области – 100-200 на 1 см2, на ладони, кончике носа, на поверхности уха их меньше – всего 40-70 на 1 см2 . Очень много свободных нервных окончаний сосредоточено в пульпе зуба. Неслучайно, даже не очень сильная электрическая или механическая стимуляция пульпы зуба у человека сопровождается отчетливыми болевыми ощущениями. В целом количество ноцицепторов в тканях зуба достигает очень больших величин. Так, в пересчете на 1 см2 на границе соприкосновения эмали и дентина располагается примерно 75000 ноцицепторов. На слизистой полости рта есть участок, практически не имеющий ноцицепторов. Он тянется от второго коренного зуба к углу рта на внутренней поверхности щеки в виде узкой полосы. Топография болевой чувствительности слизистой оболочки рта представлена на рис. 1.
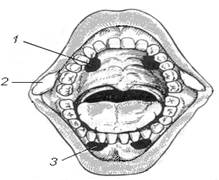
Рис. 1. Топография различной степени выраженности болевой чувствительности слизистой рта. 1, 3 – участки максимальной чувствительности верхней челюсти; 2 – отсутствие болевой чувствительности;
Физиологические свойства ноцицепторов. Большинство ноцицепторов реагируют на механические, термические и химические раздражители. Обычно «быстрая» боль вызывается механическими и термическими болевыми раздражителями. «Медленная» боль вызывается тремя видами болевых раздражителей – механическими, термическими и химическими болевыми раздражителями.
Функционально основная часть болевых рецепторов различных тканевых структур человека представляет собой мультимодальные ноцицепторы (Л. Н. Смолин). К ним относятся кожные механотермоноцицепторы, подкожные механотермоноциценторы, механотермохемоноцицепторы, механохемоноцицепторы мышц, внутренних паренхиматозных органов. Мономодальные ноцицепторы (механоноцицепторы, термоноцицепторы)встречаются редко.
Электрофизиологический механизм возникновения рецепторных потенциалов ноцицепторов изучен недостаточно.
Высказываются предположения, что в случае механического воздействия на мембрану ноцицептора рецепторный потенциал возникает в результате деформации и растяжения фрагмента мембраны, активирующих перенос катинов натрия внутрь ноцицептора. Возможен и иной механизм возникновения рецепторного потенциала. Предполагается, что под влиянием механического воздействия из терминалей сенсорной клетки выделяется медиатор. В последующем он реагирует со специфическими хеморецепторами мембраны ноцицептора, запуская генерацию рецепторного потенциала (рис. 2).
В случае термического воздействия – формирование рецепторных потенциалов протекает, очевидно, также с участием медиатора, выделяющегося из терминалей сенсорной клетки в ответ на изменение интенсивности метаболических реакций под влиянием температуры. Медиатор вступает в реакцию с хеморецепторами, запуская генерацию рецепторного потенциала, при этом динамика развития рецепторного потенциала, отражающая скорость взаимодействия медиатора с хеморецепторами и предопределяющая частоту возникающих потенциалов действия, по-видимому, модулируется температурным воздействием на ноцицептор (А. Гайтон, Дж. Холл).
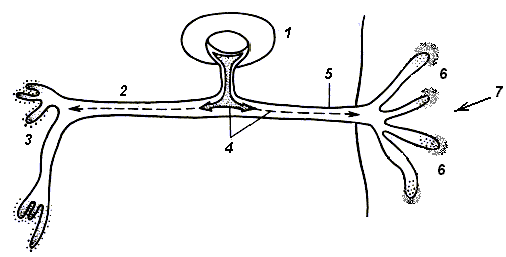
Рис. 2. Механизм возможной активации ноцицептора под влиянием сильного механического воздействия (По Ф. Лембеку, П. Холтону, Дж. Генри, В. Зилову, В. Бадикову и др., с изменениями)
1 – тело сенсорного нейрона; 2 – аксон; 3 – пресинаптические окончания аксона; 4 – медиатор (вещество Р); 5 – дендрит; 6 – свободные нервные окончания, на них выделившийся медиатор (облака, вокруг окончания), действующий на рецепторы этих же свободных нервных окончаний.; 7 – сильное механическое воздействие.
При воспалительных реакциях ощущение боли у человека обычно возникает в результате активации ноницепторов химическими веществами – алгогенами, действующими, как выяснилось, и на ноцицептор, и на проводниковую мембрану сенсорного нейрона в составе своеобразного химического конвейера. В него входят тканевые алгогены, появляющиеся в результате разрушения тканевых структур (гистамин, серотонин, простагландины, катионы калия и т. д.), а также плазменные алгогены, появляющиеся в результате выхода в межклеточное пространство компонентов крови, катализирующих механизм образования кининов – в первую очередь каллидина и брадикинина, в значительной степени усиливающих активацию ноцицепторов.
Подчеркнем, что алгогены всех типов отчетливо угнетают клеточное дыхание. Это обстоятельство допускает возможность существования некоего общего механизма раздражающего влияния алгогенов на ноницепторы избыточными концентрациями катионов водорода.
Проводниковый отдел болевого анализатора представлен тонкими миелинизированными волокнами типа Аδ (группа III) и в основном тонкими немиелинизированными волокнами типа С (группа IV) – по классификации Гассера.
Доказательства участия волокон Аδ и С в передаче болевой импульсации были получены в ходе оценки ощущений у испытуемых при градуальной электрической стимуляции кожных нервов.
Болевая импульсация от тела организма по волокнам Аδ поступает в задние рога спинного мозга, где в поверхностном слое (краевая зона) происходит переключение на нейрон второго порядка. Предполагается, что передача возбуждения здесь обеспечивается глютаминовой кислотой – одним из наиболее распространенных медиаторов ЦНС. Далее, аксоны нейронов второго порядка переходят на противоположную сторону, направляясь в ствол мозга в составе переднего спиноталамического тракта. На своем пути в стволе мозга волокна переднего спиноталамического тракта отдают коллатерали к ядрам стволовой ретикулярной формации. В дальнейшем они вступают в таламус, где происходит переключение на нейроны специфического сенсорного комплекса ядер вместе с волокнами дорзальных столбов, формирующих медиальную петлю и обеспечивающих передачу возбуждения от проприорецепторов, а также рецепторов прикосновения кожи лица, туловища, конечностей.
С–волокна вступают в задние рога спинного мозга в составе задних корешков. В области желатинозной субстанции меньшая часть волокон переключается на вставочные нейроны, тогда как большая часть направляется дальше, переключаясь на нейроны задних рогов, аксоны которых переходят на противоположную сторону, направляясь в ствол мозга в составе латерального спиноталамического тракта. Предполагается, что окончания С–волокон, контактирующие с нейронами спинного мозга, выделяют два медиатора – глютаминовую кислоту и субстанцию Р. Глютаминовая кислота действует исключительно быстро, реализуя свой специфический эффект на клетку-мишень в течение нескольких миллисекунд, тогда как, субстанция Р реализует свои эффекты весьма медленно из-за того, что наращивание ее эффективной концентрации осуществляется в течение секунд или даже минут (А. Гайтон, Дж. Холл).
Волокналатерального спиноталамического тракта на уровне ствола мозга вступают в контакт с различными нейронными структурами. Среди них – серое околоводопроводное вещество, ядра тектальной области, ядра ретикулярной формации продолговатого мозга, моста, среднего мозга. Многократно переключаясь на ретикулярных нейронах с короткими аксонами, возбуждения в последующем направляются преимущественно в неспецифические ядра таламуса. Частично эти возбуждения направляются в специфические ядра таламуса, а также в структуры гипоталамуса и других подкорковых образований мозга. 10-20% волокон латерального спиноталамического тракта вступают в неспецифические ядра таламуса, проходя ствол мозга транзитом – без переключений.
Болевая импульсация от кожи лица, слизистой полости рта, периодонта, пульпы зуба (рис. 3) по волокнам Аδ («быстрая» боль) и С («медленная» боль) в составе тройничного нерва направляется в продолговатый мозг, где они в основном заканчиваются на нейронах ядра спинального тригеминального тракта. Часть волокон подходит к ядрам ретикулярной формации продолговатого мозга, а также – к ядрам шва.
Выходные нейроны ядра спинального тригеминального тракта образуют несколько восходящих трактов. «Быстрая» болевая импульсация, возникающая при действии механических раздражителей на ноцицепторы самых различных структур челюстно-лицевой области, проводится по вентральному и дорзальному тригемино-таламическим трактам, заканчивающихся на нейронах специфических ядер и, частично, на нейронах неспецифических ядер таламуса.
Главная роль в проведении «медленной» болевой импульсации от органов челюстно-лицевой области отводится тригемино-ретикуло-таламическому тракту, обеспечивающего генерализованную передачу болевой импульсации через нейронные сети ретикулярной формации к ядрам неспецифического таламуса, а также к структурам лимбико-гипоталамической области головного мозга.
Таким образом, можно отметить, что принципиальных различий в организации проведения болевой импульсации от органов челюстно-лицевой области и прочих участков тела человека не имеется.
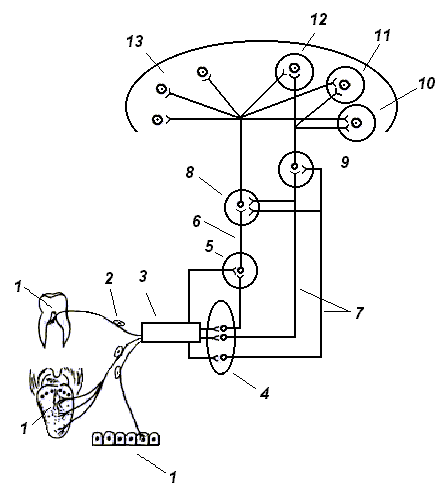
Рис. 3. Схема, иллюстрирующая восходящие болевые (ноцицептивные) пути (волокна типа С) от органов челюстно-лицевой области (По Ю. П. Лиманскому, С. М. Будылиной, В. П. Дегтяреву, с изменениями).
1– ноцицепторы пульпы, языка, слизистой оболочки, кожи лица; 2 – сенсорные клетки гассерова ганглия; 3 – сенсорный корешок тройничного нерва; 4 – ядро спинального тригеминального тракта; 5 – ретикулярная формация; 6 – тригемино–ретикуло–таламический тракт; 7 – вентральный и дорзальный (ипсилатеральный) тригемино-таламические тракты; 8 – неспецифические ядра таламуса; 9 – специфические ядра таламуса; 10 – орбитофронтальная область коры; 11 – поле С1; 12 – Поле С2; 13 – генерализованные (неспецифические) таламо-кортикальные проекции.
Участие коры больших полушарий в формировании болевых ощущений. На основании ряда экспериментальных данных казалось очевидным, что ведущими центрами болевой чувствительности организма являются ретикулярная формация ствола мозга, гипоталамус. Конечной собирательной инстанцией болевой импульсации рассматривался таламус, а не кора головного мозга. Один из аргументов в пользу таких представлений основывался на результатах наблюдений над животными, у которых полностью удалялись соматосенсорные корковые поля. Как выяснилось, животные после операции в ответ на действие болевых раздражителей демонстрировали признаки «переживания» боли почти во всех компонентах. В дальнейшем было показано, что электрическая стимуляция ядер ретикулярной формации, неспецифических ядер таламуса ведет к усилению вегетативных, гормональных, соматических проявлений болевой активации оперированных животных. Следовательно, можно было заключить, что корковые структуры в реакциях организма на болевые раздражители функционально выполняют преимущественно вспомогательные функции выделения участков тела, выступающих источником болевой импульсации, оценки качества боли, ее специфического «портрета».
Тщательное изучение проблемы боли привело к изменению представления о роли коры больших полушарий в формировании болевых ощущений, как и любых других. В частности, было установлено, что изолированное повреждение корковых областей мозга в глубине теменной части центральной борозды человека вызывает устойчивую нечувствительность к боли (частичную или полную) в контралатеральной половине тела (Р. Шмитд). Эти данные совпали с данными, полученными при проведении нейрохирургических вмешательств, сопровождавшихся локальной электрической стимуляцией глубинных участков теменной части центральной борозды. Оказалось, что такая стимуляция всегда сопровождалась отчетливыми ощущениями боли, что ранее отрицалось. Таким образом, стало ясным, что полноценное чувственное восприятие боли организмом без участия коры головного мозга является невозможным. Этот вывод представляется важным в контексте приоритетной роли коры большого головного мозга в привязке биологически отрицательных эмоциональных состояний к организации целенаправленных поведенческих актов, освобождающих организм от такого рода состояний (К. В. Судаков).
С точки зрения имеющейся на сегодняшний день информации частные функции корковых проекционных полей болевого анализатора сводят к следующему.
Первичное соматосенсорное проекционное поле (С1) – обеспечивает восприятие «быстрой» боли, идентификацию места ее возникновения на теле. Интересно, что абсолютно точная идентификация участка кожной поверхности, на которую действует болевой раздражитель, требует параллельного вовлечения в процесс кожных тактильных рецепторов. Показано, что без подключения кожных тактильных рецепторов показатели идентификации болевого участка на коже значимо ухудшаются.
Полю С1 отводится ведущая роль в экстренном включении моторной защитной реакции организма в ответ на действие болевого раздражителя. Морфологически и функционально соответствующие моторные реакции обеспечиваются прямыми синаптическими связями нейронов поля С1 с нейронами моторной коры.
Ощущения «медленной» боли обычно идентифицируются плохо. Испытуемый в опыте или пациент в клинике чаще всего сообщают, что боль возникает в «руке», в «ноге», в «затылке» и т. д. Невозможность четко локализовать «медленную» боль объясняется тем, что пути ее проведения представляют в основном мультисинаптические нейронные цепи ретикулярной формации, неспецифических ядер таламуса, генерализованно передающих возбуждения в самые различные корковые поля, в том числе в поля С1 и С2 болевого анализатора.
Вторичное соматосенсорное проекционное поле С2 располагается на границе пересечения центральной борозды с верхним краем височной доли. Нейроны данного поля имеют двусторонние связи с ядрами таламуса. Это позволяет полю С2 избирательно фильтровать проходящие через таламус возбуждения, прежде всего болевого происхождения. После их выделения, поля С2 вовлекаются в многостадийные процессы системной деятельности мозга, связанные с извлечением из памяти энграммы потребного поведенческого акта, его реализации на эффекторах, оценки качества достигнутого в поведении полезного результата.