Всесторонние исследования выявили стойкие патофизиологические изменения после вакцинации вакцинами COVID-19.
- Цзипин Лю,
- Цзюньбан Ван,
- […]
- Чжунминь Лю
Cell Discovery объем 7, Номер статьи: 99 (2021) Цитируйте эту статью
· 250K Допуски
· 7226 Altmetric
· МетрикиДетали
Абстрактный
В настоящее время во многих странах проводятся широкомасштабные вакцинации против COVID-19 в ответ на пандемию COVID-19. Здесь мы сообщаем, помимо образования нейтрализующих антител, постоянные изменения гемоглобина A1c, уровней натрия и калия в сыворотке, профилей свертывания крови и функций почек у здоровых добровольцев после вакцинации инактивированной вакциной SARS-CoV-2. О подобных изменениях также сообщалось у пациентов с COVID-19, что свидетельствует о том, что вакцинация имитировала инфекцию. Одноклеточное секвенирование мРНК (scRNA-seq) мононуклеарных клеток периферической крови (PBMC) до и через 28 дней после первой инокуляции также выявило стойкие изменения в экспрессии генов многих различных типов иммунных клеток. Снижение CD8 +Показателями были Т-клетки и увеличение содержания классических моноцитов. Более того, scRNA-seq выявила усиление передачи сигналов NF-κB и снижение ответов интерферона I типа, которые были подтверждены биологическими анализами, а также, как сообщалось, возникали после заражения SARS-CoV-2 с отягчающими симптомами. В целом, наше исследование рекомендует проявлять дополнительную осторожность при вакцинации людей с ранее существовавшими клиническими состояниями, включая диабет, электролитный дисбаланс, почечную дисфункцию и нарушения свертывания крови.
Вступление
Пандемия COVID-19 глубоко затронула человечество. Разработка вакцин против COVID-19 в различных формах идет беспрецедентными и ускоренными темпами. Несмотря на некоторую неопределенность относительно возможных последствий, во многих странах проводятся широкомасштабные вакцинации. Были разработаны различные вакцины против COVID-19, включая инактивированные вирусные частицы, мРНК-вакцины, вакцины на основе аденовирусов и т. Д. 1, 2, 3, 4, 5. Исторически исследования вакцин были сосредоточены на том, может ли вакцинация генерировать нейтрализующие антитела для защиты от вирусных инфекций, в то время как краткосрочное и долгосрочное влияние различных недавно разработанных вакцин на патофизиологию человека и другие аспекты иммунной системы человека не влияли. были полностью исследованы.
С развитием крупномасштабной технологии секвенирования одноклеточной мРНК (scRNA-seq) стало возможным систематическое исследование функции иммунной системы людей с точностью, прежде всего с помощью scRNA-seq мононуклеарных клеток периферической крови (PBMC). Во время пандемии COVID-19 большое количество исследований с использованием scRNA-seq PBMC выявило детальные изменения в экспрессии генов в различных подтипах иммунных клеток, включая различные типы T- и B-клеток, NK-клеток, моноцитов, дендритных клеток и т. Д. и после заражения, результаты которого показали значительное снижение CD4 + и CD8 +Количество Т-клеток и истощение Т-клеток при заражении SARS-CoV-2. Также наблюдались уменьшение количества неизменных T-клеток, связанных с периферическими слизистыми (MAIT), и их миграция в легкие и из них. У пациентов с COVID-19 были зарегистрированы высокоактивированные воспалительные иммунные ответы, включая интерферон-гамма (IFN-γ), интерлейкин-6 (IL-6) и NF-κB 6, 7, 8, 9, 10, 11.,12. Многие исследования выявили различия в иммунном состоянии между людьми с тяжелыми и легкими симптомами, в том, что сильные ответы на интерферон I типа (IFN-α / β) были полезными после заражения COVID-19, а ослабленные ответы IFN-α / β были связаны с развитием тяжелые симптомы 13. Напротив, более сильные воспалительные реакции NF-κB были связаны с более серьезными симптомами 14. Кроме того, сообщалось, что увеличение количества γδ-Т-клеток и снижение содержания нейтрофилов связано с более легкими симптомами 15.
После инфекций SARS-CoV-2 у многих людей развились респираторные синдромы различной степени, а у некоторых - желудочно-кишечные заболевания. Ранее сообщались, что нарушения свертывания крови, проблемы сосудистых, электролиты дисбаланс, заболевание почек, нарушение обмена веществ и т.д. были основные клинические осложнения с COVID-19 16, 17. Способ, которым вакцинация имитирует инфекцию, полностью не изучен. В это исследование мы включили здоровых добровольцев, которые должны были быть вакцинированы инактивированной вакциной против SARS-CoV-2 (Vero Cell) 3., для участия в тестах на антитела и нейтрализующие антитела, а также в детальных клинических лабораторных измерениях до и в разное время после вакцинации (применялись двухдозовые схемы с немного разными графиками). К нашему удивлению, мы наблюдали довольно последовательные патофизиологические изменения, касающиеся содержания электролитов, профилей коагуляции, функции почек, а также особенностей, связанных с метаболизмом холестерина и глюкозы, как если бы эти люди перенесли инфекцию SARS-CoV-2. Кроме того, результаты scRNA-seq PBMC также указали на последовательное снижение CD8 +.Т-клетки и увеличение содержания моноцитов, а также усиление воспалительной передачи сигналов NF-κB, что также имитировало ответы после инфекции. Удивительно, но реакции интерферона I типа, которые были связаны с уменьшением повреждений после заражения SARS-CoV-2 и более легкими симптомами, оказались уменьшенными после вакцинации, по крайней мере, через 28 дней после первой прививки. Это может означать, что в краткосрочной перспективе (1 месяц) после вакцинации иммунная система человека находится в непривилегированном состоянии и может потребовать дополнительной защиты.
Полученные результаты
Длительное наблюдение за образованием антител против SARS-CoV-2 и нейтрализующих антител после инокуляции инактивированной вакцины против SARS-CoV-2
В этом исследовании приняли участие 11 здоровых взрослых добровольцев обоего пола в возрасте 24–47 лет с ИМТ 21,5–30,0 кг / м² (рис. 1а и дополнительные таблицы S1 и S2). Вакцину против SARS-CoV-2 (Vero Cell), инактивированную (Beijing Institute of Biological Products Co. Ltd), вводили внутримышечно в дельтовидную мышцу. Добровольцы были разделены на две когорты; пять участников (когорта A) были вакцинированы полной дозой (4 мкг) инактивированной вакцины SARS-CoV-2 (Vero Cell) в дни 1 и 14, а шесть участников (группа B) получили полную дозу вакцины в дни 1 и 28 (рис. 1а). Один из добровольцев в группе B дал положительный результат на IgM и IgG к SARS-CoV-2 прямо перед вакцинацией, что наводит на мысль о потенциальных предшествующих инфекциях. Однако не было зарегистрировано ранее положительных результатов диагностики COVID-19 с помощью нуклеиновых кислот (NA) (отмечено зеленым цветом на рис. 1a). Для всех последующих обследований данные этого человека были отмечены зеленым, чтобы отслеживать любые возможные влияния от потенциальных предыдущих инфекций.
Рис. 1: Схема рабочего процесса и обнаружение антител / нейтрализующих антител SARS-CoV-2 после вакцинации.
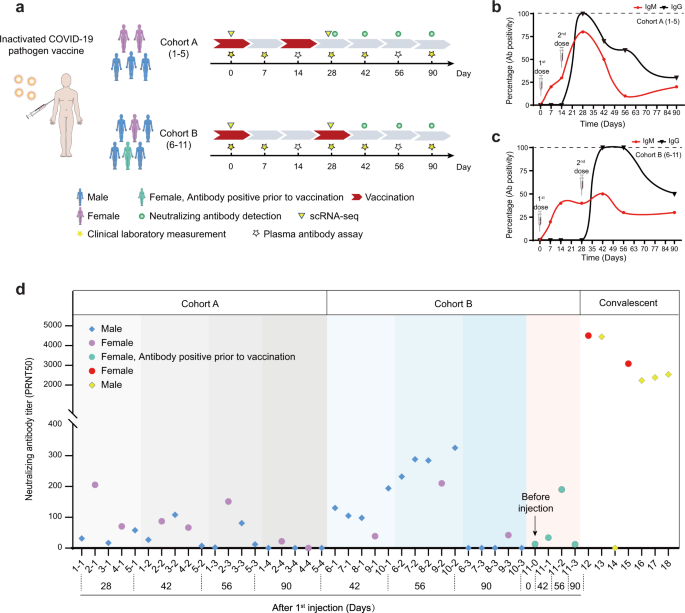
a Схематическое описание стратегий прививки вакцины, сбора образцов крови и измерений. b, c Изменения положительных антител (процент положительных / общих) с течением времени в когортах A и B. Добровольцы в когорте A были привиты в дни 1 и 14, а в когорте B - в дни 1 и 28. Красная линия представляет изменения IgM, и черный, IgG. d Нейтрализующие изменения титра антител в плазме добровольцев в когортах A и B после вакцинации, а также у испытуемых выздоравливающих лиц.
Полноразмерное изображение
Нежелательные явления отслеживались ежедневно в течение первых 7 дней после каждой прививки, а затем участники самостоятельно регистрировали их в дневниковых карточках в следующие недели. В целом побочные реакции были легкими (степень 1 или 2) и преходящими (дополнительная таблица S3). Образцы крови собирали в дни 0, 7, 14, 28, 42, 56 и 90, а образцы мочи собирали в дни 0, 14, 28, 42 и 90. Образцы плазмы подвергались воздействию анти-SARS-CoV- 2 Тестирование IgM / IgG с использованием нескольких диагностических наборов, результаты наиболее чувствительного набора использовались для количественной оценки (рис. 1b, c). Результаты тестирования когорты A продемонстрировали, что до 2-й прививки у 0% участников развился IgG к SARS-CoV-2, но к 28 дню, который был через 2 недели после 2-й прививки, 100% участников дали положительный результат (Рис. 1б). В целом, IgM обнаружился раньше, чем IgG, как и ожидалось. Положительность IgG и IgM снизилась к 42 дню и оставалась на относительно низком уровне к 90 дню в когорте A. В когорте B ни у кого не развился IgG до 2-й инокуляции. Однако к 42-му дню положительность IgG достигла 100% (рис. 1c).) и сохранялась до 56 дня, что позволяет предположить, что протокол вакцинации когорты B был более эффективным. К 90 дню положительность IgG также снизилась до 50%, что указывает на то, что выработка антител не поддерживается в течение длительного времени. Далее мы провели тесты на нейтрализующие антитела SARS-CoV-2 18 (рис. 1d), и результаты также показали, что две прививки с интервалом 28 дней (когорта B) привели к более высоким титрам защитных антител по сравнению с двумя прививками с интервалом 14 дней (когорта А). С другой стороны, оказалось, что титры нейтрализующих антител против SARS-CoV-2 в целом были ниже, чем у выздоравливающих людей с COVID-19, как сообщалось ранее 3 (рис. 1d.). К 90 дню титры нейтрализующих антител резко снизились у всех добровольцев (рис. 1d). Интересно, что человек, у которого до вакцинации были антитела, не был более склонен к выработке нейтрализующих антител по сравнению с остальными участниками, что позволяет предположить, что предшествующая потенциальная инфекция могла не произойти или не могла обеспечить длительную защиту с точки зрения нейтрализации. производство антител.
Изменения в клинических лабораторных измерениях после вакцинации
Для выявления характеристик безопасности вакцины были измерены рутинные клинические лабораторные тесты, включая показатели, связанные с инфекцией, гематологические параметры, функцию свертывания крови, уровень глюкозы в крови, липиды сыворотки, ферменты, связанные с сердечной функцией, электролиты, биомаркеры, связанные с функцией печени и почек (рис.. 2а и дополнительные таблицы S4 и S5). Количество лейкоцитов было значительно, но лишь незначительно, увеличилось после вакцинации на 7-й день. Никаких различий не было обнаружено в следующие моменты времени (рис. 2b).). К нашему удивлению, у здоровых добровольцев наблюдалось довольно последовательное повышение уровней HbA1c, независимо от того, принадлежали они к когорте A или B. К 28 дню после 1-й прививки трое из 11 человек достигли преддиабетического диапазона (рис. 2c). К 42 и 90 дням средние уровни HbA1c, по-видимому, вернулись обратно, но все же были значительно выше, чем до вакцинации. Предыдущая работа показала, что пациенты с диабетом с неконтролируемым уровнем глюкозы в крови более склонны к развитию тяжелых форм COVID-19 19. Было показано, что высокий уровень глюкозы в крови / гликолиз способствует репликации SARS-CoV-2 в моноцитах человека за счет продукции митохондриальных активных форм кислорода и активации HIF1A 20., поэтому представляет собой невыгодную особенность.
Рис. 2: Временные изменения клинических лабораторных измерений после вакцинации.
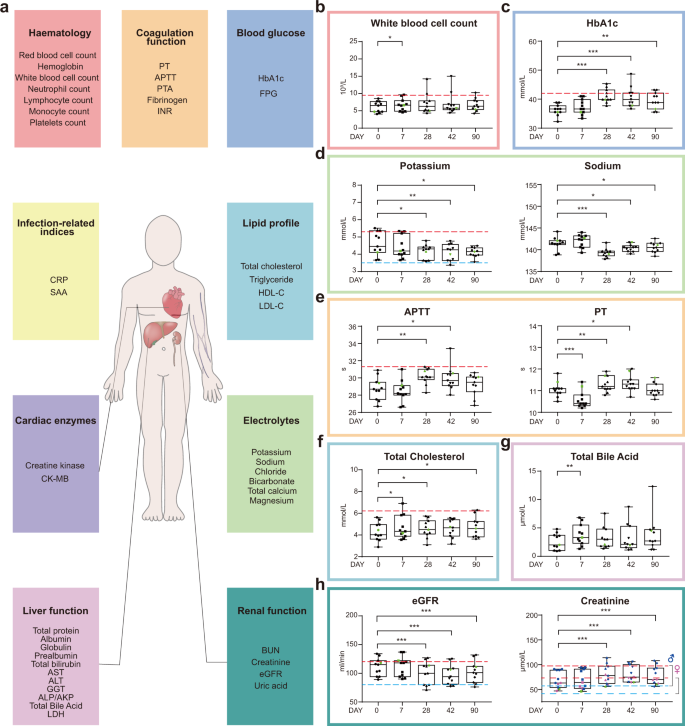
a Стандартные клинические лабораторные тесты включают гематологические параметры и параметры свертывания крови, показатели уровня глюкозы в крови и инфекции, липидный профиль, сердечные ферменты, электролиты, биомаркеры, связанные с функцией печени и почек. Дополнительную информацию можно найти в дополнительных таблицах S4 и S5. Значения лабораторных тестов количества лейкоцитов (b), HbA1c (c), калия (d, левая панель), натрия (d, правая панель), APTT (e, левая панель), PT (e, правая панель), всего холестерин (f), общая желчная кислота (g), рСКФ (h, левая панель), креатинин (h, правая панель). Точки данных представляют ценности каждого человека. Коробчатые диаграммы показали 25-й, 50-й (медиана) и 75-й процентили. Горизонтальные пунктирные линии показывают верхние нормальные пределы (красный) в b, c, d (левые панели), e (левая панель), f, h и нижние нормальные пределы (синие) в d (левая панель) и h. Значения P были рассчитаны с помощью критерия ранжирования знаков Вилкоксона путем сравнения лабораторных измерений каждый раз с базовыми измерениями. * P ≤ 0,05, ** P ≤ 0,01, *** P ≤ 0,001.