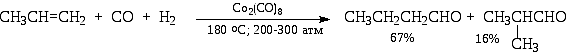1) Алкены вступают в различные реакции присоединения по месту двойной связи, так что одна молекула алкена присоединяет одну молекулу реагента (Br2, H2, H2O, HCl), в результате π-связь разрывается. Алкены присоединяют галогены — реакция галогенирования. При галогенировании обычно используют растворы галогенов в воде или органических растворителях (CCl4, CHCl3). В результате реакции галогенирования образуются дигалогенпроизводные алканов, содержащие атомы галогена у соседних атомов углерода:


Обесцвечивание желтого раствора брома в воде (или органическом растворе) — одна из качественных реакций на двойную связь. (Качественные реакции органических соединений суммированы в приложении 6.)
Алкены присоединяют водород — реакция гидрирования. В результате реакции гидрирования образуются алканы. Реакция протекает в присутствии катализатора (Ni, Pt) при комнатной температуре или нагревании:
Ni
CH2=CH2 + H2 → CH3–CH3
Ni
CH3–CH=CH2 + H2 → CH3–CH2–CH3
Алкены присоединяют воду — реакция гидратации. Продуктом реакции гидратации являются одноатомные насыщенные спирты (алканолы). Реакция протекает в присутствии катализатора (H2SO4, H3PO4, Al2O3):
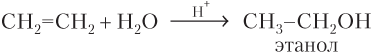
В случае несимметричных по строению гомологов этилена образуется смесь продуктов с преобладанием одного из них (см. конец данной главы), например:
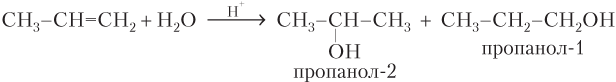
В результате реакции образуется больше пропанола-2 по правилу В.В. Марковникова (атом водорода присоединяется к наиболее гидрированому атому углерода).
Алкены присоединяют галогеноводороды — реакция гидрогалогенирования. В результате реакции гидрогалогенирования образуются галогеналканы, например:
CH2=CH2 + HBr → CH3–CH2Br
В случае несимметричных по строению гомологов этилена образуется смесь продуктов с преобладанием одного из них (см. конец данной главы):
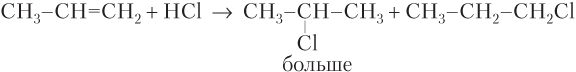
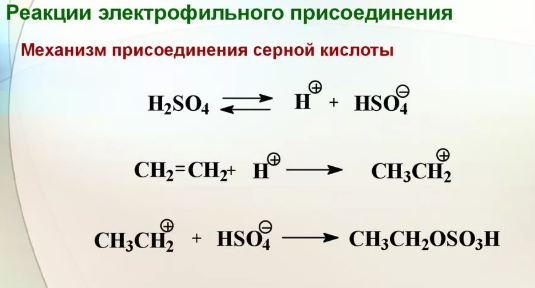
Алкены вступают в реакцию с концентрированной серной кислотой на холоде и азотной кислотой с образованием сложных эфиров:
CH2=CH2 + HO-NO2 → CH3-CH2ONO2
Пример 22.2. Напишите уравнения реакций HBr: а) с бутеном-2; б) бутеном-1. В каком случае образуется смесь продуктов?
Решение. Записываем уравнения реакций:
а) 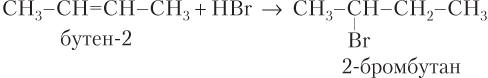
б) 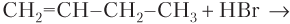
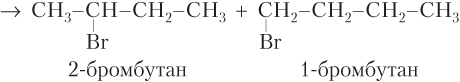
Смесь продуктов образуется в случае б), так как молекула бутена-1 имеет несимметричное строение относительно положения в ней двойной связи.
Ответ: б).
2) Алкены вступают в реакции окисления. Окисление пероксидом водорода, перманганатом калия в нейтральной или слабощелочной среде приводит к разрыву π-связи и образованию двухатомных спиртов — гликолей:
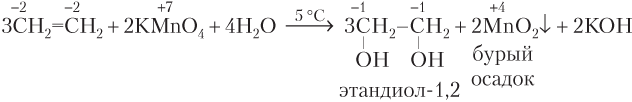
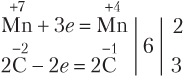
или упрощенно
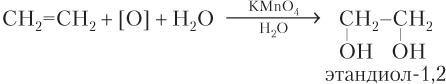
Исчезновение розовой окраски KMnO4 — качественная реакция на двойную связь.
В кислой среде реакции окисления приводят к разрыву кратной связи с образованием карбоновых кислот, кетонов или альдегидов:
CH3–CH=CH–CH3 + KMnO4 + H2SO4 → CH3COOH + MnSO4 + K2SO4 + H2O
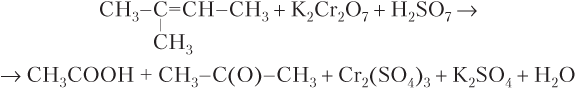
В качестве окислителей могут использоваться надкислоты (содержат пероксидную группу –O–O–), кислород в присутствии катализатора. В первом случае — реакция Прилежаева — получается эпоксид:
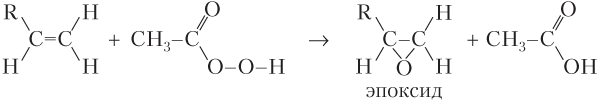
При использовании кислорода в зависимости от природы катализатора можно тоже получить эпоксид, например:
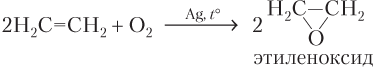
или альдегид:
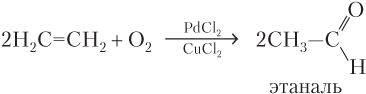
В избытке кислорода алкены сгорают с образованием углекислого газа и воды — полное окисление:
2C3H6 + 9O2 → 6CO2 + 6H2O
или в общем виде
C n H2 n +3 n/ 2O2→ n CO2+ n H2O
3) Алкены вступают в реакции полимеризации — реакции соединения большого числа молекул с образованием высокомолекулярного соединения (ВМС, полимера).
Исходный алкен или другое низкомолекулярное вещество называется мономером, а многократно повторяющиеся группы атомов в полимерной цепи — структурными или мономерными звеньями. Число мономерных звеньев в полимерной цепи называется степенью полимеризации (обозначается n):
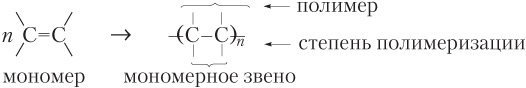
Скорость реакции полимеризации повышают инициаторы (например, пероксиды R–O–O–R), легко распадающиеся на свободные радикалы RO•. Остатки RO• находятся на концах полимерных молекул.
Примеры уравнений реакций полимеризации различных алкенов, которые нужно уметь записывать не только для этилена (радикал CH2=CH– называется винил), но и для более сложных молекул (для удобства записи молекулу алкена записываем как бы с «оголенной» двойной связью, заместители при атомах C двойной связи направляются вверх или вниз):
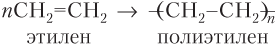
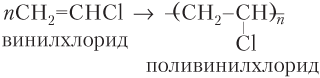
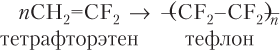
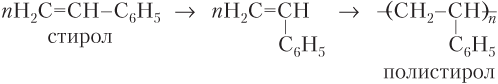
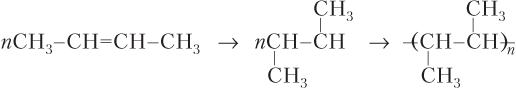
Чтобы найти степень полимеризации полимера, надо среднюю молярную массу полимера Mср разделить на молярную массу структурного звена М стр.зв:
n = Mср / M стр.зв.
Например, если Mср полиэтилена равна 70 000 г/моль, молярная масса мономерного звена –CH2–CH2– равна 28 г/моль, то согласно приведенной формуле степень полимеризации равна:
n =70 000/28=2500,
Таким образом макромолекула полиэтилена содержит 2500 повторяющихся групп –CH2–CH2-.
Как правило, полимеризация алкенов типа CH2=CHX протекает по принципу «голова к хвосту» (головой называется часть молекулы, содержащая заместитель, Х, а хвостом — другая ее часть):
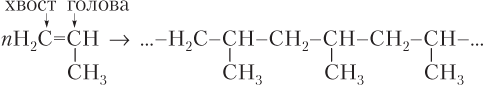
Пример 22.3. Составьте уравнения реакций полимеризации: а) пропена; б) бутена-1; в) 2-метилпропена (изобутена).
Решение. Записываем уравнения реакций:
а) 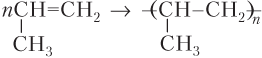
б) 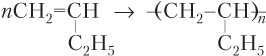
в) 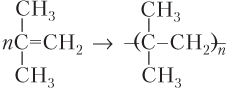
4) Реакция терморазложения:
t
3C2H4 → 2CH4 + 2C2H2
>t
3C2H4 → 2CH4 + 2C2H2
>350 ֠C
3C2H4 → 2CH4 + 2C2H2
5) Гидроформилирование алкенов: