УЧЕБНОЕ ПОСОБИЕ К ПРАКТИЧЕСКИМ ЗАНЯТИЯМ ПО ХИМИИ
Утверждено на заседании каф. 908
1 сентября 2012 г
ЧАСТЬ 1-ая.
СОКРАЩЕНИЯ В ТЕКСТЕ
кр. - кристаллический
г. - газообразный
ж. - жидкий
гр. - графит
н.у. - нормальные условия (10132 Па 273 К)
р. - раствор
н. - бутан - нормальный бутан
т.с. - теплотворная способность
водн. - водный
νj, νi- - стехиометрические коэффициенты продуктов
реакции и реагентов
мех. - механическая
Глава 1. ОСНОВЫХИМИЧЕСКОЙ ТЕРМОДИНАМИКИ
1.1. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ. ПРОЦЕССЫ
ПРИ ПОСТОЯННОМ ДАВЛЕНИИ И ПРИ ПОСТОЯННОМ
ОБЪЕМЕ
Пример 1. Рассчитайте разницу между тепловыми эффектами при постоянном давлении и постоянном объеме (Qp — Qv) реакции
С2 H4 0(г) + H2 (г) =C2 Н5 0Н(Ж), протекающей при 298 К. Чему равна эта разница, если температуру повысить до 400 К и спирт перевести в газообразное состояние?
Решение. 1-й закон термодинамики можно выразить уравнением
ΔU = Q - Aмех
где ΔU - изменение внутренней энергии системы (U2-U1) при переходе системы из состояния "1" в состояние “2"; Q — теплота; Aмех - работа механическая, равная рΔV, где р - давление, а ΔV- изменение объема (V2-V1).
Тепловой эффект процесса, протекающего при р=const
Qp= ΔH = ΔU+pΔ, (1.1.2)
ΔH - изменение энтальпии.
Тепловой эффект процесса, протекающего при р = const
Qp-Qv=pΔV=ΔnRT,
где R - газовая постоянная = 8,3144 Дж/моль *К; Δn=n2-n1 ;
n1 и n2 - количество молей реагентов и продуктов реакции газообразных веществ; T - температура, К.
Отсюда: 1) при 298 К Qр - Qv = ΔnRT = (0-2) 8,3144-298 = -4955,38 Дж;
2) при 400 К и газообразном С2Н5ОН Qp – Qv = (1-2) 8,3144-400 = -3325,76 Дж.
Ответ при 298 К Qp-Qv = -4955,38 Дж;
при 400°К Qp - Qv= -3325,76 Дж.
Пример 2. Определить стандартную энтальпию образования
ацетилена по энергиям связей отдельных его атомов:
2С(гр) + H2 → C2H2; Δ Hообр.
Решение. Стандартная энтальпия (теплота) образованиям Δ Hообр - тепло, поглощенное или выделенное в процессе синтеза 1 моля соединения из простых веществ при условии, что все компоненты системы находятся в стандартных состояниях.
Верхний индекс Δ Hо здесь и в последующих случаях Δ Gо, Δ Sо, Δ Fо обозначает, что реагирующие вещества находятся в своих стандартных состояниях. Стандартное состояние для газов - это состояние идеального газа при давлении 1 атм (101330 Па) и определенной температуре. Для жидкости - это состояние чистой жидкости, а для твердых веществ — это кристаллическое состояние при тех же условиях. Строго говоря, температура должна быть точно указана в виде индекса.
Например, Δ Hо 273 , однако, если не оговорено, то стандартное состояние относится к 298 К. Образование молекулы ацетилена Н – С ≡С- Н сопровождается образованием двух связей Н - С (358,2 кДж/моль) и одной связи С ≡ С (536 кДж/моль); разрушением связи H – H (430 кДж/моль) и переходом 2C(rp) → 2-С(г) (525 кДж/моль).
Образование связи сопровождается выделением энергии, разрушение - поглощением.
Δ Hообр C2H2 = (-358,2*2)+(-536)+430+525*2=227,6 кДж/моль.
Ответ. Δ Hообр C2H2 = 227,6 кДж/моль.
Задачи
1.Вычислить разность между Qp и Qv при 298 К для реакции полного сгорания бензола С6Н6, нафталина С10 Н8 и этилена C2H4 с образованием диоксида углерода и воды в жидком состоянии.
2. Найти разность между Qp и Qv при 298 К для следующих реакций:
N2(г) + 3H2(г) ⇄ 2NH3(г); 2SO2(г)+O2(г) ⇄2SO3(г)
2C(гр)+O2(г)=2CО2(г); NH4CL(кp) ⇄ NH3(г)+ HCL(г).
3. Тепловой эффект реакции 1/2 N2(r)+3/2 H2(г) ⇄NH3(г) при постоянном давлении, при температуре 298 К Qp = Δ H= = -46,26 кДж/моль.
Определить Qv для этой реакции при этой же температуре.
4. Тепловой эффект изобарного процесса, протекающего по реакции
2Fe(кр)+3/2 О2(г)=Fe2O3 (кр), при 291 К равен -82З,З кДж/моль. Определить тепловой эффект для изохорного процесса, протекающего по этой реакции при той же температуре.
5. Вычислить разность между Qp и Qv при 773 К для реакции CO2(г) + C(гр)= CO(г) и
3C2H2(г) → C6H6(г).
6. Энергия диссоциации H2, Cl2 и стандартная энтальпия образования HCl соответственно составляют 436,243 и -92 кДж/моль. Вычислить энергию связи H-Cl.
7. Рассчитайте тепловой эффект сгорания метилацетата по энергиям связей при 298 К. Реакция сгорания метилацетата протекает по уравнению
CH3COOCH3(ж) + 3,5O2(г) → 3H2O(г) + 3CO2(г); Δ Hо.
Структурная формула метилацетата
H O H
| || |
H— C— C —O — C — H
| |
H H
8. Рассчитать стандартную энтальпию образования этилена
H H
| |
H — C = C — H
получаемого по уравнению
2C(гр) + 2H2(г)- C2H4(г); ΔH
по величинам энергии связей. Сравнить полученный результат с табличным (см. табл. 1).
9. Вычислить стандартную энтальпию образования H — бутана
H H H H
| | | |
H — C — C — C— C— H
| | | |
H H H H
по энергиям связей.
Уравнение образования бутана
4C(гр) + 5H2(г) = C4 H10; Δ H°
10. Вычислить стандартную энтальпию образования метанола по величинам энергий связи
C(гр) + 2H2 + 1/2 O2 = CH3OH; ΔH°.
Сравнить полученную величину с табличным значением (см. табл. З).
11. Рассчитайте тепловой эффект (ΔH°) дегидратации этилового спирта по уравнению реакции
H H H H
| | \ /
H — C— C — OH(ж) → C = C + H — O — H; ΔH°
| | / \
H H H H(г)
Энергии соответствующих связей взять в табл. 1, теплоты испарения спирта
и воды - в табл. 2.
12. Рассчитать тепловой эффект (ΔH°) сгорания этилацетата
H
 | O H H
| O H H
 H — C — С | |
H — C — С | |
| O — C — C — H(ж)
H | |
H H до СO2 и H2O(ж)
по энергиям разрыва связей при 298 К. (Энергию связей см. в табл. 1, теплоту испарения этилацетата и H2 O - в табл. 2).
1.2. ЗАКОН ГЕССА. РАСЧЕТ ТЕПЛОПРОИЗВОДИТЕЛЬНОСТИ ТОПЛИВА. ЗАВИСИМОСТЬ ТЕПЛОВОГО ЭФФЕКТА РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ КИРХГОФА
Пример 1. Определить при 298 К тепловой эффект (ΔH°) реакции
Al2O3(кр) + ЗSO3(г)= Al2(SO4)3(кр) ; ΔH°.
Решение. Если ΔH реакции > О - реакция эндотермическая, идет с поглощением тепла; если ΔH реакции < О - реакция экзотермическая, идет с выделением тепла. По следствию из закона Гесса имеем: тепловой эффект реакции ΔH° равен разности между суммой стандартных энтальпий (теплот) образования Δ Hообр продуктов реакции и реагентов с учетом их стехиометрических коэффициентов νj, νi ):
продукты реагенты
δη°=ς vj Δ Hообр - ς νi Δ Hообр. (1.2.1)
Из табл. 3 выпишем значения стандартных энтальпий образования:
Δ Hо298 Al2O3(кр) = -1672 кДж/моль;
Δ Hо298 SO3(г) =-395,7 кДж/моль;
Δ Hо298 A12(S04)3(кр)= -3439,0 кДж/моль.
Тепловой эффект реакции находим по (1.2.1):
Δ Hо= Δ Hо298 A12(S04)3 - Δ Hо298 Al2O3 - 3 Δ Hо298 SO3 =
= -3439,0+1672+3*395,7 = -580,8 кДж
Ответ ΔΗ° = -580,8 кДж.
Пример 2. Определить тепловой эффект ΔΗ° реакции этерификации щавелевой кислоты метиловым спиртом, протекающей по уравнению
(СООН)2+ 2СН3 ОН—> (соосн3)2 + 2Н2О,
если стандартные энтальпии сгорания (см. табл. 5)
ΔHocгop(COOН)2 = -251,8 кДж/моль;
ΔHocгop (СН3ОН) = -727,59 кДж/моль;
ΔHocгop (COOCН3)2= -168О,19 кДж/моль.
Решение. По следствию из закона Гесса имеем: тепловой эффект реакции равен разности между суммой энтальпий сгорания реагентов и суммой энтальпий сгорания конечных продуктов с учетом их стехиометрических коэффициентов:
реагенты продукты
ΔHo=Σ νi ΔHocгop - Σ νj ΔHocгop (1.2.2)
Следовательно,
ΔHo = ΔHocгop(COOН)2 + 2 ΔHocгop (СН3ОН) - 2 ΔHocгop (COOCН3)2 - 2 ΔHocгop (H2O)= - 251,8 - (2*727,59)+1680,19 = -26,79 кДж.
Энтальпия сгорания Н20 (а также CO2) равны нулю.
Ответ. ΔHo = -26,79 кДж.
Пример 3. Определить стандартную энтальпию образования (Δ Hо298 обр) этилена, если тепловой эффект реакции горения этилена равен - 1412,99 кДж/моль, а стандартные энтальпии образования (Δ Hо298 обр) CО2 и H2O(ж) равны соответственно - 394,07 и - 286,26 кДж/моль.
Решение. Горение этилена происходит по реакции
C2H4(г) + 3О2 = 2СО2(г) + 2Н2О(ж);
ΔΗ = -1412,99 кДж/моль
По следствию из закона Гесса (1.2.1):
Δ Hо =2Δ Hо298 Н2О + 2Δ Hо298 СО2 - Δ Hо298 С2Н4 - Δ Hо298 О2
Стандартные энтальпии образования простых веществ равны нулю, отсюда Δ Hо298 О2= 0. Тогда
Δ Hо298 C2H4 = 2Δ Hо298 H20 +2Δ Hо298 CO2 - Δ Hо =-(2*286,26)- (2*394,07) +1412,99 = -572,52-788,14+ +1412,99 = 52,3 кДж/моль.
Ответ. Δ Hо298 C2H4 = 52,3 кДж/моль.
Пример 4. Рассчитать теплотворную способность метана. Реакция горения метана протекает по уравнению
СН4 + 2O2 = СО2 + 2H2O;Δ Hо.
ΔHocгop метана равна -891,63 кДж/моль.
Решение. Теплотворной способностью топлива называется количество тепла, выделяющееся при сгорании одного килограмма топлива (топливо состоит из горючего и окислителя).
По формуле (1.2.2) имеем
ΔΗ°= ΔHocгop CH4 + ΔHocгop O2 - ΔHocгop CO2 - ΔHocгop H2O;
ΔHocгop для O2, Н2O и СO2 равны нулю,
Поэтому ΔΗ0= ΔHocгop CH4 = -891,632 кДж/моль. Это количество тепла выделяется при сгорании 80 г топлива (вес 1-го моля метана и 2-х молей кислорода). Следовательно, теплотворная способность метана
Т.С. = (891,632/80)*1000=1114,54кДж/кг
Ответ. т.С. метана равна 1114,54 кДж/кг.
Пример 5. Определить тепловой эффект реакции
CH3OH(г) + 3/2O2=CO2(г) + 2H2O(г) при 500К и 1013 гПа
Решение. Зависимость теплового эффекта реакции от температуры выражается уравнением Кирхгофа (если в данном процессе отсутствуют фазовые превращения)
ΔΗΤ = ΔΗ0Т0 + 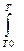 ΔС°р dT, (1.2.3)
ΔС°р dT, (1.2.3)
где ΔС°р -разность сумм молярных изобарных теплоемкостей продуктов реакций и реагентов с учетом их стехиометрических коэффициентов. Приняв, что ΔС°р не зависит от температуры в данном температурном интервале(T0 до T), уравнение (1.2.3) запишем в виде
ΔΗт= ΔΗ0Т0 + ΔС°р (Т-Т0). (1.2.4)
Для решения этого уравнения необходимо знать тепловой эффект реакции при какой-либо температуре Т0. Удобно воспользоваться тепловым эффектом, вычисленным по закону Гесса- при Т0=298 К. Стандартные энтальпии образования компонентов берем из табл. 3. По формуле (1.2.1)
Δ Hо298= Δ Hо298 CO2 + 2Δ Hо298 H2O - Δ Hо298 CH3OH(г) -3/2 Δ Hо298 O2=
= -394-(2*241,8)-(-201,2)-0=-676,4 кДж.
Далее находим ΔС°рпо табличным значениям Ср (табл.4):
ΔС°р= С°р CO2 + 2 С°рH2O - С°рCH3OH -3/2 ΔС°рO2=
37,13+2.33ι56-43,9-3/2·(29,36)=16>31 Дж/моль*К =
= 16,31·10-3 кДж/моль*К, отсюда по формуле (1.2.4)
δΗ°500 = -676,4+16,31·10-3(500-298) = -676,4 + 3,29 = -673,11 кДж.
Ответ. δΗ°500 = -673,11 кДж.
Задачи
13. Вычислить тепловой эффект реакции дегидрирования этана
2С2Н6→ 2СН4 + C2H2+H2.
Расчет произвести по стандартным энтальпиям сгорания компонентов табл. 5 и по стандартным энтальпиям образования табл. 3. Ответы сравнить.
14. Опpедeлить теплоту cгopания фocфopиcтогo водорода
2PH3 + 4O2 = P2 O5 +3H2O(ж); ΔНo.
Cтандapтныe энтальпии образования компонентов взять в табл. 3.
15. Опpедeлить тепловой эффект peaкции:
Fe3O4 + CО = 3FeO + CO2; ΔHo.
16. При cοединении 2,1 г железа c ceρой выдeлилocь
3,77 кДж. Pаccчитать cтандаpтнyю энтальпию oбpазoвания сульфида железа.
17. Найти кoличecтво теплоты, выделяющейся при взрыве
8,4 л гpeмучeгo газа, взятого при ноpмaльныx ycлoвияx.
18. Определить cтандаρтнyю энтальпию (Δ Hо298) обpазoвания
РH3, иcxoдя из ypавнения
2PH3(г)+4O2(г)=P2О5(кр) + 5H2O(ж); ΔHо=-2398 кДж
19. Cpавнить Δ Hо298 peакций воccтановления оксида железа (III) различными вoccтановителями при 298 K:
а) Fe2O3(кр)+2H2(г)=2Fe(кр) + 3H2O(г);
б) Fe2O3(кр)+3C(гр)=2Fe(кр) + 3СО(г);
в) Fe2O3(кр)+3CO(г)=2Fe(кр) + 3СО2(г).
20. Bычиcлить Δ Hо298 обpaзования MgCO3(кр) при 298 K, пользуясь cледyющими данными:
C(гр)+O2(г) = CO2 (г) ; Δ Hо298 = -394 кДж;
2Mg+O2 = 2MgO(кp); ΔHo298 = -1203,6 кДж;
MgO(кр) + CO2 (г)=MgCO3(кр); ΔHo298 = -117,6 кДж.
2. Bычиcлить Δ H298 pеaкций:
а) 2Li(кр)+2H2O(ж)=2Li+(водн) + 2OH-(водн) + H2(г);
б) 2Na(кр)+ 2H2O(ж)=2Nа+(водн) + 2OH-(водн) + H2(г).
Cтандаpтные энтальпии обpазοвания Li+(водн), Na+(водн) и OH-(водн) принять cooтвeтcтвeннo paвными - 278,5: -239 и 228,9 кДж/моль.
22. Bычиcлить, какое кoличеcтвo тепла выделяeтcя при протекающих в opганизмe pеакциях пpевpaщения глюкозы:
а) C6 H12 O6 (кр) =2 C2 H5 OH( ж) + 2 CO2 (г); Δ H о1
б) C6H12O6(кр)+6O2(г)=6СO2(г) + 6H2O(ж); ΔHо2.
Какая из этих реакций πocтавляeт оpганизмy больше энергии?
23. Cтандаpтная теплота oбpазoвания жидкого бензола при
298 K paвнa 82,9 кДж/моль. Haпишитe ypaвнение peaкции, к
котopой отноcитcя этот тепловой эффект.
24. Сколько тепла выдeлитcя при вoccтанoвлeнии 8г окиси
меди водородом c oбpазoванием жидкой воды?
25. Реакция oбpазoвания xлopиcтoгo водоpодa из xлоpа и
водорода выpажаeтcя ypавнeниeм:
H2+Cl2=2HCl; Δ H°= -184,6 кДж.
Cкoлькo тепла выдeлитcя при coeдинeнии 1 литра xлopа c
водородом?
26. Oпpeдeлить тeплотвоpнyю cпоcобноcть этилена. Реакция
гоpeния этилена выpажаeтcя уравнением:
С2H4+3O2=2CO2+2H2O.
27. Определить теплотвоpнyю cпocoбнocть этана. Реакция
горения этана:
C2H6 +3,5O2 =2CO2+3H2O.
28. Рассчитать тeплoтвopнyю cпоcобноcть ацетилена. Реакция горения ацетилена:
C2H2+ 2,5O2=2CO2+H2O.
29. Οпpeдeлить тепловой эффект реакции:
CH4+2О2 =CO2+2H2О(г) при Т=700 K.
30. Οпpеделить тепловой эффект реакции:
4NH3+5O2=4NO+6H2O(г) пpи Т= 500 K.
31. Οпpeдeлить тепловой эффект peакции:
2CO+O2=2CO2 при 800 K.
32. Οпpeдeлить тепловой эффект реакции:
2SO2 + O2 =2SO3 при 400 K.
ЗЗ. Οпредeлить тепловой эффект реакции oбpазoвания хлориcтoгo водopoда из xлopа и вoдopoдa при 800 K.
34. Реакция получения водяного газа H2+CO идет по уравнению
C(гр)+H2O(г)=CO(г)+H2(г); ΔHo.
Вычислите тепловой эффект ΔHo реакции. Найдите, сколько поглощается тепла при образовании 1000 л водяного газа (н.у.).
35. Исходя из ΔHo298 образования H2O(г) (-241,8 кДж/моль)
и следующих данных:
FeO(кр)+ CO(г)= Fe(кр)+ CO2(г); Δ Hо298 =-18,2 кДж
2CO(г) + O2 (г)= 2CO2(г); Δ Hо298 = -566,0 кДж.
вычислить Δ Hо298 реакции
FeO(кр)+H2(г)=Fe(кр)+H2O(г).
36. Найти массу метана, при полном сгорании которой с образованием жидкой воды выделяется теплота, достаточная для нагревания 100 г воды от 293 K до 303 K. Мольную теплоемкость воды принять равной 75,3 Дж/моль*К.
37. Рассчитайте тепловой эффект ΔHo реакции
2Cl2 + 2H2O=4HCl + O2,
протекающей при 798 K, считая, что теплоемкости вcex веществ - участников реакции - в интервале 298 - 798K остаются постоянными.
38. Укажите, как изменится (увеличится, уменьшится или останется неизменным тепловой эффект реакции СО +2Н2= СН3ОН(г) при изменении температуры от 298 K до 1ООО K при
P=const.
1.3. ВТОРОЙ 3AKОH ТЕРМОДИНАМИКИ. ЭНТРОПИЯ.
ЭНЕРГИИ ГИББСА И ГЕЛЬМГОЛЬЦА. КРИТЕРИЙ
САМОПРОИ3ВОЛЬНОГО ПРОТЕКАНИЯ ПРОЦЕССА
Пример 1. Один моль кислорода расширяется до десятикратного увеличения объема и одновременно охлаждается от 400К до 300К. Чему равно изменение энтропии, если для заданного
температурного интервала мольная изобарная теплоемкость кислорода C = 29,2 Дж/моль*К (Ср считаем в данном интервале температур постоянной).
Решение. Общее изменение энтропии ΔS будет складываться из изменения энтропии газа ΔS1 при его расширении и изменения энтропии газа ΔS2 при изменении температуры:
ΔS1= R ln  , (1.3.1)
, (1.3.1)
где R - газовая постоянная; V1 и V2 — соответственно конечный и начальный объемы газа..Находим по формуле (1.3.1)
ΔS1= 8,31*ln10=19,1 Дж/моль*K.
ΔS2 =Cp*ln  , (1.3.2)
, (1.3.2)
где С - мольная изобарная теплоемкость О2; Т2 и Т1 — конечная и начальная температуры.
Отсюда
ΔS2 = 29,2·1n  = -8,05 Дж/моль*К, тогда ΔS = ΔS1+ΔS2= 19,1-8,05 = 11,05 Дж/моль*К.
= -8,05 Дж/моль*К, тогда ΔS = ΔS1+ΔS2= 19,1-8,05 = 11,05 Дж/моль*К.
Ответ. ΔS = 11,05 Дж/моль*К.
Пример 2. При охлаждении 12 л кислорода от 473 до 233 K одновременно повышается давление от 105 до 6·106. Рассчитать изменение энтропии, если мольная изобарная теплоемкость кислорода Ср = 29,2 Дж/моль*К (газ считать идеальным).
Решение. Рассчитаем число молей кислорода из уравнения состояния идеального газа
pV= nRT; n=  =(105*12*10-3)/(8,31*473)= 0,3052 моля.
=(105*12*10-3)/(8,31*473)= 0,3052 моля.
Общее изменение энтропии ΔS будет складываться из изменения энтропии ΔS1 при увеличении давления и изменения энтропии Δ S2 при охлаждении газа
ΔS1 =R ln  , (1.З.З)
, (1.З.З)
где Ρ1 и Ρ2 — исходное и конечное давления; R — газовая постоянная.
ΔS2 находим по формуле (1.3.2).
Отсюда
ΔS = R ln  + Cpln
+ Cpln  .
.
Так как у нас участвует 0,3052 молей кислорода, то
ΔS =0,3052(8,31*ln(105/(6*106)) + 29,2*ln(233/437))=-16,77 Дж/моль*К.
(энтропия уменьшается при охлаждении газа).
Ответ. ΔS = —16,77 Дж/моль*К.
Пример 3. Определить изменение энтропии ΔS при нагревании 30 г ледяной уксусной кислоты (СН3 СООН) от температуры плавления до 333 K. Τпл уксусной кислоты 289,6 K. Теплота
плавления ΔΗпл= 194 Дж/г, удельная теплоемкость уксусной кислоты равна 2,19 Дж/г*К.
Решение. Общее изменение энтропии Δ S Равно сумме изменения энтропии при плавлении уксусной кислоты Δ S1 и при нагревании жидкой уксусной кислоты от Τпл до заданной температуры (333 К) Δ S2
Δ S1= Δ Hпл/Tпл (1.3.4)
1 моль СН3СООН= 60 г.
По формуле (1.3.4) находим Δ S1=194*30/289,6*60=20,1 Дж/К
Δ S2 рассчитываем по формуле (1.3.2):
Δ S2=Сpln(T2/T1)=2,19*30ln(333/289,6)=9,20 Дж/К.
Тогда
Δ S = Δ S1 + Δ S2= 20,1+9,2=29,3 Дж/К.
Ответ: Δ S = 29,3 Дж/К.
Пример 4. Определить изменение энтропии ΔSо и энергии Гиббса ΔGо при стандартных условиях для системы
Fe3О4 + CO = 3FeO + CO2
и решить вопрос о возможности самопроизвольного протекания ее при указанных условиях.
Решение. Значения ΔSо и ΔGо Для реакции определяем по следствию из закона Гесса (2.2.1). Стандартные энтропии S°298 и энергии Гиббса ΔGо 298 компонентов берем из табл.3.
Следовательно,
продукты реагенты
ΔSо = ∑ νj S°298 - ∑νi S°298.
или
ΔSо = 3Sо298 FeO + Sо298 CO2 - Sо298 Fe3O4 - Sо298 CO =3*58,79 + 213,6 -151,46 – 197,4 = 39,11Дж
продукты реагенты
ΔGо = ∑ νj ΔGо 298 - ∑νi ΔGо 298. (1.3.6)
или
ΔGо = 3 ΔGо 298 FeO + ΔGо 298 CO2 - ΔGо 298 Fe3O4 - ΔGо 298 CO = 3(-246,0) – 394,89 +1010 +137,4 = 14,51 кДж
Если ΔG < О, процесс идет самопроизвольно, при ΔG > 0 процесс не идет. В данном случае ΔG > 0, следовательно, процесс самопроизвольно не пойдет.
Ответ. ΔS° = 39,11 Дж; ΔGо = 14,51 кДж, реакция самопроизвольно не пойдет.
Пример 5. Вычислить стандартное значение изменения свободной энергии ΔGо реакции: C2H2+5/2 О2 = 2 CО2 + Н2О (ж); ΔGо,
По табличным данным -Sо298 и ΔΗо298 для компонентов (табл. 3).
Решение. Определяем тепловой эффект и изменение энтропии реакции по закону Гесса (формулы (1.2.1) и (1.3.5)).
ΔΗ° = ΔΗ°298 H2O + 2ΔΗ°298 CO2 - 2ΔΗ°298 C2H2= -285,8+2* (-394)-226,8= -1299,6 кДж/моль;
ΔS°= Sо298 H2O + 2Sо298 CO2 - Sо298 C2H2 – 5/2Sо298 O2 =
= 70+2213,6-200,8-2,5*205= -216,2 Дж/моль*К;
ΔS°= -0,2162 кДж/моль*К.
Изменение изобарно-изотермического потенциала находим по формуле
ΔG° = ΔΗ°- T ΔSо, (1.3.7)
ΔG°= -1299,6+0,2162*298= -1235,19 кДж/моль.
Таким образом, ΔGо < 0 - самопроизвольный процесс возможен.
Ответ. ΔGо =-1235,19 кДж.
Задачи
39. Определить изменение энтропии для 1 кг воздуха при нагревании его от 223 до 323 К (при этом происходит изменение давления от 106 до 105 Па). Массовая теплоемкость воздуха 1,005 Дж/г*К. Средняя молекулярная масса воздуха 29.
40. Средняя массовая теплоемкость железа равна 0,486 Дж/г* К. Определить изменение энтропии ΔS при нагревании 1 кг железа от 100 до 150оС.
41. Определить суммарное изменение энтропии при нагревании 1 моля бензола от температуры плавления (5,49 С) до полного испарения при температуре кипения (80,2оС). Теплота
плавления бензола 126,54 Дж/г, теплота парообразования 396 Дж/г, массовая теплоемкость бензола 1,94 Дж/г* К.
42. Вычислить cyммаpное изменение энтропии при нагревании 1 моля воды от темпеpатуpы плавления до полного иcпаpения пpи температypе кипения. Теплота плавления льда 335,2 Дж/г, теплота паpообpазоваиия воды 2260 Дж/г, маccовая теплоемкость воды 4,188 Дж/г*K.
43. Вычиcлить изменение энтpопии ΔS пpи cтандapтныx
уcловияx для yравнений pеакций:
2H2S+SO2=2H2O(ж)+3S(кр); Zn(кр)+H2SO4(ж) = ZnSO4(ж) + H2(г).
CH4 + 2O2 = CO2 +2H2O(r).
44. Oпpеделить изменение энеpгии Гиббcа для реакции
N2+2H2O(ж)=NH4NO2; ΔGo
и дать заключение о возможноcти ее пpотекания пpи cтандаpтных ycловиях.
45. Вычиcлить изобарно-изотeрмичecкий потеициал ΔGo реакций и дать заключение о возможноcти иx пpοтекания пpи cтандаpтныx yсловияx:
а) 3С2H2=C6H6; ΔGo1;
б) CO2+2NH3→NH2-CO-NH2 + H2O(ж); ΔG°2;
в) СH3-CH2-CH2OH→ CH3-СН=СН2 + Н2О(ж); ΔG°3.
46. Hе пpоизводя вычиcлений, ycтанοвить знак ΔS cледyющиx пpоцеcсов:
а) 2NH3(г)=N2(г)+3H2(г);
б) CO2(кр)=CO2(г);
в) 2NO(г)+O2(г)=2NO2(г);
г) 2H2S(г)+3O2(г)=2H2O(ж)+2SO2(г);
д) 2CH3OH(г)+3O2(г)=4H2O(г)+2CO2(г).
47. Опpеделить знак изменения энтpoпии для pеакций:
2A2(г)+B2(г)=2A2B(ж).
Возможно ли пpотекание этой pеакции в cтандаpтныχ ycловияx? Ответ обоcновать.
48. Установить, пpотекание какиx из нижеcледyющих pеакций возможно в cтандаpтных ycловияx пpи 298 K:
а) N2(г)+1/2O2(г) =N2O(г);
б) 4HCl(г)+ O2 (г) = 2Cl2 (г) + 2H2O(ж);
в) Fe2O3(кр)+ 3CO(г)=2Fe(кр)+ 3CO2(г).
49. Вычислить ΔG для реакции:
CаCO3(кр) = СаО(кр)+CO2(г)
при 298 К, 773 К и 1773 K. Зависимостью ΔH, ΔS от температуры пренебречь. Построить график зависимости ΔG от температуры и найти по графику температуру, выше которой указанная реакция может протекать самопроизвольно.
50. Вычислить ΔG°298 следующих реакций восстановления
оксида железа (II):
а) FeO(кр) + 1/2 C(гр) = Fe(кр) + 1/2 CО2 (г);
б)FeO(кр) + C(гр) = Fe(кр) + CO(г) ;
в) FeO(кр) + CO(г) = Fe(кр) + CO2(г).
Протекание какой из этих реакций наиболее вероятно?
51. Указать, какие из реакций образования оксидов азота,
и при каких температурах (высоких или низких) могут протекать самопроизвольно:
а) 2N 2(г) + O2 (г) = 2N2O(г); Δ Hо298>0;
б) N2(г) + O2(г) = 2NO(г) ; Δ Hо298>0;
в) 2NO(г) + O 2(г) = 2NO2(кр); Δ Hо298<0;
г) NO(г) + NO2(г) = N2 O3 (кр); Δ Hо298<0;
д) N2(г) + 2O2(г) = 2NО2(г) ; Δ Hо298>0;
52. На основании расчета ΔG°298 реакций сделайте вывод,
какие из перечисленных ниже окислов могут быть восстановлены алюминием при 298 К: CаО; FеO; СuО, PbO; Fe2O3; Cr2O3?
53. Можно ли получить пероксид водорода H2О2 по реакции:
2H2O(ж) + O2 (г) = 2N2O2(ж).
54. Возможно ли горение кальция в атмоофере оксида углерода по реакции
Са (кр) + CО(г) = CаO(кр) + C(кр).
55. Чему равно изменение энтропии Δ S при плавлении одного моля льда при 273,15 K, если изменение энтальпии при плавлении льда Δ Hпл= 6016,8 Дж/моль.
1.4. ХИМИЧЕСКОЕ РАВНОВЕСИЕ. КОНСТАНТА ХИМИЧЕСКОГО РАВНОВЕСИЯ
Пример 1. Вычислить изменение энергии Гиббса ΔG в реакции димеризации диоксида азота 2NО2(г)= N2O4(г) при стандартной температуре 298 К, 273 К и 373 К. Сделать вывод о направлении процесса. Определить константы равновесия реакции димеризации диоксида азота при выше указанных температурах. Определить температуру, при которой Δ G = 0. Сделайте вывод о направлении этой реакции выше и ниже этой температуры. Термодинамические характеристики компонентов:
ΔΗ°298 So298
В-во кДж/моль Дж/моль*K
NO2 (г) 33,3 240,2
N2O4(г) 9,6 303,8
Решение. Для обратимого процесса:
aA(г) + bB(г) ⇄ сС(г) + dD(г)
выражение для константы равновесия Kр будет
Kр =(PcC*PdD)/(PaA*PbB)
где PA, PB, PC, PD - равновесные парциальные давления газообразных компонентов А,В,С,D a, b, c, d - стехиометрические коэффициенты.
Для процесса aA(ж)+bB (ж ) ⇄ с C (ж)+dD(ж) выражение для константы равновесия
Kc = (CcC*CdD)/(CaA*CbB)
где CA, CB, CC, CD - равновесные концентрации веществ А,В,С,D a, b, c, d - стехиометрические коэффициенты.
По формуле (1.4.1) для системы 2NO2⇄ N2O4 имеем
Kр =PN2O4/P2NO2
При стандартной температуре 298 K изменение энтальпии (ΔHo реакции) определим по формуле (1.2.2)
ΔHo реакции = ΔΗ°298 N2O4 - 2ΔΗ°298 NO2 = 9,6-2*33,5 = -57400 Дж.
Изменение энтропии (1.3.5)
ΔSo реакции = S°298 N2O4 - 2S°298 NO2 =303,8-2* (240,2)=-176 Дж/моль*К
Пользуясь принципом Ле-Шателье, который говорит о том, что при изменении условий, при которых обратимая реакция находится в состоянии равновесия, равновесие сместится в сторонy процесса ослабевающего изменения, предскажем направление смещения равновесия. Значение ΔΗо отрицательно, следовательно реакция образования экзотермическая (идет c выделением тепла) и при понижении температуры равновесие должно смещаться вправо, при повышении температуры - влево. Кроме того, по фopмyлe (1.3.6), зная, что ΔH<O; ΔS < 0 мы можем сделать заключение о том, что Δ G < 0 будет при низких температypax; Δ G < 0 характеризует возможность самопроизвольного процесса; Δ G > 0 характеризует невозможность самопроизвольного процесса (см. пример 4 разд. 1.3). Следовательно, в нашем случае при понижении температуры будет предпочтительнее образование N2О4 (равновесие смещается вправо), а при увеличении температуры предпочтительнее образование NO2 (равновесие смещается влево). Качественные выводы подтвердим расчетами
ΔGo273; ΔGo298; ΔGo373 и K273; K298; K373
Значение энергии Гиббса для заданных температур рассчитаем по формуле (1.3.7):
ΔGo298=ΔHo-TΔSo=-57400-298*(-176)=-4952Дж.,
ΔGo273=-57400-273*(-176)=-9352Дж:
ΔGo373=-57400-373*(-176)= 7129 Дж.
Отрицательное значение ΔGo298 говорит о смещении равновесия реакции вправо, а более высокое отрицательное значение ΔGo273 свидетельствует о том, что при снижении температуры от (298 до 273 К) равновесие смещается вправо.
Положительное значение ΔGo373 указывает на изменение направления самопроизвольного процесса. При этой температуре предпочтительнее становится обратная реакция (смещение равновесия влево).
Константы равновесия Кp и энергию Гиббса ΔGo связывает формула
ΔGo=-RTlnKp
где Кp — константа равновесия процесса; R - газовая постоянная; T - абсолютная температура. По формуле (1.4.3) имеем:
lnK273=- ΔGo273/RT=9352/8,31*273=4,12
K273= 61
lnK298= -ΔGo298/RT=4952/8,31*298=2
K298=7,3
lnK373= -ΔGo373/RT=-7129/8,31*298=-2,3
K373=0,1
значение К298 и K273 > 1 показывает на смещение равновесия вправо (сравни с (1.4.1)) и тем больше, чем выше значение константы равновесия. K373 < 1, говорит ο смещении равновесия в системе влево (сравни с (1.4.1)).
Условию ΔGoреакции =0 отвечает константа равновесия,
реакции
равная единице.
Рассчитаем температуру Т, соответствующую этой константе по формуле (1.3.7):
ΔG°=ΔΗ°-TΔSo; O=ΔHo-TΔSo;
TΔG=0 =ΔΗ°/ΔS°=57400/176=326,19 K
Вывод. При температуре 326,19 K прямая и обратная реакции протекают c одинаковой вероятностью, Kр=1. С понижением температуры равновесие будет смещаться вправо с повышением влево.
Пример 2. Константа равновесия Кр реакции синтеза NH3 по реакции N 2+3 H2==2NH3 при 623 K равна 2,32*10-13. Вычислить Кс при той же температуре.
Решение. Связь Кр и Кс осуществляется по формуле
K p= Kc (RT)Δn, (1.4.4)
Δn= n2- n1 =2-4= -2, где n1и n2 количество молей peaгентов и продуктов. Следовательно,
Kc=Kp/(RT)Δn=0,624*10-5
Ответ. К = 0,624*10-5.
Пример 2. Упругость диссоциации карбоната кальция при 1154 К равна 80380 Па, а при 1164 K - 91177 Па. Рассчитать, при какой температуре упругость диссоциации карбоната кальция будет равна 101325 Па.
Решение. Реакция диссоциации CaCO3(кр) ⇄ CaO(кр)+СО2(г)
Отсюда по (1.4.1)
Kp=PCO2
Следовательно, при каждой температуре (Т1 - 1154 K; Τ =1164 К* Τ = X) константы равновесия будут соответствовать давлению:
KT1 = 80380; KT2 = 91177; K T3 = 101325.
Зависимость константы равновесия от температуры показывает уравнение Аррениуса
dlnKp/dT= ΔΗ/RT2 (1.4.5)
где Кp - константа равновесия; Τ - температура, К; ΔΗ - тепловой эффект реакции; R - газовая постоянная.
Интегрируя уравнение (1.4.5) в интервале температур Т1-Т2 при Δ H= соnst получим
lnKT1/KT2= ΔΗ/R(1/T1-1/T2),
Где KT1 и KT2 – константы равновесия при T1 и T2.
Определим сначала ΔΗ (по 1.4.6)
ΔΗ=ln(91177*8,31*1154*1164/80380*10)=140500 Дж/моль.
Далее определяем T3
ln(101325/91177)=140500/8,31(1/1164-1/T3)
T3=1172 K
Ответ. При Т=1172К упругость диссоциации карбоната кальция будет равна 101325 Па.
Задачи
56. Константа диссоциации уксусной кислоты при 298 К равна 1,75*10-5. Чему равно изменение энергии Гиббса диссоциации уксусной кислоты?
57. Найти значение энергии Гиббса (ΔGo298) и константы равновесия K298 для реакции BaSО4(кр) → Ba2+(р) + SО2-4(p).
Для расчета использовать следующие данные:
Вещество Sо298 Дж/моль*К ΔHo 298кДж/моль 2^ 2^
BaSO4(кр) 132,4 -1447,39
Ba2+(р) 9,64 -533,83
SO2-4 (р) 18,44 -904,2.
58. Найти константу равновесия при 473 К для реакции гидратации этилена
С2Н4(г) + H2O(г)=С2Н5ОН(г).
Свойства реагентов взять в табл. 3. Зависимостью ΔS и ΔH от температуры пренебречь.
59. Считая, что ΔHo 298 и ΔSо298 реакции 4HCl+O2 ⇄ 2Н2О + 2Сl2 не зависят от температуры, найти температуру, при которой
Кр =1, а ΔGo = О.
60. Пользуясь табличными данными, вычислить константы равновесия следующих реакций при 298 К и при 1000 К:
а) Н2О(г) + СО ⇄ СО2 + Н2
б) СО2 + С(гр) ⇄ 2СО;
c) N2 + 3H2 ⇄ 2NH3.
Изменениями ΔHoи Sоот температуры пренебречь.
61. Для некоторой самопроизвольно протекающей реакции Δ S < О. Как будет изменяться константа равновесия с повышением температуры: а) увеличиваться, б) уменьшаться, в) по данным задачи нельзя определить.
62. Не пользуясь вычислениями, установить знак ΔSo следующих процессов:
а) 2NH3(г) ⇄ N2(г) + H2(г) ;
б) CO2(кр) ⇄ CO2(г);
в) 2NO(г) + O2(г) = 2NO2(г);
г) 2Н2S(г) + 3O2 = 2H2O(ж) + 2SO2(г);
д) 2СН3ОН(г) + 3О2(г) = 4H2O(г) + 2СО2(г).
63. В каком из следующих случаев реакция возможна при любых температурах: а) ΔН°< 0, ΔS°> 0; б) Δ Н°<0, ΔS°<0; в) Δ Н°>0, ΔS°> 0?
64. В каком из следующих случаев реак