ОБЩИЕ ПОНЯТИЯ О РАСТВОРАХ
Основные понятия
Растворы имеют важное значение в жизни и практической деятельности человека. Так, процессы усвоения пищи человеком и животными связаны с переводом питательных веществ в раствор. Растворами являются все важнейшие физиологические жидкости (кровь, лимфа и т.д.) Производства, в основе которых лежат химические процессы, обычно связаны с использованием растворов.
Растворы – это многокомпонентные системы, состоящие из 2 и более компонентов, составные количества которого могут меняться в широких пределах. Компонент, который находится в большем количестве называется растворителем, в меньшем - растворенным веществом.
Системы, образующиеся в результате распределения одного вещества в состоянии тонкого измельчения (диспергирования) в другом, представляющем непрерывную фазу, называются дисперсными.
Процесс измельчения и равномерного распределения вещества в газообразной, жидкой или твердой средах, называется диспергированием.
Сплошная непрерывная фаза называется дисперсионной средой или растворителем.
Раздробленные частицы, находящиеся в дисперсионной среде, называются дисперсной фазой или растворенным веществом.
Растворы классифицируют по размерам частиц дисперсной фазы (грубодисперсные, предельно-высокодисперсные и истинные растворы) и по агрегатному состоянию дисперсной фазы и дисперсионной среды.
Классификация дисперсных систем по степени раздробленности
частиц дисперсной фазы
| Системы | Раздробленность вещества | Поперечник частиц, м | Число атомов в одной частице |
| Грубодисперсные - взвеси наиболее неустойчивые растворы, они расслаиваются, частицы растворенного вещества можно увидеть не только в микроскоп, но и не вооруженным взглядом и можно отделить отстаиванием или фильтрованием | Макроскопи-ческая | 10-2 - 10-4 | ›1018 |
| Микроскопи-ческая | 10-4 - 10-7 (т.е. > 100 нм) | ›109 | |
| Предельно-высокодисперсные или коллоидные (золи) Растворы могут быть как малоустойчивыми, так и долго сохраняться во времени. Они однородны, но через некоторое время осаждаются. При нагревании или добавлении кислот, щелочей, солей коагулируют(свертываются). | Коллоидная | 10-7 - 10-9 (т.е. 1-100 нм) | 109 - 103 |
| Истинные растворы Растворы гомогенны, устойчивы, не отслаиваются, свойства их сохраняются во времени. Частицы растворенного вещества можно выделить выпариванием или перегонкой | Молекулярная и ионная | 10-9 - 10-10 (т.е. < 1 нм) | ‹ 103 |
В зависимости от того, одинаковы или нет размеры частиц, различают соответственно монодисперсные и полидисперсные системы. Подавляющее большинство реальных систем полидисперсны.
Классификация дисперсных систем по агрегатным состояниям
дисперсной фазы и дисперсионной среды
| Дисперсионная среда (растворитель) | Дисперсная фаза (растворенное вещество) | ||
| Твердая | Жидкая | Газообразная | |
| Твердая | твердые сплавы (рубиновое стекло - это силикатное стекло, в котором находятся частички золота размером 4-30 мкм) | твердые эмульсии (жемчуг, где в твердом карбонате кальция диспергирована вода) | твердые пены (пенобетоны, пенопласт, пемза, хлеб и т.п.) |
| Жидкая | суспензии или взвеси (грубодисперсные системы твердых частиц в жидкостях, например, глина, песок, известь в воде) и коллоидные растворы (тонкодисперсные системы твердых частиц в жидкостях, например, желатин, канц. клей, молоко). | эмульсии (дисперсная фаза жидкость раздроблена в другой, не растворяющей ее жидкости, например, нефть и нефтепродукты, масло, жир в воде) | газовые эмульсии, пены (кислород, углекислый газ растворены в воде) |
| Газообразная | дым, пыль - аэрозоли с твердой дисперсной фазой (пыль образуются при измельчении твердых веществ, а дым - при конденсации твердых веществ из газовой фазы). | туманы — аэрозоли с жидкой дисперсной фазой | Пример - воздух |
Дисперсные системы характеризуются следующими свойствами:
1) Степень дисперсности – количественная характеристика дисперсности вещества: D = 1/ l,
где l – либо диаметр сферических частиц, либо – длина ребра кубических частиц, либо толщина пленок.
2) Агрегативная устойчивость – способность раздробленных систем сохранять присущую им степень дисперсности.
3) Седиментация – свободное оседание частиц под действием силы тяжести.
4) Сорбция – процесс поглощения одного вещества (сорбтив) другим (сорбент), независимо от механизма поглощения. Поглощение газов, паров и растворенных веществ поверхностью других веществ, называется адсорбцией. Поглощение одного вещества другим, происходящее во всем объеме, называется абсорбцией. Поглощение одного вещества другим, сопровождающееся химическими реакциями, называется хемосорбцией. Удаление адсорбированных веществ с адсорбентов называется десорбцией.
5) Коагуляция – соединение частиц в более крупные агрегаты.
Наиболее важными и часто встречаемыми являются жидкие растворы.
Большинство веществ, находящихся в кристаллическом состоянии, растворяются в жидкостях с поглощением теплоты, т.к. при растворении кристаллов происходит разрушение их кристаллической решетки, что требует затраты энергии. Однако при растворении многих веществ происходит заметное повышение температуры, что указывает на взаимодействие между растворителем и растворенным веществом, при котором выделяется в виде теплоты больше энергии, чем ее расходуется на разрушение кристаллической решетки. Процесс взаимодействия молекул растворенного вещества с молекулами растворителя называется сольватацией, а если растворителем является вода, то гидратацией. При этом образуются соединения – сольваты, частный случай – гидраты. Предположение о существовании в водных растворах гидратов высказано и обосновано Д. И. Менделеевым, который считал, что растворение – это не только физический процесс, но и химический. (Аррениус же был основоположником физической теории растворов, согласно которой раствор уподоблялся газовой смеси, где растворитель и растворенное вещество не меняют своей природы). Подтверждением химизма процесса растворения является тот факт, что многие вещества выделяются из водных растворов в виде кристаллов, содержащих так называемую кристаллизационную воду, причем на каждую молекулу растворенного вещества приходится определенное число молекул воды. Вещества, в кристаллы которых входят молекулы воды, называются кристаллогидратами. Пример. Таким образом, при растворении вещества, подвергающегося гидратации, общий тепловой эффект складывается из теплового эффекта разрушения кристаллической решетки твердого растворяемого вещества (эндотермический процесс) и теплового эффекта гидратации (экзотермический эффект). Поэтому тепловой эффект процесса растворения может быть как «+», так и «–».
(Растворение кристалла в жидкости происходит следующим образом: когда вносят кристалл в жидкость, в которой он может растворяться, от поверхности его отрываются отдельные молекулы, которые благодаря диффузии равномерно распределяются по всему объему растворителя. Одновременно идет обратный процесс – кристаллизация. Перешедшие в раствор молекулы, ударяясь о поверхность еще нерастворившегося вещества, снова притягиваются к нему и входят в состав его кристаллов.)
При растворении твердого кристаллического вещества в воде идут два противоположных процесса – растворение и кристаллизация, которые сопровождаются определенными скоростями (υр и υкр).
Система, в которой скорость растворения (υр) больше скорости кристаллизации (υкр) называется ненасыщенной.
Система, в которой скорость растворения (υр) равна скорости кристаллизации (υкр) называется насыщенной.
Система, в которой скорость растворения (υр) меньше скорости кристаллизации (υкр) называется пересыщенной. Такую систему можно создать, если производить охлаждение насыщенного раствора осторожно и медленно, в противном случае избыток растворенного вещества выделится в осадок.
Насыщенные и пересыщенные растворы применяются сравнительно редко. Чаще используют ненасыщенные растворы. Растворы с низким содержанием растворенного вещества называются разбавленными, с высоким - концентрированными.
Содержание растворенного вещества в определенной массе (определенном объеме) раствора или растворителя называется концентрацией.
Рассмотрим различные способы выражения концентраций:
1. Число граммов растворенного вещества, содержащихся в 100 г раствора, называется массовой долей (ω) растворенного вещества.
ω = 100⋅m р.в/m р-ра, m р-ра = Vρ, ω = 100⋅ m р.в/Vρ (%).
2. Мольная доля (N) – отношение количества растворенного вещества (ν1) к суммарному количеству всех компонентов раствора, то есть ν1 + ν2 (где ν2 –количество растворителя)
N = ν1/(ν1 + ν2).
3. Число молей растворенного вещества, содержащихся в 1 дм3 раствора, называется молярной концентрацией (с) или молярностью (моль/дм³, М).
c = 1000 mр.в./MV.
4. Число эквивалентов растворенного вещества, содержащихся в 1 дм3
раствора, называется эквивалентной концентрацией (cн) или нормальностью (моль/дм³, н).
cн = 1000 mр.в/MэV.
5. Масса растворенного вещества, содержащаяся в 1 см³ раствора, называется титром (Т, г/см3).
Т = mр.в/V.
6. Число молей растворенного вещества, содержащихся в 1000 г растворителя, называется моляльной концентрацией (cm) или моляльностью (моль/кг, m).
cm = 1000 mр.в/Mmр-ля.
Способность вещества растворяться в том или ином растворителе называется растворимостью. Количественно растворимость вещества часто выражается массой вещества, растворяющегося в 100 г растворителя.
Растворимость веществ в воде
| Растворимость, г в 100 г растворителя | Характеристика вещества | Пример |
| Более 10 | Хорошо растворимое | Нитрат калия |
| 10 - 1 | Растворимое | Хлорид натрия |
| Меньше 1 | Малорастворимое | Сульфат кальция |
| Меньше 0,01 | Практически нерастворимое | Иодид серебра |
Растворимость для различных веществ колеблется в значительных пределах и зависит от их природы, взаимодействия частиц растворенного вещества между собой и с молекулами растворителя, а также от внешних условий (давления, температуры и т. д.). Так как большинство твёрдых веществ при растворении в воде поглощают энергию, то в соответствии с принципом Ле-Шателье, растворимость многих твёрдых веществ увеличивается с повышением температуры.
Осмос. Осмотическое давление
Пусть имеется сосуд, разделенный полупроницаемой перегородкой (пунктир на рисунке) на две части, заполненные до одинакового уровня О-О. В левой части помещается растворитель, в правой - раствор.
 |
 К понятию явления осмоса
К понятию явления осмоса
Вследствие различия концентраций растворителя по обе стороны перегородки, растворитель самопроизвольно (в соответствии с принципом Ле-Шателье) проникает через полупроницаемую перегородку в раствор, разбавляя его. При разбавлении раствора за счёт самопроизвольной диффузии растворителя объём раствора увеличивается, и уровень перемещается из положения О в положение II. Односторонняя диффузия определенного сорта частиц в растворе через полупроницаемую перегородку называется осмосом.
Количественно охарактеризовать осмотические свойства раствора можно по осмотическому давлению - это мера стремления растворителя к переходу сквозь полупроницаемую перегородку в данный раствор. Растворы, характеризующиеся одинаковым осмотическим давлением, называются изотоническими.
Вант-Гофф показал, что осмотическое давление в растворе неэлектролита пропорционально молярной концентрации растворенного вещества
Росм= сRТ,
где Росм - осмотическое давление, кПа; с - молярная концентрация, моль/дм3; R - газовая постоянная, равная 8,314 Дж/моль∙К; Т - температура, К
Рассмотрим разбавленный раствор нелетучего (твёрдого) вещества А в летучем жидком растворителе В. При этом общее давление насыщенного пара над раствором определяется парциальным давлением пара растворителя, поскольку давлением пара растворённого вещества можно пренебречь.
Франсуа Мари Рауль (1830-1901) показал, что давление насыщенного пара растворителя над раствором Р меньше, чем над чистым растворителем Р°.
Разность Р° - Р = DР называется абсолютным понижением давления пара над раствором. Эта величина, отнесенная к давлению пара чистого растворителя, то есть (Р°-Р)/Р° =DР/Р°, называется относительным понижением давления пара.
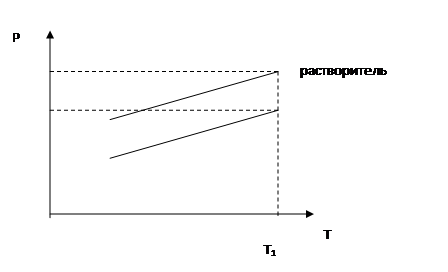 |
Зависимость давления насыщенного пара растворителя
над чистым растворителем и над раствором
Согласно закону Рауля, относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворённого нелетучего вещества
(Р° - Р)/Р° = N
где N = νA/(νа + νВ); N - мольная доля растворенного вещества; ν A - число молей растворённого вещества; νВ - число молей растворителя.
Следствие закона Рауля. Понижение давления пара растворителя над раствором нелетучего вещества по сравнению с чистым растворителем (Н2О), можно пояснить с привлечением принципа смещения равновесия Ле-Шателье. Действительно, при увеличении концентрации нелетучего компонента в растворе равновесие в системе вода - насыщенный пар сдвигается в сторону конденсации части пара (реакция системы на уменьшение концентрации воды при растворении вещества), что и вызывает уменьшение давления пара.
Понижение давления пара растворителя над раствором по сравнению с чистым растворителем вызывает повышение температуры кипения и понижение температуры замерзания растворов по сравнению с чистым растворителем (Dt). Эти величины пропорциональны моляльной концентрации растворенного вещества - неэлектролита, то есть
Dt = К∙сm = К∙1000 mр.в/Mmр-ля,
где сm- моляльная концентрация раствора. Коэффициент пропорциональности К, в случае повышения температуры кипения, называется эбуллиоскопической константой для данного растворителя (Кэб), а для понижения температуры замерзания - криоскопической константой (К кр). Эти константы различны для одного и того же растворителя.