Лабораторная работа №7
Получение чугуна и стали. Закалка и отпуск стали. Распознавание руд железа
Цель: Ознакомится с процессами производства чугуна и стали спомощью флеш -анимации; изучить химические процессы производства, сырьё, продукты, виды чугуна, виды сталей; научиться выполнять расчеты, связанные с получением металлов.
youtube.com ›watch?v=-jG7wNTVl6Y
Краткие теоретические сведения
Железо в химически чистом виде - блестящий серебристо-белый вязкий и ковкий металл, имеющий плотность 7,8 г/см3 и температуру плавления 1539±1°С. Образует сплавы со многими элементами. Наиболее распространенными являются железоуглеродистые сплавы (чугун, стали), играющие ведущую роль в современной технике.
Среднее содержание железа в земной коре - 5,0 %, оно является одним из наиболее распространенных элементов и входит в состав большого числа минералов (более 300). Главные промышленно-ценные минералы железа - оксиды.
Железная руда - природное минеральное сырьё, содержащее соединения железа, применяемое для получения сплавов на основе железа.
Рудная часть железной руды обычно представлена минералами на основе оксидов железа. Пустая порода железной руды состоит из кварца и песчаников с примесями глины. Перед металлургической плавкой железную руду специально подготавливают с целью снижения содержания пустой породы в ней.
  Железная руда Железная руда
|
| Пустая порода |
| Рудная часть |
Таблица 5 – содержание железа
| Руда | Рудный минерал | Содержание железа % |
| Красный железняк | Гематит - Fe2O3 | 50 - 60 |
| Магнитный железняк | Магнетит - Fе3O4 | 55 - 75 |
| Бурый железняк | Лимонит - 2Fe2О3· пH2О | 40 - 50 |
| Шпатовый железняк | Сидерит - FeCO3 | 30 - 40 |
Чугун- сплав железа с углеродом (1,7-5%) и металлургическими примесями (Mn, Si, P и др)
Серый чугун получают при медленном охлаждении металла при литье изделий, а также при повышенном содержании кремния, углерода. Обозначается он буквами СЧ Применяется для производства слабонагруженных деталей, работающих в легких условиях. Например, корпуса редукторов, насосов, электродвигателей, различные крышки, отопительные батареи и т.п.
Ковкий чугун получают из белого чугуна путем специального отжига. Это длительная термическая обработка, при которой белый чугун медленно нагревается, после определенной выдержки медленно охлаждается. Приt°950-1000 таком отжиге происходит графитизация цементита белого чугуна с образованием хлопьевидных включений графита. Обозначается ковкий чугун буквами КЧ. Применяется этот чугун для изготовления деталей, работающих в более тяжелых условиях по сравнению с деталями из серого чугуна ‑ например, картеры редукторов, коробок передач автомобилей, кронштейны рессор, различные крюки, фланцы и т.п.
Высокопрочный чугун получают путем модифицирования его при выплавке магнием или церием в количестве 0,05 %. Модификаторы способствуют формированию шаровидных включений графита. Обозначаются высокопрочные чугуны буквами ВЧ и в Применяется высокопрочный чугун для изготовления ответственных деталей, работающих в довольно сложных условиях. Например, коленчатые и распределительные валы легковых автомобилей, прокатные валки, корпуса турбин, детали кузнечно-прессового оборудования и др.
Для выплавки чугуна в доменных печах используют: руду: магнитный железняк (Fe3O4); красный железняк (Fe2O3), бурый железняк (гидраты оксидов железа 2Fe2O3 * 3H2O и Fe2O3 * H2O) и др.
· Топливо: кокс, но возможна частичная замена газом, мазутом.
· Флюсы: известняк CaCO3, доломитизированный известняк(CaCO3 + MgCO3)
|
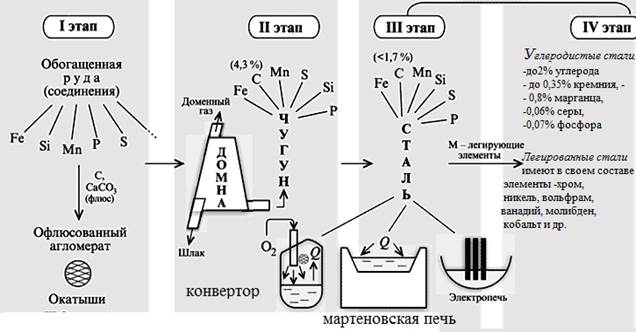
1.ТЕХНОЛОГИЧЕСКИЙ ПРОЦЕСС Подготовка руды - дробление и сортировка, обогащение руды (промывка, магнитная сепарация), агломерация. Для агломерации шихту, состоящую из железной руды (40…50 %), известняка (15…20 %), кокса (4…6 %), влаги (6…9 %), спекают при температуре 1300…1500 0С., образуются окатыши.
2.Доменный процесс. А гломерат направляют в доменную печь, где при температуре1000…1100 0C. восстановленное из руды твердое железо, взаимодействуя с оксидом углерода, коксом и сажистым углеродом, интенсивно растворяет углерод. Капли железоуглеродистого сплава, протекая по кускам кокса, дополнительно насыщаются углеродом (до4%), марганцем, кремнием, фосфором которые при температуре 12000 C восстанавливаются из руды, и серой, содержащейся в коксе. В нижней части доменной печи образуется шлак в результате сплавления окислов пустой породы руды, флюсов и золы топлива. Сливают чугун каждые 3…4 часа, шлак -1,5-2 часа. Шлаки содержат Al2O3, CaO, MgO, SiO2, MnO, FeO, CaS. Чугун отправляют на производство стали или формуют (литьем) в виде чушек-слитков массой 45 кг.
3.Сталь – сплав железа с углеродом (до 1,7%) и металлургическими примесями Mn, Сr, Si,Ni. Основными исходными материалами являются передельный чугун и стальной лом (скрап). Способы получения стали:
4. Конверторный способ основан на продувке сжатым воздухом расплавленного чугуна. Мартеновский способ вызван к жизни необходимостью перерабатывать стальной лом
Плавка стали в электропечах дает возможность получать высококачественные стали.
По химическому составу стали делят на углеродистые и легированные.
Углеродистые стали, кроме углерода, содержат до 0,35% кремния, 0,8% марганца, 0,06% серы, 0,07% фосфора. Различают мало-, средне- и высокоуглеродистые стали.
Легированные стали имеют в своем составе легирующие элементы (хром, никель, вольфрам, ванадий, молибден, кобальт и др.) для сообщения стали требуемых свойств.
Нержавеющей сталью называется сталь, обладающая стойкостью против атмосферной коррозии. Это обеспечивается введением легирующих элементов хрома и меди.
По назначению делятся на конструкционные, инструментальные и стали с особыми физ.свойствами.
По способу выплавки различают сталь обыкновенного качества, качественную и высококачественную.
Закалка — распространенный процесс термической обработки стальных деталей. Она осуществляется путем нагрева деталей,выдержки при этой температуре и быстрого охлаждения. Основная цель закалки стали — получение высокой твердости, износостойкости и физико-механических свойств.
Отпуск заключается в нагреве закаленной заготовки до определенной температуры и последующем охлаждении ее на воздухе, в воде, масле или других охлаждающих средах. Отпуск уменьшает хрупкость, повышает вязкость, улучшает обрабатываемость резанием.
Теоретические основы:
Чугун — сплав на основе железа, содержащий от 2 до 4,5% углерода, а также марганец, кремний, фосфор и серу. Чугун значительно тверже железа, обычно он очень хрупкий, не куется, а при ударе разбивается. Этот сплав применяется для изготовления различных массивных деталей методом литья, так называемый литейный чугун и для переработки в сталь — передельный чугун.
В зависимости от состояния углерода в сплаве различают серый и белый чугун.
Белые чугуны образуются при быстром охлаждении. В своей структуре они содержат большое количество цементита, обладающего высокой твердостью, прочностью, хрупкостью и имеющего белый цвет, чем и обусловлен цвет и название белых чугунов. Из-за большого количества цементита в своей структуре белые чугуны обладают высокой твердостью, износостойкостью, хрупкостью и поддаются обработке резанием только сверхтвердыми сплавами.

Серые чугуны образуются только при малых скоростях охлаждения в узком интервале температур, когда мала степень переохлаждения жидкой фазы. В этих условиях весь углерод или его большая часть графитизируется в виде пластинчатого графита, а содержание углерода в виде цементита составляет не более 0,8 %. Графитизация чугуна и ее полнота зависит от скорости охлаждения, химического состава и наличия центров графитизации.

| Вид | Состав | Свойства | Применение |
| Серый чугун | Содержит 1,7—4,3% С, 1,25—4,0% $i и до 1,5% Мп. Из-за большого содержания кремния снижается растворимость углерода, поэтому углерод находится в свободном состоянии в виде графита | Сравнительно мягкий и поддающийся механичеcкой обработке материал. Свобод- ный углерод придает чугуну вязкость | Производство литых деталей (шестерни, колеса, трубы и т. д.) |
| Белый чугун | Содержит 1,7—4,3% С, более 4% Мп, но очень мало кремния. Углерод в основном содержится в виде цементита — карбида железа Fе3С | Твердый и хрупкий материал. Эти свойства придает цементит, который обладает большой твердостью | Переработка в сталь |
Сталь — сплав на основе железа, содержащий менее 2% углерода. По химическому составу стали разделяют на два основных вида: углеродистая и легированная.
Углеродистая сталь представляет собой сплав железа главным образом с углеродом, но, в отличие от чугуна, содержание в ней углерода, а также Мп, Si, Р и S гораздо меньше. В зависимости от количества углерода стали подразделяют на мягкие (содержание углерода не превышает 0,3%), средней твердости (углерода несколько больше, чем в мягких) и твердые (углерода может быть до 2%). Из мягкой и средней твердости стали делают детали машин, трубы, болты, гвозди, скрепки, а из твердой — различные инструменты.
Легированная сталь — это тоже сплав железа с углеродом, только в него введены еще специальные, легирующие добавки: хром, никель, вольфрам, молибден, ванадий и др.
Легирующие добавки придают сплаву особые качества. Так, хромоникелевые стали очень пластичные, прочные, жаростойкие, кислотоупорные, устойчивые против коррозии (ржавления). Они применяются в строительстве (например, облицовка колонн станции «Маяковская» московского метро выполнена из хромоникелевой стали), а также для изготовления нержавеющих предметов домашнего обихода (ножей, вилок, ложек), всевозможных медицинских и других инструментов. Хромомолибденовые и хромованадиевые стали очень твердые, прочные и жаростойкие. Они используются для изготовления трубопроводов, компрессоров, двигателей и многих других деталей машин современной техники.
Хромовольфрамовые стали сохраняют большую твердость при очень высоких температурах. Они служат конструкционным материалом для быстрорежущих инструментов.
Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д.
Всвободном виде встречаются металлы, расположенные в ряду напряжений правее водорода (Аg, Нg, Рt, Аu, Сu), хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений.
Металлы встречаются в природе как в свободном состоянии (самородные металлы), так и, главным образом, в виде химических соединений.
В виде самородных металлов находятся наименее активные металлы. Типичными их представителями являются золото и платина. Серебро, медь, ртуть, олово могут находиться в природе как в самородном состоянии, так и в виде соединений, все остальные металлы (стоящие в ряду стандартных электродных потенциалов до олова) — только в виде соединений с другими элементами.
Минералы и горные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно,называют рудами.
Минералы и горные породы, содержащие металлы или их соединения и пригодные для промышленного получения металлов, называются рудами.
Важнейшими рудами металлов являются их оксиды и соли (сульфиды, карбонаты и др.). Если руды содержат соединения двух или нескольких металлов, то они называются полиметаллическимирудами(например, медноцинковые, свицово-серебряные и др.).
Получение металлов из руд — задача металлургии.