Аминокислоты, преимущественно α-аминокислоты, необходимы для синтеза белков в живых организмах. Нужные для этого аминокислоты человек и животные получают в виде пищи, содержащей различные белки. Последние подвергаются в пищеварительном тракте расщеплению на отдельные аминокислоты, из которых затем синтезируются белки, свойственные данному организму. Некоторые аминокислоты применяются в медицинских целях. Многие аминокислоты служат для подкормки животных.
Производные аминокислот используются для синтеза волокна, например капрона.
Вопросы для самоконтроля
· Написать электронное строение азота и водорода.
· Написать электронную и структурную формулу аммиака.
· Что такое углеводородный радикал?
· Какие вы знаете углеводородные радикалы?
· Замените в молекуле аммиака один водород на метильный радикал.
· Как вы считаете, что это за соединение и как оно называется?
· Какое вещество получится, если заменить остальные атомы водорода на углеводородные радикалы, например, метильные?
· Как изменятся свойства полученных соединений?
· Определите формулу органического вещества, если известно, что плотность его паров по водороду равна 22,5, массовая доля углерода – 0,533,массовая доля водорода – 0,156 и массовая доля азота – 0,311. (Ответ: С2Н7N.)
· Учебник Г.Е.Рудзитис, Ф.Г.Фельдман. Страница 173, № 6, 7.
ü Что такое кислота?
ü Что такое функциональная группа?
ü Какие вы помните функциональные группы?
ü Что такое аминогруппа?
ü Какими свойствами обладает аминогруппа?
ü Какими свойствами обладает кислота?
ü Как вы считаете, какую реакцию среды будет давать молекула, содержащая кислотную и основную группу?
ü ТЕСТ
1 вариант.
1) В состав аминокислот входят функциональные группы:
а) -NH2 и –ОН
б) -NH2 и –СОН
в) -NH2 и –СООН
г) -ОH и –СООН
2. Аминокислоты можно рассматривать как производные:
а) алкенов;
б) спиртов;
в) карбоновых кислот;
г) углеводов.
3. Аминокислоты вступают в реакцию
а) полимеризацию;
б) поликондесацию;
в) нейтрализацию.
4.Связь между аминокислотами в полимере:
а) водородная;
б) ионная;
в) пептидная.
5. Незаменимые аминокислоты - это …
2 вариант.
1.Общая формула аминокислот:
а)R-СН2 (NH2)-СООН;
б) R-СООН;
в) R-СОН;
г) R-ОН.
2. В растворе аминокислот среда
а) щелочная;
б) нейтральная;
в) кислотная.
3. Аминокислоты могут взаимодействовать друг с другом при этом образуя:
а) углеводы;
б) нуклеиновые кислоты;
в) полипептиды;
г)крахмал.
4. Аминокислоты – это...
а) органические основания;
б) кислоты
в) органические амфотерные соединения.
5. Аминокислоты применяют в …
ü Из каких неорганических веществ можно получить аминоуксусную кислоту? Напишите соответствующие уравнения реакций.
ü Задача. Определите формулу аминокислоты, если массовые доли углерода, водорода, кислорода и азота соответственно равны: 48%, 9,34%, 42,67% и 18, 67%. Напишите все возможные структурные формулы и назовите их.
ПЛАН ЗАНЯТИЯ № 16
Дисциплина: Химия.
Тема: Белки.
Цель занятия: Изучить первичную, вторичную, третичную структуры белков. Химические свойства белков: горение, денатурация, гидролиз, цветные реакции. Биологические функции белков.
Планируемые результаты
Предметные: сформированность представлений о месте химии в современной научной картине мира; понимание роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач;
Метапредметные: использование различных видов познавательной деятельности и основных интеллектуальных операций (постановки задачи, формулирования гипотез, анализа и синтеза, сравнения, обобщения, систематизации, выявления причинно-следственных связей, поиска аналогов, формулирования выводов) для решения поставленной задачи;
Личностные: чувство гордости и уважения к истории и достижениям отечественной химической науки; химически грамотное поведение в профессиональной деятельности и в быту при обращении с химическими веществами, материалами и процессами;
Норма времени: 2 часа
Вид занятия: Лекция.
План занятия:
1. Белки. Первичная, вторичная, третичная структуры белков.
2. Химические свойства белков: горение, денатурация, гидролиз, цветные реакции.
3. Биологические функции белков.
Оснащение: Учебник.
Литература:
1. Химия 10 класс: учеб. для общеобразоват. организаций с прил. на электрон. Носителе (DVD) / Г.Е. Рудзитис, Ф.Г. Фельдман. – М.:Просвещение, 2014. -208 с.: ил.
2. Химия для профессий и специальностей технического профиля: учебник для студ. учреждений сред. проф. образования / О.С.Габриелян, И.Г. Остроумов. – 5 - изд., стер. – М.: Издательский центр «Академия», 2017. – 272с., с цв. ил.
Преподаватель: Тубальцева Ю.Н.
Тема 16. БЕЛКИ.
План:
1. Белки. Первичная, вторичная, третичная структуры белков.
2. Химические свойства белков: горение, денатурация, гидролиз, цветные реакции.
3. Биологические функции белков.
1) Белки. Первичная, вторичная, третичная структуры белков.
1 – Состав белка: С – 54%, О – 23%, Н – 7%, N – 17%, S – 2% и другие: Zn, P, Fe, Cu, Mg, Mn
В 1903 г. немецкий ученый Э.Г.Фишер предложил пептидную теорию, которая стала ключом к тайне строения белка. Фишер предположил, что белки представляют собой полимеры из остатков аминокислот, соединенных пептидной связью NH–CO. Идея о том, что белки – это полимерные образования, высказывалась еще в 1888 г. русским ученым А.Я.Данилевским.
 2 - Белки – ВМС – протеины
2 - Белки – ВМС – протеины
“Протос” от греческого – “первичный, важнейший”. Белки – природные полимеры, состоящие из АК.
Mr (альбумина)=36000
Mr (миозина)=150000
Mr (гемоглобина)=68000
Mr (коллагена)=350000
Mr (фибриногена)=450000
Формула белка молока – казеина C1894H3021O576N468S21
Белки – это природные высокомолекулярные природные соединения (биополимеры), построенные из альфа-аминокислот, соединенных особой пептидной связью. В состав белков входит 20 различных аминокислот, отсюда следует огромное многообразие белков при различных комбинациях аминокислот. Как из 33 букв алфавита мы можем составить бесконечное число слов, так из 20 аминокислот – бесконечное множество белков. В организме человека насчитывается до 100 000 белков.
Число аминокислотных остатков, входящих в молекулы, различно: инсулин – 51, миоглобин – 140. Отсюда M r белка от 10 000 до нескольких миллионов.
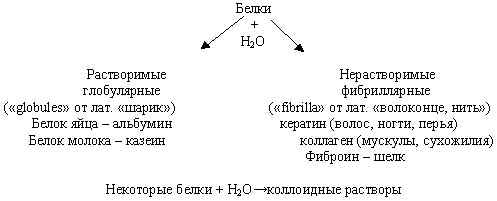
Белки подразделяют на протеины (простые белки) и протеиды (сложные белки).
3 -
4 - 20 АК – “кирпичики” белкового здания, соединяя их в разном порядке, можно выстроить неисчислимое множество веществ с самыми разными свойствами. Химики пытаются расшифровать строение белковых молекул-великанов. Задача эта очень трудная: природа тщательно прячет “чертежи”, по которым выстроены эти частицы.
В 1888 году русский биохимик А.Я. Данилевский указал на то, что в молекулах белков содержатся повторяющиеся пептидные группы атомов –С–N–
В начале ХХ столетия немецкому ученому Э.Фишеру и другим исследователям удалось синтезировать соединения, в молекулы, которых входило 18 остатков различных АК, соединенных пептидными связями.

 5 - Первичная структура белка – это последовательное чередование АК (полипептидная цепь ППЦ). Пространственная конфигурация белковой молекулы, напоминающая спираль образуется благодаря многочисленным водородным связям между группами.
5 - Первичная структура белка – это последовательное чередование АК (полипептидная цепь ППЦ). Пространственная конфигурация белковой молекулы, напоминающая спираль образуется благодаря многочисленным водородным связям между группами.
– СО– и –NH–
Такая структура белка называется вторичной. В пространстве закрученная спираль ППЦ образует третичную структуру белка, которая поддерживается взаимодействием разных функциональных групп ППЦ.
–S–S– (дисульфидный мостик)
–СООН и –ОН (сложноэфирный мостик)
–СООН и –NH2 (солевой мостик)
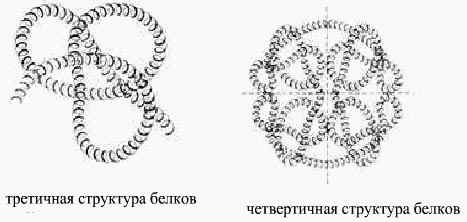 Некоторые белковые макромолекулами могут соединяться друг с другом и образовывать крупные молекулы. Полимерные образования белков называются четвертичными структурами (гемоглобин только при такой структуре способен присоединять и транспортировать О2 в организм)
Некоторые белковые макромолекулами могут соединяться друг с другом и образовывать крупные молекулы. Полимерные образования белков называются четвертичными структурами (гемоглобин только при такой структуре способен присоединять и транспортировать О2 в организм)
2) Химические свойства белков: горение, денатурация, гидролиз, цветные реакции.
1. Для белков характерны реакции, в результате которых выпадает осадок. Но в одних случаях полученный осадок при избытке воды растворяется, а в других – происходит необратимое свертывание белков, т.е. денатурация.
Денатурация – это изменение третичной и четвертичной структур белковой макромолекулы под влиянием внешних факторов (повышение или понижение температуры, давления, механического воздействия, действия химических реагентов, УФ – излучения, радиации, ядов, солей тяжелых металлов (свинец, ртуть и др.))