Механические смеси чистых компонентов (1-го рода)
Исходные данные:
• компоненты: химические элементы А и В (K=2)
• оба компонента неограниченно растворимы в жидком состоянии, а в твердом состоянии нерастворимы и не образуют химических соединений
• фазы: жидкость L, кристаллы А и В; максимальное число фаз Фmax = 3. 
8. 888 Диаграмма состояния сплавов, образующих
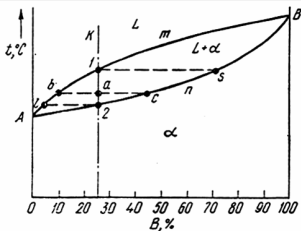
Неограниченные твердые растворы (2-го рода)
Напомним условия образования неограниченных твердых растворов:
• компоненты имеют одинаковый тип решетки (изоморфизм)
• размеры атомов компонентов отличаются не более, чем на 15 %
• компоненты имеют одинаковую валентность.
Исходные данные:
• компоненты: А, В (K = 2)
• оба компонента неограниченно растворимы в жидком и твердом состояниях и не образуют химических соединений
• фазы: жидкий сплав L, твердый раствор α.
9. 999 Диаграмма состояния сплавов, образующих
ограниченные твердые растворы и эвтектику (3-го рода)
Исходные данные:
• компоненты: А, В (K = 2)
• оба компонента неограниченно растворимы в жидком состоянии, ограничено – в твердом состоянии и не образуют химических соединений
• фазы: жидкий сплав L, ограниченные твердые растворы α = А(В) и β = В(А). 
10. 10 Диаграмма состояния четвертого типа. Она характеризует сплавы, в которых компоненты неограниченно растворимы в жидком состоянии, совершенно нерастворимы в твердом и при затвердевании образуют химические соединения.

11. 11 Желе́зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 26. Железо — типичный металл, в свободном состоянии — серебристо-белого цвета с сероватым оттенком. Чистый металл пластичен, различные примеси (в частности — углерод) повышают его твёрдость и хрупкость. Обладает ярко выраженными магнитными свойствами. Часто выделяют так называемую «триаду железа» — группу трёх металлов (железо Fe, кобальт Co, никель Ni), обладающих схожими физическими свойствами, атомными радиусами и значениями электроотрицательности.
|
|
Для железа характерен полиморфизм, он имеет четыре кристаллические модификации:
до 769 °C существует α-Fe (феррит) с объёмноцентрированной кубической решёткой и свойствами ферромагнетика (769 °C ≈ 1043 K — точка Кюри для железа)
в температурном интервале 769—917 °C существует β-Fe, который отличается от α-Fe только параметрами объёмноцентрированной кубической решётки и магнитными свойствами парамагнетика
в температурном интервале 917—1394 °C существует γ-Fe (аустенит) с гранецентрированной кубической решёткой
выше 1394 °C устойчиво δ-Fe с объёмоцентрированной кубической решёткой
1 Диаграмма Fe–C (рисунок) Аустенит – твердый раствор углерода в гамма-железе. Растворимость углерода в гамма-железе зависит от температуры. Феррит – твердый раствор углерода в альфа-железе. Растворимость углерода в феррите, как и в альфа-железе, переменная и зависит от температуры: с повышением температуры растворимость увеличивается, с понижением – падает. Цементит (карбид железа Fе3С) – химическое соединение железа с углеродом (6,67 %). Он хрупок, очень тверд. Перлит – механическая смесь феррита и цементита, содержащая 0,8 % углерода. Ледебурит – механическая смесь аустенита и цементита при температуре более
727 °С или перлита и цементита – при меньшей температуре. В ледебурите 4,3 % углерода, он очень тверд и хрупок (НВ 620 кгс/мм2, d > 50 %). Графит – свободный углерод. Механические свойства графита очень низки. Включения графита наблюдаются в чугунах.
|
|
12. 12 Рисунок
13. 13 Чугу́н — сплав железа с углеродом с содержанием более 2,14 % (точка предельной растворимости углерода в аустените на диаграмме состояний). Углерод в чугуне может содержаться в виде цементита и графита. В зависимости от формы графита и количества цементита, выделяют: белый, серый, ковкий и высокопрочные чугуны.
В белом чугуне весь углерод находится в виде цементита. Структура такого чугуна — перлит, ледебурит и цементит. Такое название этот чугун получил из-за светлого цвета излома.
Серый чугун это сплав железа, кремния (от 1,2- 3,5 %) и углерода, содержащий также постоянные примеси Mn, P, S. В структуре таких чугунов большая часть или весь углерод находится в виде графита пластинчатой формы. Излом такого чугуна из-за наличия графита имеет серый цвет.
Ковкий чугун получают длительным отжигом белого чугуна, в результате которого образуется графит хлопьевидной формы. Металлическая основа такого чугуна: феррит и реже перлит. Ковкий чугун получил свое название из-за повышенной пластичности и вязкости (хотя обработке давлением не подвергается). Ковкий чугун обладает повышенной прочностью при растяжении и высоким сопротивлением удару.
Высокопрочный чугун имеет в своей структуре шаровидный графит, который образуется в процессе кристаллизации. Шаровидный графит ослабляет металлическую основу не так сильно как пластинчатый, и не является концентратором напряжений.
|
|
В зависимости от содержания углерода серый чугун называется доэвтектическим (2,14-4,3 % углерода), эвтектическим (4,3 %) или заэвтектическим (4,3-6,67 %). Состав сплава влияет на структуру материала.
В зависимости от состояния и содержания углерода в чугуне различают: белые и серые (по цвету излома, который обуславливается структурой углерода в чугуне в виде карбида железа или свободного графита), высокопрочные с шаровидным графитом, ковкие чугуны, чугуны с вермикулярным графитом. В белом чугуне углерод присутствует в виде цементита, в сером — в основном в виде графита.
14. 14 Виды термической обработки
Среди основных видов термической обработки следует отметить:
Отжиг (гомогенизация и нормализация). Целью является получение однородной зёренной микроструктуры и растворение включений. Последующее охлаждение является медленным, препятствующим образованию неравновесных структур типа мартенсита.
Закалку проводят с повышенной скоростью охлаждения с целью получения неравновесных структур типа мартенсита. Критическая скорость охлаждения, необходимая для закалки зависит от материала.
Отпуск необходим для снятия внутренних напряжений, внесённых при закалке. Материал становится более пластичным при некотором уменьшении прочности.
Дисперсионное твердение (старение). После проведения отжига проводится нагрев на более низкую температуру с целью выделения частиц упрочняющей фазы. Иногда проводится ступенчатое старение при нескольких температурах с целью выделения нескольких видов упрочняющих частиц.
Отжиг 1-го рода — без фазовой перекристаллизации — применяется для приведения металла в более равновесное структурное состояние: снимается наклёп, понижается твёрдость, возрастают пластичность и ударная вязкость, снимаются внутренние напряжения (в связи с процессами отдыха и рекристаллизации). разновидности отжига 1-го рода: гомогенизационный, дорекриеталлизационный смягчающий, дорекристаллизационный упрочняющий, рекристаллизационный и уменьшающий напряжения отжиг.
15. 15Отжиг 2-го рода осуществляется с фазовой перекристаллизацией: сталь нагревается до температуры выше критических точек, затем следует выдержка различной продолжительности и последующее сравнительно медленное охлаждение.
Отжиг II рода: полный неполный изотермический сфероидизирующий светлый Нормализация
16. 16 Зака́лка — вид термической обработки материалов (металлы, их сплавы, стекло), заключающийся в их нагреве выше критической температуры (температуры изменения типа кристаллической решетки, т. е. полиморфного превращения, либо температуры, при которой в матрице растворяются фазы, существующие при низкой температуре), с последующим быстрым охлаждением.
Чаще всего охлаждение осущестляется в воде или масле, но существуют и другие способы охлаждения: в псевдокипящем слое твёрдого теплоносителя, струёй сжатого воздуха, водяным туманом, в жидкую полимерную закалочную среду. Различают закалку с полиморфным превращением, для сталей, и закалку без полиморфного превращения, для большинства цветных металлов.
Материал, подвергшийся закалке приобретает бо́льшую твердость, но становится хрупким, менее пластичным и вязким, если сделать большее количество повторов нагревание-охлаждение. Для снижения хрупкости и увеличения пластичности и вязкости, после закалки с полиморфным превращением применяют отпуск. После закалки без полиморфного превращения применяют старение. При отпуске имеет место некоторое снижение твердости и прочности материала.
Способы закалки
Закалка в одном охладителе — нагретую до определённых температур деталь погружают в закалочную жидкость, где она остаётся до полного охлаждения. Этот способ применяется при закалке несложных деталей из углеродистых и легированных сталей.
Прерывистая закалка в двух средах — этот способ применяют при закалке высокоуглеродистых сталей. Деталь сначала быстро охлаждают в быстро охлаждающей среде (например воде), а затем в медленно охлаждающей (масло).
Струйчатая закалка заключается в обрызгивании детали интенсивной струёй воды и обычно её применяют тогда, когда нужно закалить часть детали. При этом способе не образуется паровая рубашка, что обеспечивает более глубокую прокаливаемость, чем простая закалка в воде. Такая закалка обычно производится в индукторах на установках ТВЧ.
Ступенчатая закалка — закалка, при которой деталь охлаждается в закалочной среде, имеющей температуру выше мартенситной точки для данной стали. При охлаждении и выдержке в этой среде закаливаемая деталь должна приобрести во всех точках сечения температуру закалочной ванны. Затем следует окончательное, обычно медленное, охлаждение, во время которого и происходит закалка, то есть превращение аустенита в мартенсит.
Изотермическая закалка. В отличие от ступенчатой при изотермической закалке необходимо выдерживать сталь в закалочной среде столько времени, чтобы успело закончиться изотермическое превращение аустенита.
17. 17Отпуском называют термическую операцию, заключающуюся в нагреве закалённой стали до температур, не превышающих точку Аc1 (т.е. не выше линии PSK), выдержке и последующем охлаждении чаще всего на воздухе. Отпуск является окончательной операцией термической обработки, в результате которой сталь получает требуемые механические свойства. Кроме того, отпуск частично или полностью устраняет внутренние напряжения, возникшие при закалке.
Низкий (низкотемпературный отпуск) проводят при температурах не выше 250...300°С.
Средний (средне-температурный) отпуск выполняют при температурах 350...500°С
Высокий(высокотемпературный) отпуск проводят при 500...600°С.
18. 18 Химико-термическая обработка (ХТО) - нагрев и выдержка металлических (а в ряде случаев и неметаллических) материалов при высоких температурах в химически активных средах (твердых, жидких, газообразных).
В подавляющем большинстве случаев химико-термическую обработку проводят с целью обогащения поверхностных слоев изделий определенными элементами. Их называют, насыщающими элементами или компонентами насыщения.В результате ХТО формируется диффузионный слой, т.е. изменяется химический состав, фазовый состав, структура и свойства поверхностных слоев. Изменение химического состава обуславливает изменения структуры и свойств диффузионного слоя.
В зависимости от насыщающего элемента различают следующие процессы химико-термической обработки:
однокомпонентные: цементация - насыщение углеродом; азотирование - насыщение азотом; алитирование - насыщение алюминием; хромирование - насыщение хромом; борирование - насыщение бором; силицирование - насыщение кремнием;
многокомпонентные: нитроцементация (цианирование, карбонитрация) - насыщение азотом и углеродом; боро- и хромоалитирование - насыщение, бором или хромом и алюминием, соответственно; хромосилицирование – насыщение хромом и кремнием и т.д.
19. 19 Азотирование стали — насыщение поверхности стальных деталей азотом для повышения твердости, износоустойчивости и коррозионной стойкости. Для азотирования нагревают детали при 480—650°С в атмосфере диссоциированого аммиака, при этом образуется атомарный азот, который поглощается поверхностью стальных деталей с образованием твердого раствора азота в матрице металла, нитридов железа и нитридов легирующих элементов.
20. 20 Нитроцементация сталей — процесс насыщения поверхности стали одновременно углеродом и азотом при 700—950 °C в газовой среде, состоящей из науглероживающего газа и аммиака. Наиболее часто нитроцементация проводится при 850—870 °С. После нитроцементации следует закалка в масло с повторного нагрева или непосредственно из нитроцементационной печи с температуры насыщения или небольшого подстуживания. Для уменьшения деформации рекомендуется применять ступенчатую закалку с выдержкой в горячем масле 180—200 °С.
По сравнению с цементацией нитроцементация имеет ряд существенных преимуществ. При легировании аустенита азотом снижается температура α ↔ γ-превращения, что позволяет вести процесс насыщения при более низких температурах. Одновременно в присутствии азота резко возрастает диффузионная подвижность углерода в аустените (табл. 1). С повышением температуры эффект ускорения уменьшается
21. 21???
22. 22???
23. 23 Алюми́ний — элемент главной подгруппы третьей группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 13.
Физические свойства
Микроструктура алюминия на протравленной поверхности слитка, чистотой 99,9998 %, размер видимого сектора около 55×37 мм
Металл серебристо-белого цвета, лёгкий
плотность — 2,7 г/см³
температура плавления у технического алюминия — 658 °C, у алюминия высокой чистоты — 660 °C
удельная теплота плавления — 390 кДж/кг
температура кипения — 2500 °C
удельная теплота испарения — 10,53 МДж/кг
временное сопротивление литого алюминия — 10-12 кг/мм², деформируемого — 18-25 кг/мм², сплавов — 38-42 кг/мм²
Твёрдость по Бринеллю — 24…32 кгс/мм²
высокая пластичность: у технического — 35 %, у чистого — 50 %, прокатывается в тонкий лист и даже фольгу
Модуль Юнга — 70 ГПа
Алюминий обладает высокой электропроводностью (37·106 См/м) и теплопроводностью (203,5 Вт/(м·К)), 65 % от электропроводности меди, обладает высокой светоотражательной способностью.
Слабый парамагнетик.
Температурный коэффициент линейного расширения 24,58·10−6 К−1 (20…200 °C).
Температурный коэффициент электрического сопротивления 2,7·10−8K−1.
Алюминий образует сплавы почти со всеми металлами. Наиболее известны сплавы с медью и магнием (дюралюминий) и кремнием (силумин).
Дюралюми́ний — торговая марка одного из первых упрочняемых старением алюминиевых сплавов. Основными легирующими элементами являются медь (4,5 % массы), магний (1,6 %) и марганец (0,7 %). Типовое значение предела текучести составляет 450 МПа, однако зависит от состава и термообработки.
Силуми́н — сплав алюминия с кремнием. Химический состав — 4-22 % Si, основа — Al, незначительное количество примесей Fe, Cu, Mn, Ca, Ti, Zn, и некоторых других. Некоторые силумины модифицируются добавками натрия или лития. Добавка всего 0,05% лития или 0,1% натрия позволяет увеличить содержание кремния в эвтектическом сплаве до 14%. Сплав Al-Si (силумины) обладают наилучшими литейными свойствами.
Для литейных сплавов особенно важны литейные характеристики — высокая жидкотекучесть, малая склонность к образованию усадочных и газовых пустот, трещин, раковин.
Жаропрочные сплавы — металлические материалы, обладающие высоким сопротивлением пластической деформации и разрушению при действии высоких температур и окислительных сред.
24. 24 Медь — элемент побочной подгруппы первой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 29. Физические свойства
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет. Наряду с осмием, цезием и золотом, медь - один из четырёх металлов, имеющих явную цветовую окраску, отличную от серой или серебристой у прочих металлов. Этот цветовой оттенок объясняется наличием электронных переходов между заполненной третьей и полупустой четвертой атомными орбиталями: энергетическая разница между ними соответствует длине волны оранжевого света. Тот же механизм отвечает за характерный цвет золота.
Медь образует кубическую гранецентрированную решётку, пространственная группа F m3m, a = 0,36150 нм, Z = 4.
Медь обладает высокой тепло-[4] и электропроводностью (занимает второе место по электропроводности среди металлов после серебра). Удельная электропроводность при 20 °C 55,5-58 МСм/м[5]. Медь имеет относительно большой температурный коэффициент сопротивления: 0,4 %/°С и в широком диапазоне температур слабо зависит от температуры.
Существует ряд сплавов меди: латуни — с цинком, бронзы — с оловом и другими элементами, мельхиор — с никелем, баббиты — со свинцом и другие.
Латунь — это двойной или многокомпонентный сплав на основе меди, где основным легирующим элементом является цинк, иногда с добавлением олова, никеля, свинца, марганца, железа и других элементов.
Бро́нза — сплав меди, обычно с оловом как основным легирующим элементом, но применяются и сплавы с алюминием, кремнием, бериллием, свинцом и другими элементами, за исключением цинка и никеля. Сплавы с содержанием цинка и никеля получили название шпиатр и не являются бронзой, а являются ее более дешевой (в ценах древнего Рима) подделкой.
25. 25 Тита́н (лат. Titanium; обозначается символом Ti) — элемент побочной подгруппы четвёртой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 22.
Физические свойства Титан — легкий серебристо-белый металл. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой (a=2,951 Å; с=4,679 Å[8]; z=2; пространственная группа C6mmc), β-Ti с кубической объёмноцентрированной упаковкой (a=3,269 Å; z=2; пространственная группа Im3m), температура перехода α↔β 883 °C, ΔH перехода 3,8 кДж/моль. Точка плавления 1660±20 °C, точка кипения 3260 °C, плотность α-Ti и β-Ti соответственно равна 4,505 (20 °C) и 4,32 (900 °C) г/см³[1], атомная плотность 5,71·1022 ат/см³[источник не указан 1185 дней]. Пластичен, сваривается в инертной атмосфере. Удельное сопротивление 0,42 мкОм·м при 20 °C
Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок.
При обычной температуре покрывается защитной пассивирующей плёнкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной).
Титановая пыль имеет свойство взрываться. Температура вспышки 400 °C. Титановая стружка пожароопасна.
Анализ рынков потребления В 2005 компания Titanium Corporation опубликовала следующую оценку потребления титана в мире:
60 % — краска;
20 % — пластик;
13 % — бумага;
7 % — машиностроение.
26. 26 Цинк — элемент побочной подгруппы второй группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 30.
Физические свойства
В чистом виде — довольно пластичный серебристо-белый металл. Обладает гексагональной решеткой с параметрами а = 0,26649 нм, с = 0,49431 нм, пространственная группа P 63/mmc, Z = 2. При комнатной температуре хрупок, при сгибании пластинки слышен треск от трения кристаллитов (обычно сильнее, чем «крик олова»). При 100—150 °C цинк пластичен. Примеси, даже незначительные, резко увеличивают хрупкость цинка. Собственная концентрация носителей заряда в цинке 13,1·1028 м−3
Zamak семейство цинковых сплавов, легированных алюминием, магнием и медью, очень широко использующихся в литейном производстве. МНЦ медно-никелево-цинковый сплав.
27. 27 Материалы со специальными свойствами (стали, сплавы)
В связи с быстрым развитием приборостроения, электротехнической и электронной промышленности особую роль стали играть прецизионные сплавы, обладающие различными физическими и физико-механическими свойствами, качество которых зависит от точности химического состава, степени очистки сплава от включений и вредных примесей, структурного состояния и технологии получения. Преобладающее большинство прецизионных сплавов получают на основе следующих металлов: железа, кобальта, меди, никеля и ниобия.
Прецизионные сплавы можно разделить на три основные группы:
1. Сплавы, не изменяющие существенно своих физических и механических свойств при изменении внешних условий (механических нагрузок, вибрации, температурных, электрических и магнитных факторов). К ним относятся манганин, константан, инвар, магнитно-мягкий перминвар и др.
2. Сплавы, резко изменяющие свои свойства при воздействии на них внешних факторов: пермаллои, магнито-стрикционные материалы, пружинные сплавы и др.
3. Сплавы с заданными физико-механическими свойствами и различными их сочетаниями (например, ковар, платинит, сплавы, обладающие сверхпроводимостью и др.).
Прецизионные сплавы поставляются в виде проволоки, прутков, тонкой ленты, листов.
28. 28 Композиционные материалы — многокомпонентные материалы, состоящие из пластичной основы - матрицы, и наполнителей, играющих укрепляющую и некоторые другие роли. Между фазами (компонентами) композита имеется граница раздела фаз.
Сочетание разнородных веществ приводит к созданию нового материала, свойства которого существенно отличаются от свойств каждого из его составляющих. Т.е. признаком композиционного материала является заметное взаимное влияние составных элементов композита, т.е. их новое качество, эффект.
29. 29 Полиме́ры (греч. πολύ- — много; μέρος — часть) — неорганические и органические, аморфные и кристаллические вещества, состоящие из «мономерных звеньев», соединённых в длинные макромолекулы химическими или координационными связями. Полимер — это высокомолекулярное соединение: количество мономерных звеньев в полимере (степень полимеризации) должно быть достаточно велико. Во многих случаях количество звеньев может считаться достаточным, чтобы отнести молекулу к полимерам, если при добавлении очередного мономерного звена молекулярные свойства не изменяются.[1] Как правило, полимеры — вещества с молекулярной массой от нескольких тысяч до нескольких миллионов.
По химическому составу все полимеры подразделяются на органические, элементоорганические, неорганические.