Выше говорилось, что ЭДС обычного химического элемента приблизительно равна 1,5 В. Для увеличения ЭДС применяют батарею с последовательным соединением элементов. В этом случае “+” одного элемента соединяют с “–” другого и т. д. “Минус” первого и “плюс” последнего являются полюсами всей батареи (рис. 6.).
При последовательном соединении элементов ЭДС возрастает во столько раз, сколько соединено элементов.

Рис.6. Последовательное и параллельное соединение элементов в батарею.
Реже встречается параллельное соединение элементов, при котором положительные полюсы всех элементов соединяются вместе, образуя положительный полюс батареи, а отрицательный полюс батареи получается путем соединения отрицательных полюсов элементов (рис. 6). При параллельном соединении элементов ЭДС батареи не увеличивается, но возрастают емкость и максимальный разрядный ток. Поэтому параллельное соединение применяют, когда нужно получить больший разрядный ток и большую емкость, чем у одного элемента.
Значительно чаще прибегают к смешанному соединению, при котором увеличиваются и ЭДС, и емкость, и максимальный разрядный ток. В этом случае обычно соединяют параллельно несколько групп элементов, а в каждой группе соединяют последовательно столько элементов сколько нужно для получения необходимой ЭДС.

Рис. 7. Смешанное соединение элементов в батарею.
Число параллельных групп определяется необходимой величиной максимального разрядного тока (рис. 7). Вообще желательно составлять батареи из последовательно соединённых элементов с достаточным разрядным током. И только в случае, когда необходимо получить больший ток или увеличенную емкость, прибегают к смешанному соединению. Включение дополнительных элементов по принципу смешанного соединения применяется также для повышения напряжения, если элементы сильно разрядились.
Во время бездействия батареи параллельные группы элементов надо отсоединять друг от друга, так как за счет даже незначительной разницы в ЭДС одна группа может разряжаться на другую.
КИСЛОТНЫЕ АККУМУЛЯТОРЫ.
По сравнению с гальваническими элементами аккумулятор обладают более постоянным напряжением и могут давать большие разрядные токи. Недостатком аккумуляторов является необходимость периодического заряда их от какого-либо источника постоянного тока.
Срок службы аккумуляторов значительно выше, чем гальванических элементов. При правильном уходе аккумуляторы могут работать несколько лет и допускают до нескольких сотен циклов заряд-разряд.
Простейший кислотный (свинцовый) аккумулятор состоит из двух свинцовых пластин, опущенных в раствор серной кислоты. В таком виде он не дает никакой разности потенциалов. Чтобы в аккумуляторе возникла ЭДС, его нужно зарядить, то есть пропустить через него постоянный ток от какого-либо источника. Во время заряда в аккумуляторе происходит химическое разложение серной кислоты, причем на катоде выделяется водород, а на аноде – кислород. Последний окисляет поверхность анодной пластины, и она покрывается коричневым слоем диоксида свинца; катодная пластина остается чисто свинцовой. В результате получается элемент с двумя разнородными пластинами в растворе кислоты. Если теперь отсоединить заряжающий источник, то окажется, что аккумулятор обладает некоторой ЭДС и при включении на внешнюю цепь может дать ток.
Во время разряда аккумулятора направление тока противоположно направлению зарядного тока и химические процессы при разряде происходят в обратном порядке: на положительной пластине выделяется водород, а на отрицательной – кислород. Вследствие этого через некоторое время обе пластины становятся одинаковыми и ЭДС аккумулятора уменьшается до нуля. Если аккумулятор снова зарядить, то он опять будет давать ток, пока не разрядится.
При заряде аккумулятор накапливает энергию, а при разряде отдает ее. Само слово «аккумулятор» означает накопитель. Однако электрическая энергия накапливается в аккумуляторе не непосредственно. Энергия зарядного тока расходуется на создание новых химических веществ, а при разряде они разлагаются и почти полностью отдают энергию, затраченную на их образование. В нормальном режиме работы аккумулятор отдает около 75 % энергии, полученной при заряде.
Свинцовый аккумулятор имеет ЭДС примерно 2 В. Внутреннее сопротивление у него очень невелико, рабочее напряжение можно считать равным ЭДС. К концу заряда ЭДС аккумулятора увеличивается до 2,7 В, но при разряде сначала быстро снижается до 2 В, а затем остается почти постоянной. Лишь в конце разряда ЭДС довольно быстро уменьшается до 1,8 В. Ниже этого напряжения разряжать аккумулятор не следует.
Рассмотрим процессы, происходящие в свинцовом аккумуляторе. Свинцовые пластинки в воздухе всегда покрыты пленкой оксида свинца PbO. Под действием серной кислоты оксид свинца превращается в сернокислый свинец (сульфат свинца) PbSO4, по уравнению
PbO + Н2SO4 = PbSO4 + Н2О.
При заряде серная кислота разлагается на ионы Н2 и SO4. Отрицательные ионы SO4 подходят к аноду и превращают сульфат свинца в диокид свинца PbO2:
PbSO4 + SO2 + 2Н2О = PbO2 + 2Н2SO4.
Ионы водорода во время заряда подходят к катоду и восстанавливают на его поверхности чистый свинец:
PbSO4 + Н2 = Pb + Н2SO4.
Как видно, при заряде образуется серная кислота, то есть концентрация ее в растворе возрастает. Так как разрядный ток противоположен по направлению зарядному, то все реакции при разряде происходят в обратную сторону (написанные выше уравнения надо читать в обратном направлении). Поэтому в конце разряда пластины снова будут покрыты сульфатом свинца. Концентрация серной кислоты при разряде уменьшается.
Аккумулятор из двух свинцовых пластин мало пригоден для практического использования. Он обладает слишком небольшой емкостью и может давать ток весьма непродолжительное время, так как диоксида свинца при заряде получается мало.
Пластины современных аккумуляторов изготовляются решетчатыми (рис.8) и заполняются активной массой, состоящей из диоксида свинца для положительных пластик и губчатого (мелко раздробленного) свинца для отрицательных.
Применение пластин с активной массой значительно повышает ёмкость аккумулятора. Кроме того, для увеличения емкости в аккумуляторе устанавливают не две пластины, а большее их количество (например, пять
семь или девять). Число отрицательных пластин бывает на одну больше, чем положительных. Каждую положительную пластину размещают между двумя отрицательными (рис. 9). Поэтому поверхность пластин используется с обеих сторон; только у крайних пластин в работе участвует лишь одна поверхность. Чтобы не допустить короткого замыкания пластин, между ними помещают
пористые изоляционные прокладки-сепараторы. Сосуды аккумуляторов делаются чаще всего из кислотоупорной пластмассы.
 Рис. 8. Пластина кислотно-
го аккумулятора.
Рис. 8. Пластина кислотно-
го аккумулятора.
|
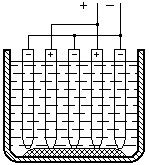 Рис. 9. Принцип устройства многопластинчатого аккуму-лятора.
Рис. 9. Принцип устройства многопластинчатого аккуму-лятора.
|
Электролит приготовляется из химически чистой серной кислоты и дистиллированной или снеговой воды. Недостаточно чистая кислота или вода, содержащая примеси, могут испортить аккумулятор. У электролита плотность должна быть 1,25 – 1,26 при температурах выше нуля и 1,30 – 1,35 при температурах ниже нуля. Если температура выше 30°, то плотность электролита снижают до 1,20 – 1,21. Для измерения плотности электролита служит ареометр, представляющий собой запаянную стеклянную трубку, в нижней части которой помещён груз, а выше расположена бумажная шкала с делениями, соответствующими различным плотностям. Чем меньше плотность раствора, тем глубже опускается ареометр в раствор. Отсчет плотности ведётся по уровню раствора.
При приготовлении электролита кислоту тонкой струёй наливают в дистиллированную воду, непрерывно размешивая раствор чистой стеклянной палочкой. Нельзя наливать воду в кислоту, так как при этом происходит сильное нагревание и даже кипение с разбрызгиванием кислоты, которая может испортить одежду и вызвать ожоги. Во время работы с кислотой необходимо иметь под руками раствор щёлочи, на пример соды. Если кислота попала на тело или одежду, этим раствором нужно сейчас же смочить место, на которое попала кислота, и тем самым нейтрализовать её. Электролит наливают в аккумулятор так, чтобы уровень его был несколько выше пластин. Плотность электролита, заливаемого в новый аккумулятор должна быть 1,12. В крышке аккумулятора сделаны отверстия для наливания электролита, закрытые пробками. В пробках имеются небольшие отверстия для выхода газов. После заливки электролита в новый аккумулятор его оставляют на шесть часов, чтобы активная масса пропиталась электролитом.
При заряде положительный полюс аккумулятора соединяется с положительным полюсом заряжающего источника, напряжение которого должно быть несколько выше, чем ЭДС аккумулятора. Для установления нужного тока применяется реостат, который включается в один из проводов, идущих к аккумулятору. Для того чтобы контролировать ток, иногда включают еще амперметр. Зарядный ток (в ампер-часах) не должен превышать  емкости аккумулятора (в ампер-часах). Например, максимальный зарядный ток для аккумулятора емкостью в 40 А·ч равен 4 А. Нормальный заряд аккумулятора обычно длится 12 часов. При большем токе аккумулятор перегревается и происходит разрушение активной массы пластин. Если заряд вести меньшим током, что вполне допустимо и даже желательно, то продолжительность заряда соответственно увеличивается. Когда заряжается новый, еще не работавший аккумулятор, то заряд осуществляют более продолжительное время, повторяя его несколько раз и разряжая аккумулятор в промежутках между такими зарядами. Правила заряда подробно указаны в инструкции, прилагаемой к аккумулятору.
емкости аккумулятора (в ампер-часах). Например, максимальный зарядный ток для аккумулятора емкостью в 40 А·ч равен 4 А. Нормальный заряд аккумулятора обычно длится 12 часов. При большем токе аккумулятор перегревается и происходит разрушение активной массы пластин. Если заряд вести меньшим током, что вполне допустимо и даже желательно, то продолжительность заряда соответственно увеличивается. Когда заряжается новый, еще не работавший аккумулятор, то заряд осуществляют более продолжительное время, повторяя его несколько раз и разряжая аккумулятор в промежутках между такими зарядами. Правила заряда подробно указаны в инструкции, прилагаемой к аккумулятору.
Когда аккумулятор совершенно разряжен, то в начале заряда его ЭДС равна 1,8 В, а в конце заряда она повышается, как известно, до 2,7 В. В конце заряда происходит бурное выделение пузырьков газа в электролите, который как бы «кипит». Если имеется вольтметр, то конец заряда можно определить и по возрастанию ЭДС аккумулятора до 2,7 В. Обычно аккумулятору дают «покипеть» час-два, после чего заряд считают оконченным.
Необходимо помнить, что из аккумулятора выделяется водород и кислород, смесь которых представляет собой так называемый гремучий газ, легко взрывающийся от искры или пламени. Поэтому к аккумулятору нельзя подносить зажженные предметы.
При разряде аккумуляторов нужно соблюдать следующие правила. Максимальный разрядный ток не должен превышать  емкости аккумулятора. Надо остерегаться короткого замыкания аккумулятора, при котором возникает очень большой ток. Он вызывает порчу аккумулятора: его пластины коробятся и из них выпадает активная масса, которая может замкнуть накоротко пластины. Нельзя пробовать аккумулятор «на искру», соединяя его полюсы накоротко.
емкости аккумулятора. Надо остерегаться короткого замыкания аккумулятора, при котором возникает очень большой ток. Он вызывает порчу аккумулятора: его пластины коробятся и из них выпадает активная масса, которая может замкнуть накоротко пластины. Нельзя пробовать аккумулятор «на искру», соединяя его полюсы накоротко.
Как только ЭДС при разряде понизится до 1,8 В, нужно не позднее чем через сутки поставить аккумулятор на заряд, иначе пластины аккумулятора покроются белым налётом сернокислого свинца (сульфата). Этот налёт сильно снижает емкость аккумулятора. Удалить сульфат с пластин очень трудно.
 Рис. 10. Внешний вид кис-лотного аккумулятора.
Рис. 10. Внешний вид кис-лотного аккумулятора.
|
Аккумулятор постепенно разряжается, даже находясь в бездействующем состоянии. Каждые сутки за счет саморазряда теряется примерно 1 % емкости. Такой саморазряд увеличивается, если в электролите и в пластинах имеются вредные примеси. Кроме того, аккумулятор может разряжаться через плохую изоляцию между своими выводами. Необходимо тщательно вытирать сосуды и следить за изоляцией между выводами. Быстрый саморазряд происходит также при коротком замыкании между пластинами аккумулятора. Чтобы не допустить полного саморазряда, необходимо аккумулятор заряжать раз в месяц, даже если он не разрядился полностью или совсем не работал. Вообще не рекомендуется оставлять на длительное время заряженный аккумулятор без работы. Лучше его разрядить, вылить кислоту и несколько раз промыть водой.
При снижении уровня электролита вследствие испарения воды нужно доливать дистиллированную воду, а не кислоту. Все выступающие наружу свинцовые выводы от пластин и зажимы следует смазывать вазелином, предварительно удаляя с них оксидный слой. Нельзя допускать загрязнения аккумулятора и попадания в него пыли. Свинцовые аккумуляторы боятся сильных сотрясений и толчков. Во время заряда из аккумулятора выделяются вредные для дыхания пары, поэтому аккумуляторы не следует заряжать в жилом помещении.
Промышленностью выпускаются кислотные аккумуляторы многих типов на различные ёмкости и батареи на различные напряжения, состоящие из нескольких аккумуляторов, соединённых последовательно. Внешний вид кислотного аккумулятора показан на рис. 10.
ЩЕЛОЧНЫЕ АККУМУЛЯТОРЫ.
По сравнению с кислотными аккумуляторами щелочные аккумуляторы обладают следующими достоинствами: они значительно легче, не боятся толчков и сотрясений, не портятся от коротких замыканий, а также от больших зарядных и разрядных токов, могут длительное время оставаться в разряженном состоянии. Но щелочные аккумуляторы дороже свинцовых и имеют меньшую ЭДС. Они отдают при разряде не более 65% энергии, полученной во время заряда. Электролитом в щелоных аккумуляторах служит раствор щелочи (едкого кали или едкого натра) с небольшой добавкой едкого лития, который несколько увеличивает ёмкость. Для этих аккумуляторов применяются железные никелированные сосуды. Пластины представляют собой железные рамки с коробочками из тонкого листового железа, имеющего много отверстий. Эти коробочки наполнены активной массой, состоящей для положительных пластин из гидрата оксида никеля и графита, а для отрицательных пластин – из кадмия и железа. Аккумуляторы с такими пластинами называются кадмиево-никелевыми. Кроме того, применяются ещё железо-никелевые аккумуляторы, у которых активная масса имеет несколько иной состав и не содержит кадмия. Свойства аккумуляторов обоих типов примерно одинаковы.
Положительные пластины обычно соединяются с сосудом аккумулятора, а отрицательные пластины изолируются от него. В каждом аккумуляторе количество положительных пластин на одну больше, чем отрицательных. На рис. 11. показан внешний вид одного из щелочных аккумуляторов.

Рис.11. Внешний вид Рис.12. Устройство герметичного