Группа№21, химия,урок№83
Тема программы: Белки.
Тема урока: Гидролиз белков. Денатурация белков.
Цель: Рассмотреть гидролиз белков и денатурацию белков.
План.
1. Гидролиз белков.
2. Денатурация белков.
Опорный конспект
Гидролиз
Пептидные связи H-N-C=O, образующие полимерную цепь белковой молекулы, в присутствии кислот или щелочей гидролизуются, при этом происходит разрыв полимерной цепи, что, в конечном итоге, может привести к исходным аминокислотам. Пептидные связи, входящие в состав?-спиралей или b-структур, более устойчивы к гидролизу и различным химическим воздействиям (по сравнению с теми же связями в одиночных цепях). Более деликатную разборку белковой молекулы на составляющие аминокислоты проводят в безводной среде с помощью гидразина H2N-NH2, при этом все аминокислотные фрагменты, кроме последнего, образуют так называемые гидразиды карбоновых кислот, содержащие фрагмент C(O)-HN-NH2 (рис.).
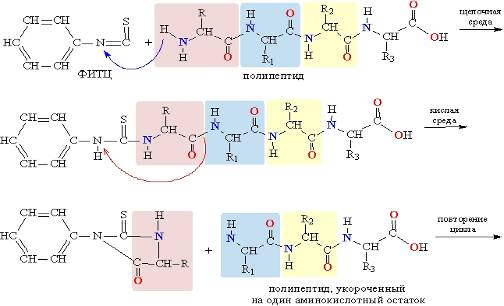
Рис.. Расщепление полипептида на составляющие аминокислоты, получаемые в форме гидразидов.
Органические группы в аминокислотах обозначены R, R1, R2 и R3. Для наглядности фрагменты различных аминокислот помещены на фоне прямоугольников с различающейся окраской
Подобный анализ может дать информацию об аминокислотном составе того или иного белка, однако важнее знать их последовательность в белковой молекуле. Одна из широко применяемых для этой цели методик - действие на полипептидную цепь фенилизотиоцианата (ФИТЦ), который в щелочной среде присоединяется к полипептиду (с того конца, который содержит аминогруппу), а при изменении реакции среды на кислую, отсоединяется от цепи, унося с собой фрагмент одной аминокислоты (рис. 13).
В щелочной среде фенилизотиоцианат (ФИТЦ) присоединяется к концу цепи, содержащему аминогруппу, атом водорода аминогруппы перемещается к азоту ФИТЦ (указано синей изогнутой стрелкой). При изменении реакции среды на кислую аминокислотный остаток отсоединяется от цепи, замыкаясь в цикл (указано красной изогнутой стрелкой) и образуя с ФИТЦ индивидуальное низкомолекулярное соединение. Его выделяют из реакционной смеси и анализируют. Затем весь цикл повторяют, отщепляя следующий аминокислотный остаток
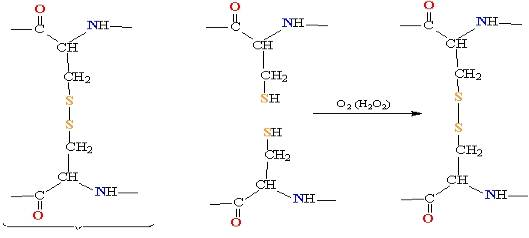
Рис. Последовательное расщепление полипептида на составляющие компоненты.
Денатурация – неполный гидролиз белка, нарушение его структуры: четвертичная структура превращается в третичную, вторичную, первичную, утрачивается биологическая активность белка.
Причинами денатурации могут быть: действие температуры, механическое воздействие (например, взбивание белка), облучение рентгеновскими лучами, химическое воздействие (действие кислот, щелочей, спирта и др.). Все эти приемы широко используют в пищевой промышленности. Денатурация облегчает усвоение белковой пищи.
Список литературы
1. Габриелян О.С. Химия. Методическое пособие. 10-11 классы. М.: «Дрофа», 2005г.
2. Еремин В.В., Кузьменко Н.Е., Тренин В.И., химия. 10 класс: учебник для общеобразовательных учреждений(базовый уровень). – М.: Дрофа, 2009г.
3. Еремин В.В., Кузьменко Н.Е.,Дроздов А.А., химия. 11 класс: учебник для общеобразовательных учреждений базовый уровень). – М.: Дрофа, 2009г.
4. Рудзитис Г.Е., Фельдман Ф.Г, химия. 10 класс: учебник для общеобразовательных учреждений (базовый уровень). – М.: Просвещение, 2005
5. Рудзитис Г.Е., Фельдман Ф.Г, химия. 11 класс: учебник для общеобразовательных учреждений (базовый уровень). – М.: Просвещение, 2005
Перечень цифровых образовательных ресурсов и Web-сайтов Интернет
1. https://school-collection.edu.ru/. - единая коллекция цифровых образовательных ресурсов:
Перечень Web-сайтов,рекомендуемых для использования в работе:
1. http//www.chem.msu.su/rus/school/ - сайт журнала «Химия: методика преподавания в школе»
2. https://www.chem.msu.su/rus/school/ - школьные учебники по химии для 8-11 классов общеобразовательной школы
3. https://c-books.narod/ru- литература по химии
4. https://experiment.edu.ru/catalog.asp- естественнонаучные эксперименты
5. chem.msu.su –портал фундаментального химического образования России
6.alhimik.ru – образовательный сайт по химии
Д.З. Изучите конспект и ответьте на вопросы: