Классификация органических реакций
Классификацию органических реакций проводят на основе общих для всех реакций признаков: строение и состав исходных и конечных продуктов; изменение степеней окисления реагирующих частиц; тепловой эффект реакции; ее обратимость и т.п.
Наиболее часто органические реакции классифицируют по следующим признакам:
· по конечному результату реакции (на основе сопоставления строения исходных и конечных продуктов);
· по минимальному числу частиц, участвующих в элементарной реакции;
· по механизму разрыва ковалентных связей в реагирующих молекулах.
Тип многостадийных реакций определяют по самой медленной (лимитирующей) стадии. Различные способы классификации часто сочетаются друг с другом.
Классификация реакций по конечному результату
В основе этой классификации лежит сопоставление числа, состава и строения исходных и конечных продуктов по уравнению реакции. В соответствии с конечным результатом различают следующие типы органических реакций:
· замещение;
· присоединение;
· отщепление (элиминирование);
· изомеризация (перегруппировка);
· разложение.
Если процесс сопровождается изменением степени окисления атома углерода в органическом соединении, то выделяют также реакции окисления и восстановления. Окисление и восстановление органических веществ может проходить по какому-либо из названных выше типов реакций.
Реакции замещения
Атом или атомная группировка в молекуле органического соединения замещается на другой атом (или атомную группировку):
АВ + С→ АС + В
Реакции этого типа можно рассматривать как реакции обмена, но в органической химии предпочтительней термин "замещение", поскольку в обмене участвует (замещается) лишь меньшая часть органической молекулы.
Примеры:
C2H6 + Cl2 (на свету)→CH3CH2Cl + HCl хлорирование этана
CH3CH2Cl + KOH (водн. р-р) → CH3CH2OH + KCl щелочной гидролиз хлорэтана
Реакции присоединения
В реакциях присоединения молекула органического соединения и молекула простого или сложного вещества соединяются в новую молекулу, при этом другие продукты реакции не образуются:
А + В→С
Примеры:
CH2=CH-CH3 + Br2 →CH2Br-CHBr-CH3 бромированиепропена
CH2=CH2 + H2O→CH3CH2OH гидратация этилена
К реакциям присоединения относятся также реакции полимеризации:
n A → An
Например, образование полиэтилена: n CH2=CH2→(-CH2-CH2-) n
Реакции отщепления
В реакции отщепления (элиминирования) происходит отрыв атомов или атомных групп от молекулы исходного вещества при сохранении ее углеродного скелета.
А→ В + С
Например:
· отщепление хлороводорода ( при действии на хлоралкан спиртовым раствором щёлочи )
CH3-CH2Cl →CH2=CH2 + HCl
· отщепление воды (при нагревании спирта с серной кислотой)
CH3-CH2OH→CH2=CH2 + H2O дегидратация этанола
· отщепление водорода от алкана (в присутствии катализатора)
CH3-CH3 →CH2=CH2 + H2 дегидрирование этана
Реакции изомеризации или перегруппировки
В органическом соединении происходит переход (миграция) отдельных атомов или групп атомов от одного участка молекулы к другому без изменения ее качественного и количественного состава:
А→В
В этом случае исходное вещество и продукт реакции являются изомерами (структурными или пространственными).
Например, в результате перегруппировки может изменяться углеродный скелет молекулы:
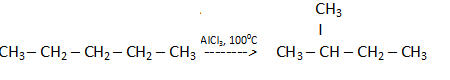
Реакции разложения
В результате реакции разложения из молекулы сложного органического вещества образуется несколько менее сложных или простых веществ:
А→ В + С +...
К этому типу реакций относится процесс крекинга – расщепление углеродного скелета крупных молекул при нагревании и в присутствии катализаторов:
CnH2n+2→ CmH2m+2 + CpH2p (n = m + p)
Например
C10H22→ C5H12 + C5H10
Реакции разложения при высокой температуре называют пиролизом, например:
СН4 → C + 2H2 пиролиз метана (1000 oC)
Реакции окисления и восстановления
Окислительно-восстановительные реакции - реакции, в ходе которых меняется степень окисления атомов, входящих в молекулу. Для органических реакций этого типа применимы те же законы, что и для неорганических. Отличием является то, что в органической химии окислительно-восстановительные процессы рассматриваются прежде всего по отношению к органическому веществу и связываются с изменением степени окисления углерода, являющегося реакционным центром молекулы. Эти реакции могут проходить по типу реакций присоединения, отщепления, замещения и т.п.
Если атом углерода в органической молекуле окисляется (отдает электроны более электроотрицательному атому), то этот процесс относят к реакциям окисления, т.к. продукт восстановления окислителя (обычно неорганическое вещество) не является конечной целью данной реакции. И наоборот, реакцией восстановления считают процесс восстановления атома углерода в органическом веществе.
Часто в органической химии ограничиваются рассмотрением реакций окисления и восстановления как реакций, связанных с потерей и приобретением атомов водорода и кислорода.
Вещество окисляется, если оно теряет атомы H и (или) приобретает атомы O. Кислородсодержащий окислитель обозначают символом [O]:

Вещество восстанавливается, если оно приобретает атомы H и (или) теряет атомы O. Восстановитель обозначают символом [H]:
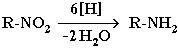
Степень окисления углерода в его соединениях изменяется в диапазоне от -4 (например, в метане CH4) до +4 (в CO2). В органических соединениях атомы углерода в одной и той же молекуле могут иметь разные степени окисления:
-3CH3--1CH2-OH