Изомеры – это соединения с одинаковым элементным составом, но имеющие различный порядок соединения атомов или различное расположение их в пространстве; изомеры отличаются своими физическими и химическими свойствами.
Различаются структурная изомерия и стереоизомерия.
Структурные изомеры – различный порядок соединения атомов.
1) изомерия положения заместителей:

2) изомерия положения кратных связей:
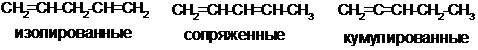
3) межклассовая изомерия:

Органические молекулы имеют пространственную трехмерную структуру, и для них возможна пространственная (стерео) изомерия.
Пространственные различия можно разделить на два типа:
1) Конформационные различия, переходящие друг в друга при повороте вокруг химической связи.
2) Конфигурационные различия: их нельзя перевести друг в друга поворотом вокруг связи, для этого необходимо разорвать связи и затем образовать новые.
КОНФОРМАЦИИ
Конформации возникают в результате вращения фрагментов вокруг химических связей и обладают малой устойчивостью, они существуют все вместе: вещество представляет собой смесь молекул в различных конформациях. В любых конформациях сохраняется конфигурационная целостность молекулы. Различные конформации отличаются по термодинамической устойчивости, относительно устойчивые конформации называются конформерами.
Ациклические молекулы
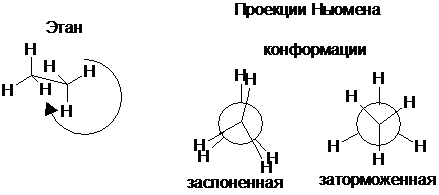
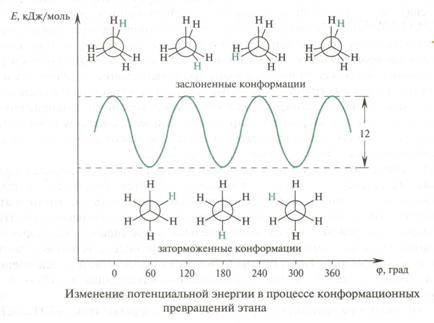

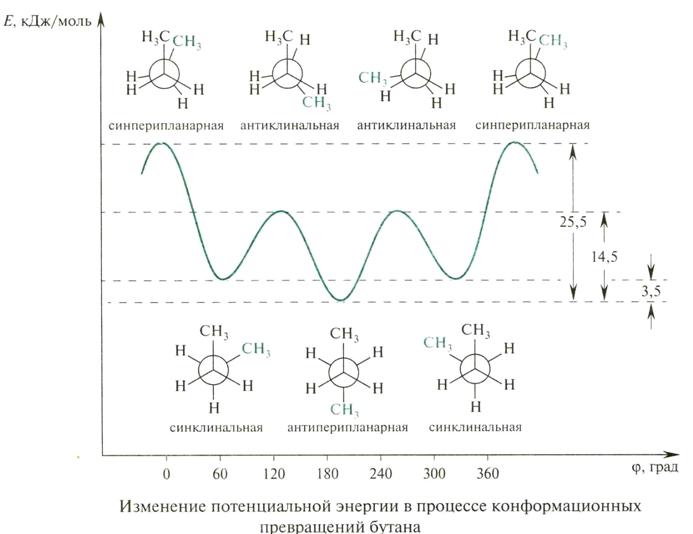
Циклы

π-Диастереомерия соединений с двойной связью

Геометрически цис- и транс-изомеры – это конформации, но устойчивые из-за невозможности свободного вращения вокруг двойной связи.
E,Z-система: Определяется старшинство заместителей попарно. Если оба старших заместителя по одну сторону – это Z-изомер (zusammen), если по разные стороны – это Е-изомер (entgegen):
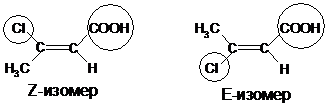
КОНФИГУРАЦИОННАЯ СТЕРЕОИЗОМЕРИЯ
Конфигурация – это порядок соединения атомов, не меняющийся при вращении фрагментов вокруг связи (в отличие от конформации).
Хиральность – это свойства несовместимости предмета с его зеркальным отражением.
Хиральные предметы: рука, буквы и др. Хиральность свойственна и некоторым молекулам:

Атом С – хиральный центр.
Признаки хиральности атома углерода: 1) sp3 гибридизация (тетрагональная геометрическая структура); 2) все четыре заместителя разные.
Отличительное свойство хиральных молекул – оптическая активность (пояснить).
Стереохимическая номенклатура
D,L-система (Розанов, 1906 г.)
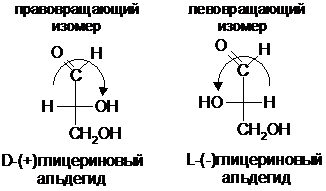
Опорное вещество (стандарт Розанова) – глицериновый альдегид. Правовращающему и левовращающему глицериновому альдегиду произвольно приписаны следующие структуры:
Для других веществ отнесение изомеров произведено путем химических превращений, не затрагивающих хиральный центр. Например, для глицериновой кислоты, полученной окислением глицеринового альдегида:

R,S-система (Канн, Ингольд, Прелог, 1951 г.)

Старшинство определяется порядковым номером элемента, связанного с хиральным центром (неподеленная пара электронов – самая младшая). Например:
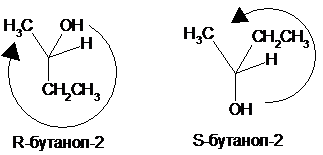
Виды стереоизомеров
Энантиомеры – это соединения, молекулы которых относятся друг к другу как предмет и несовместимое с ним его зеркальное отражение. Энантиомеры отличаются друг от друга только знаком оптической активности, все остальные физические и химические свойства их одинаковы.
Диастереомеры – это стереоизомеры, молекулы которых не относятся друг к другу как предмет и несовместимое с ним его зеркальное отражение. Физические и химические свойства диастереомеров различны. Диастереомерия наблюдается у соединений, имеющих несколько хиральных центров. Общее количество стереоизомеров у таких соединений определяется по формуле: N = n2 (N – общее количество стереоизомеров, n – количество хиральных центров).
Рацемическая смесь (рацемат) – это оптически неактивная смесь равномолярных количеств энантиомеров.
Мезосоединения – это соединения, имеющие хиральные центры, но, в целом, нехиральные и не обладающие оптической активностью.
Примеры:
D-молочная кислота и L-молочная кислота – пара энентиомеров, их равномолярная смесь – рацемат молочной кислоты.

ЛИТЕРАТУРА:
Основная
1. Белобородов В.Л., Зурабян С.Э., Лузин А.П., Тюкавкина Н.А. – Органическая химия (основной курс) – Дрофа, М., 2003 г., с.88 – 118.
Дополнительная
1. Тюкавкина Н.А., Бауков Ю.И.– Биоорганическая химия – ДРОФА, М.,
2007 г., с.47-85.
14.08.09