ОТВЕТЫ
Математический аппарат, который нужен в химии.
| 1) Умение округлять числа до тысячных, сотых, десятых и целых. (27-29 задания) |
| 2) Знание того, что такое проценты, а что такое доли и как они связаны. (27, 34 задание) |
| 3) Умение решать уравнения с одним неизвестным. (расчёт степени окисления, 34,35 задачи) |
| 4) Умение решать пропорции (28,29,34,35 задания). |
| 5) Умение решать систему уравнений с двумя неизвестными (34 задание, особенности задач 2020 года) |
Блок. Округление.
1) Округлить до тысячных число 3,14159 = 3,142
2) Округлить до тысячных число 3,14155 = 3,142
3) Округлить до тысячных число 3,14154 = 3,142
4) Округлить до сотых 6,951 = 6,95
5) Округлить до сотых 6,9545 = 6,96
6) Округлить до десятых 7,13 = 7,1
7) Округлить до десятых 7,67 = 7,7
8) Округлить до десятых 2,64 = 2,6
9) Округлить до целых 502,36 = 502
10) Округлить до целых 201,67 = 202
11) Округлить до целых 199,56 = 200
2 блок. Проценты/100% =доли
1) Дано 96,34%. Сколько это будет в долях, если нужно округлить до сотых? (0,9634=0,96)
2) На калькуляторе получилось число 0,56489756125. Напишите ответ в процентах, округлив его до сотых. (56,49%)
3) В условиях задачи дана массовая доля натрия равная 12,05%. Сколько это будет в долях? (0,1205)
3 блок. Решение уравнений с одним неизвестным.
1) Решение уравнений с одним неизвестным на примере определение степеней окисления элемента.
Правила: Вся молекула должна иметь заряд = 0(т.е. должна быть электронейтральна). Обозначаем за х – степень окисление элемента, которую нужно найти.
| Теория на примере. Нужно найти с.о. Цинка в комплексной соли состава K2[Zn(OH)4]. |
| Решение.(исходя из правил к этой части- см.выше). х – с.о. цинка. Составляем уравнение с одним неизвестным – х. Калий имеет заряд +1 (постоянный), Кислород =-2, водород=+1, не забываем учитывать индексы. Тогда получаем уравнение: (+1)*2+х+(-2)*4+(+1)*4=0 – Обязательно пишем всё с зарядами, тогда х получится сразу с нужной степенью окисления и зарядом (+ или -). !!! Если у вас возникает проблема с решением таких уравнений, то надеюсь, что после этой практики у вас останется меньше проблем, но если они будут – сразу пишите мне – не ждите мая!!! Решаем уравнение: (+1)*2+х+(-2)*4+(+1)*4=0 1. Раскрываем скобки, сохраняя знаки: +2+х-8+4=0 2. Складываем числа без х х-2=0 3.Переносим числа без х в другую сторону от равно: Х=+2 – степень окисления Цинка (да, она постоянная, но для примера нужно было разобрать =)). Дальше вам стоит отработать =) |
1) Задание - Определить с.о. выделенного элемента:
1) Сu Cl (+1)
2) Cu SO4 (+2)
3) H N O2 (+3)
4) H N O3 (+5)
5) N H3 (-3)
6) S O2 (+4)
7) P 2O5 (+5)
8) Pt 2O3 (+3)
9) H Br O (+1)
10) H Br O3 (+5)
11) H Cl O2 (+3)
12) N 2O (+1)
Решение различных уравнений с одним неизвестным.
(тренируем математический аппарат).
Задание – найти Х. (не забываем тренироваться решать на КАЛЬКУЛЯТОРЕ!)
1) 4х+20=12
4х=12-20=-8
Х=-2
2) 4(х+5)=12
4х+20=12
4х=12-20=-8
Х=-2
3) 23+15(х+3)=0
23+15х+45=0
15х=-68
Х=-4,53
4) 54=3+5у+98у
51=103у
У=0,495
5) 43у+5=25+13*(23+109у)
43у+5=25+299+1417у
43у-1417у=25+299-5
-1374у=319
У=-0,23
6) z=1258+556z (если просто написано z, то это значит что его всего ОДНА штука, если математически, то можно написать 1*z, т. е. если у нас уравнение z +z=1*z+1*z=2z (ответ 2z))
z-556z=1258
-555z=1258
Z=-2.27
7) 5(х-1)=-8x+1
5x-5=-8x+1
5x+8x=1+5
13x=6
X=0.46
8) 20-35х=841х+(-125)
20-35x=841x-125
145=876x
X=0.17
Блок 4. Умение решать пропорции.
| Теория на пример.Данное умение вам понадобится во всех задачах ЕГЭ по химии (27-29+34,35). |
| Давайте разберем парочку примеров и потом вы сами потренируетесь, если будут возникать вопросы – пишите вк. |
Задание.Пусть х – это масса неизвестной соли, которую нужно добавить в раствор (примерно задача 27, но лишённая основных условий химических, чтобы вас не пугать пока что). Нам нужно найти значение х, если у нас получилась пропорция (в 27 задачах мы составляем их сами, сейчас она будет вам дана).
Нужно найти х – массу соли.
Дана пропорция:
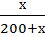 =0,35
Решение:
1. Вспоминаем, что значит «перекрёстное умножение» и перемножаем:
х=0,35*(200+х)
2. Раскрываем скобки и перемножаем
х= 0,35*200+0,35х=70+0,35х
3.Переносим числа с х в одну сторону от равно, а без х в другую:
х-0,35х=70
(Чтобы вы сразу поняла, если вдруг математика – это совсем не ваше, то х =1*х, то есть х-0,35х =х(1-0,35)- если мы вынесли х, то есть на калькуляторе считаем 1-0,35 и получаем коэффициент перед переменной х равный 0,65)
0,65х =70
3. Находим х
Х=70/0,65=107,69 – масса соли
Запоминаем сразу! - в 27-29 задаче всегда(!) указано до какого знака округлять ответ (целых, сотых, десятых и т.д.)
- в задачах 34 и 35 НЕ указано, но мы всегда округляем ДО СОТЫХ(!) =0,35
Решение:
1. Вспоминаем, что значит «перекрёстное умножение» и перемножаем:
х=0,35*(200+х)
2. Раскрываем скобки и перемножаем
х= 0,35*200+0,35х=70+0,35х
3.Переносим числа с х в одну сторону от равно, а без х в другую:
х-0,35х=70
(Чтобы вы сразу поняла, если вдруг математика – это совсем не ваше, то х =1*х, то есть х-0,35х =х(1-0,35)- если мы вынесли х, то есть на калькуляторе считаем 1-0,35 и получаем коэффициент перед переменной х равный 0,65)
0,65х =70
3. Находим х
Х=70/0,65=107,69 – масса соли
Запоминаем сразу! - в 27-29 задаче всегда(!) указано до какого знака округлять ответ (целых, сотых, десятых и т.д.)
- в задачах 34 и 35 НЕ указано, но мы всегда округляем ДО СОТЫХ(!)
|
Часто с помощью пропорций вы будете определять количество молей одного из участников реакции по уравнению реакции. Давайте рассмотрим на примере (также опущу химию, оставлю только математику).
Например, вам дано 2 моля меди, которая вступает в химическую реакцию с концентрированной серной кислотой, сколько молей кислоты израсходуется в данной реакции, если нужно использовать все 2 моля? (подвод к 29 задаче ЕГЭ по химии, потому что там тоже сначала, когда вы выучите свойства, вам нужно будет писать уравнение реакции, здесь я вам, конечно, всё напишу).
Уравнение реакции с коэффициентами
Cu +2H2SO4 (конц) = CuSO4 +SO2 +2H2O
1) Дано 2 моль Меди (Cu). Вопрос – сколько молей нужно израсходовать серной кислоты, чтобы вся медь закончилась?
2) Над веществами в уравнении пишем то, что нам известно и то, что нужно найти, внизу под веществами пишем чему равны коэффициенты в реакции:
(так как продукты нам не нужны, уравнение я вам показала просто так, чтобы вы в целом понимали, что и откуда, то дальше, то над продуктами я ничего не пишу – вставляю картинки).
 Таким образом наша пропорция выглядим вот там:
Таким образом наша пропорция выглядим вот там:
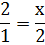 3) Решаем пропорцию «перекрёстным умножением»
2*2=1*х
4=х, то есть серной кислоты надо израсходовать 4 моль, чтобы вся медь израсходовалась. Химически коэффициент перед серной кислотой показал, что чтобы растворить всю медь серной кислоты нужно израсходовать в два раза больше.
3) Решаем пропорцию «перекрёстным умножением»
2*2=1*х
4=х, то есть серной кислоты надо израсходовать 4 моль, чтобы вся медь израсходовалась. Химически коэффициент перед серной кислотой показал, что чтобы растворить всю медь серной кислоты нужно израсходовать в два раза больше.
|
С практическим применение (Зачем я вам вообще это всё пишу) вроде бы разобрались. Пришла пора снова отработать математический аппарат.
Задание – решить пропорции и найти Х, если дана пропорция:
1) 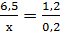
6.5*0.2=1.3=1.2x
X=1.08
2) 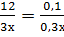
12*0.3x=0.1*3x
3.6x=0.3x
А всё уже всё, решения я то нет)
3) 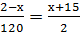
2(2-х)=120(х+15)
4-2х=120х+1800
-1796=122х
Х=-14,72
4) 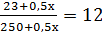
23+0,5х=12(250+0,5х)
23+0,5х=3000+6х
23-3000=6х-0,5х
-2977=5,5х
Х=-2977/5,5 = -541,27
5) 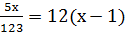
5х=123*(12х-12)
5х=1476х-1476
1476=1471х
Х=1,00
6) 12(3х-12)= 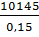
(36х-144)*0,15=10145
5,4х-72=10145
5,4х=10073
Х=10073/5,4=1865,37
ДОП.Задание. Связь Химии и математики (для желающих):
Задание – даны химические реакции и расставлены коэффициенты, нужно найти сколько молей выделенного вещества будет истрачено/получено. (По примеру составляете пропорцию и находите неизвестное).
1. CaCO3 +2HNO3 =Ca(NO3)2 +H2O +CO2
Найти количество молей CaCO3 =х, если азотной кислоты истратили 4 моль.
Решение: х/1=4/2. Решаем пропорцию: 2х=4, тогда х = 2 моль.
2. N2 +3H2 = 2NH3
Найти количество моле аммиака, который получается в ходе данной реакции, если израсходовалось 0,5 моль водорода.
Решение: 0,5/3=х/2, решаем пропорцию 2*0,5=3х, тогда 1=3х, х=1/3=0,33 моль
3. 2KOH(изб)+Al +6H2O = 2K2[Al(OH)4] +3H2
Дано 3 моль алюминия, нужно найти сколько молей:
- израсходуется КОН
Решение: х/2=3/1, тогда х=6 моль
-образуется комплексной соли – тетрагидроксоалюмината калия K2[Al(OH)4]
Решение: х/2=3/1, тогда 1*х=2*3, х=6 моль
- выделится водорода?
Решение: х/3=3/1, тогда х=3*3=9 моль
4. 2Al +6HCl =2AlCl3 +3H2
В результате реакции выделилось 0,2 моль водорода, вычислить сколько молей алюминия было израсходовано в ходе данной реакции?
Решение: 0,2/3=х/2, тогда 3*х=2*0,2=0,4, тогда молей алюминия х=0,4/3=0,13 моль
Блок 5. Умение решать системы уравнений с двумя неизвестными.
Раньше задачи №34, где встречались системы уравнений с двумя неизвестными были редкостью, но да они были, причём в одной задаче обычно составлялась одна система уравнений – решалась и дальше было всё математически проще. В 2020 году впервые появились новые задачи 34, где математика была совсем на другом уровне, например, из задач, которые я встречала и решала в августе в недрах Интернета, то там была система уравнений (иногда в ходе задачи из нужно было составить две!), причём они обычно состояли не просто из уравнения, а из пропорции (блок выше), поэтому я в этом году считаю своим долгом – помочь вам научиться решать эти системы до того как вы пойдете понимать химические сложности (химическую логику) в задачах №34.
| Теория на примере.Допустим у нас есть система уравнений вида: х+36у=120 (1) 12у+61х=2 (2) Нужно найти х и у. 1) Выражаем х из (1) уравнения (можно из любого, просто в первом уравнении х с коэффициентов = 1, поэтому ни на что ни придётся делить) Х=120-36у 2) Подставляем выраженное значение х в уравнение (2): 12у+61*(120-36у)=2 Получили уравнение с одной переменной. Решаем его и находим значение у. 12у+7320-2196у=2 12у-2196у=2-7320 -2182у=-7318 У=3,35 3) Подставляем найденное значение у в выраженное значение для х, то есть сейчас есть мини-система: Х=120-36у У=3,35 Подставляем у в х и находим значение х: Х=120-36*3,35=-0,6 Ответ: х=-0,6; у=3,35 (в математике возможно, но в химии у вас не будет отрицательных значение (!), здесь я просто наугад брала чиселки в системе уравнений) |