Тема: Первый закон термодинамики. Необратимость процессов в природе.
Закон сохранения энергии, записанный применительно к термодинамической системе, выглядит следующим образом:
Q = A / + ∆U,
где Q – количество теплоты, переданное системе;
A / - работа системы (газа);
∆U - изменение внутренней энергии системы (газа).
Первый закон термодинамики: сообщенное системе количество теплоты расходуется на совершение системой работы против внешних сил и изменение внутренней энергии системы. Если работу совершают внешние по отношению к системе тела, то работа газа считается отрицательной, работа внешних тел положительной и А = - A /
Тогда первый закон термодинамики лучше написать в виде ∆U = Q + А.
Применение первого закона термодинамики к изопроцессам.
1. Изотермический процесс. Т = const.
∆T = 0; ∆U =0, Q = A /
1. Изохорный процесс.
∆V = 0; A / = 0.
Q = ∆U.
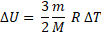
1. Изобарный процесс.
Р = const; A / >0, ∆U>0
Q = ∆U + A /.
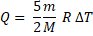
Используя уравнение Менделеева-Клапейрона, получим
υR(T2 – Т1) = P(V2-V1) = P∙∆V;
Подстановка в уравнение первого закона термодинамики количества теплоты дает
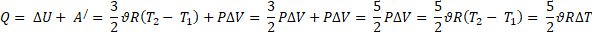
1. Адиабатный процесс.
Процесс, протекающий без теплообмена, т.е. Q = 0.
Тогда система может совершать работу либо за счет уменьшения внутренней энергии (газ расширяется) A / = - ∆U, либо за счет работы внешних тел над системой (происходит сжатие газа) А = ∆U.
Уравнение теплового баланса.
Если в замкнутой системе тела обмениваются энергией и работа этими телами не совершается, то суммарное изменение внутренней энергии системы равно нулю; тогда соответственно равна нулю и сумма количеств теплоты, полученных или отданных телами системы,
Q1 +Q2 +Q3 +Q4 +...+Qn = 0
Первый закон термодинамики не определяет направление тепловых процессов. Необратимыми называются такие явления, которые самопроизвольно протекают только в одном направлении; в обратном направлении они протекают только при внешнем воздействии.
Формулировка второго закона термодинамики: невозможно перевести тепло от менее нагретого тела к более нагретому телу при отсутствии других одновременных изменений в обеих системах или в окружающих их телах (или невозможен процесс, единственным результатом которого является передача энергии в форме теплоты от тела менее нагретого, к телу более нагретому).
Статистический характер второго закона термодинамики.
Состояние макроскопической системы (например, газ в баллоне) может быть реализовано огромным числом микросостояний (комбинацией в расположении молекул). Вероятность того, что первоначально находившийся в какой-либо части объёма газ весь снова соберется в какой-то момент времени в той же его части очень мала. А при очень большом числе частиц - ничтожно мала.
Вероятность обратимых процессов, наоборот, тем больше, чем меньше число частиц в системе. Поэтому справедливость второго закона термодинамики определяется достаточно большим объёмом и достаточно большим числом частиц системы. Так, например, ничтожно мала (реально равна 0) вероятность того, что спокойно висящий маятник начнет раскачиваться в результате одновременного, направленного в одну сторону удара всех молекул воздуха, до какого-то момента, двигавшихся хаотично по всем сторонам.
Направление термодинамических процессов определяется вторым законом термодинамики. Первый и второй законы термодинамики позволяют сделать заключение о невозможности создания вечного двигателя I и II рода.