К-витаминной активностью обладают многие производные нафтохинона (см. стр. 68). В зависимости от деталей их структуре существенно изменяется величина биологической активности соединения. Сравнительная оценка биологической активности витаминов группы К представлена в табл. 2.
| Таблица 2 | |||
| Биологическая активность витаминов группы К | |||
| Витамины | Активность, % | Витамины | Активность, % |
| К1 | К5 | ||
| К2 | К6 | ||
| К3 | К7 | ||
| К4 |
Как видно из данных табл. 2, гидрирование хиноидных групп, находящихся в положении 1,4, не оказывает существенного влияния на биологическую активность витаминов К. В то же время гидрирование самого нафтохинонового ядра приводит к почти полной утрате биологической активности молекулы. Замена гидроксильной группы на аминогруппу не сопровождается утратой биологической активности витамина. Для проявления биологической активности обязательно наличие метильной группы в положении 2 нафтохинонового ядра. Введение метильной группы в других позициях нафтохиноновой системы сопровождается резким уменьшением физиологической роли соединения.
Представляет особый интерес влияние изменения длины боковой изопреноидной цепи на биологическую активность производных нафтохинонов. Оказывается, что как укорочение, так удлинение углеводородной цепи вызывает снижение витаминной активности препарата. Наряду с этим полное удаление боковой цепи увеличивает активность молекулы в три раза.
Введение гидроксильных групп в различные позиции нафтохинонового ядра, за исключением положений 1 и 4, почти полностью лишает соединения витаминной активности. Примером 'такого соединения является фтиокол, или 2-метил-З-гидрокси-11,4-нафтохинон:

|
| Фтиокол |
Это соединение почти не обладает К-витаминной активностью, по данным некоторых ученых даже имеет антивитаминные свойства. Некоторые химические соединения, имеющие отдельные черты сходства в строении с витаминами группы К, обладают антивитаминными свойствами. Одним из первых антивитаминов К был открыт дикумарол – вещество, выделенное из испорченного сена бобовых растений (донник, клевер):

|
| Дикумарол (3,3’-метилен-бис-4-оксикумарин) |
Другим представителем антивитаминов К является производное фтиокола 2,2’-метилен-бис(3-гидрокси-1,4-нафтохинон) представляющее собой производное двух молекул фтиокола, формула которого приводится ниже:

|
| 2,2’-метилен-бис(3-гидрокси-1,4-нафтохинон) |
Третьим представителем этой группы соединений является варфарин:

|
| Варфарин |
Все названные вещества обладают геморрагическим действия на организм.
Биохимические функции
Как отмечено выше, обнаружение К-авитаминоза было связано с клинической картиной, показывающей замедление процессов свертывания крови. Это выражалось в точечном кровоизлии в ткани. Кровь, взятая из организма К-авитаминозных цыплят и других животных, часами оставалась жидкой при ее хранении.
В последующие годы было выяснено, что витамин К имеет отношение к синтезу протромбина – одного из факторов сложной ферментативной системы свертывания крови. Роль системы состоит в превращении растворимого в плазме белка фибриногена под ферментативным действием тромбина сначала в мономерную форму белка фибрина, а затем в полимерный, уже нерастворимый белок фибрин. Тромбин образуется из протромбина. Особенно сложным является многоступенчатый процесс превращения протромбина в тромбин. В плазме крови постоянно содержатся плазменные факторы свертывания крови (см. табл. 3), являющиеся белковыми веществами, и ионы кальция. В форменных элементах крови – тромбоцитах – содержится особый липопротеид, называемый тромбопластином тромбоцитов, или фактором III тромбоцитов. При разрушении тромбоцитов этот неактивный белок превращается под действием белков плазмы акцеллерина и конвертина в активную тромбокиназу, которая в присутствии других названных плазменных факторов и, кроме того, тканевого фактора начинает ферментативный процесс образования тромбина.
| Таблица 3 | |||
| Факторы свертывающей системы, содержащиеся в крови | |||
| Индекс | Название фактора | Индекс | Название фактора. |
| Ф.I | Фибриноген | Ф.VII | Конвертин и проконвертин |
| Ф.II | Протромбин (тромбин) крови | Ф.VIII | Антигемофильный глобулин А |
| Ф.III | Полный тромбопластин | Ф.IX | Антигемофильный глобулин В, фактор Кристмаса |
| Ф.X | Фактор Проуэра–Стюарта | ||
| Ф.IV | Ионы Са | Ф.XI | Фвктор Розенталя |
| Ф.V | Проакцеллерин | Ф.XII | Фактор Хагемана |
| Ф.VI | Акцеллерин | Ф.XIII | Фибринстабилизирующий фактор |
| – | Витамин К |
Как видно из схемы, витамин К непосредственно не входит в систему свертывания крови. Он необходим для синтеза в печени протромбина, проконвертина, фактора Х и фактора IX (см. табл. 3).
Специальное изучение биохимической роли витамина К позволяет предположить, что она заключается во влиянии на заключительную стадию формирования молекулы протромбина на посттрансляционном уровне. Наряду с этим имеются сведения об изменении способности протромбина К-авитаминозных организмов взаимодействовать с липидами, углеводами и кальцием. Вследствие этого нарушается активирующее действие факторов ввертывающей системы крови и процесса превращения протромбина в тромбин.
| Са2+ | ФIII тромбоцитов (липопротеид) | Плазменные факторы свертывания | Фибриноген | |
   
| Аутокатализ | 
| 
| |
| Протромбин | 
| Тромбин | Фибрин-мономер | |
 
| аутокатализ | 
| ||
| Тканевой фактор (тканевой тромбопластин) | Плазменные факторы свертывания | Фибрин-полимер (сгусток) | ||
| Схема свертывания крови |
Помимо участия витаминов К в процессе биосинтеза белковых факторов свертывания крови у высших животных, установлено, что они участвуют в окислительно-восстановительных превращениях. Это обусловлено способностью нафтохинонового ядра к обратимым окислительно-восстановительным превращениям. На некоторых микроорганизмах, в частности Escherichia Coli, и микобактериях показана роль менахинонов в биосинтезе пиримидиновых оснований при аэробных условиях. Менахинон принимает участие в превращении дигидрооротовой кислоты в оротовую. Возникающая при этом молекула восстановленного витамина К (менахинола) дегидрируется в присутствии фумаровой кислоты:

|  
| 
|  
| 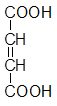
|
| Оротовая кислота | Менахинол | Фумаровая кислота | ||

| 
| 
| ||
| Дигидрооротат | Менахинон | Янтарная кислота |
Для растительных организмов показано участие витаминов я в транспорте электронов. Не исключена также роль витаминов Ц в процессах окислительного фосфорилирования в митохондриях животных клеток.
Связь с витаминами
При недостаточности витамина К наблюдали снижение активности аденозинтрифосфатазы и креатинкиназы в крови и скелетной мышце. Это приводит к пониженному использованию макроэргов, что отражается на повышении содержания АТФ в печени и сердце крыс и цыплят. Дополнительное введение витамина Е в рацион, лишенный витамина К, предупреждает снижение активности указанных энзимов в мышцах крыс. Это обнаруживает образование метаболитов, не обладающих антигеморрагическим действием, но, подобно витамину К, обеспечивающих нормальный биосинтез энзиматических белков.
Включение в рацион крыс витамина А – кислоты в дозе, не превышающей 50 ИЕ, значительно снижало содержание протромбина и повышало выделение витамина К с калом. Таким образом, витамин А кислота тормозила всасывание витамина К. Как недостаточность витамина А, так и гипервитаминоз А вызывают хрупкость лизосомных оболочек клеток толстой кишки, приводит к выделению из клеток ряда энзимов – b-глюкуронидазы, кислой фосфатазы и арилсульфатазы – и повышает их активность. Пероральное введение витамина К предупреждало освобождение этих энзимов при гипервитаминозе А. Подобное же освобождение арилсульфатазы происходит и из лизосом печени при гипервитаминозе А. Добавление витамина К1 в инкубируемую среду предохраняет лизосомы печени от освобождения арилсульфатазы. Следовательно, витамин К стабилизирует мембраны клеток и их органелл.
Биосинтез
Установлены основные этапы биосинтеза витамина К у микроорганизмов. Шикимовая кислота является одним из предшественников ароматического ядра хиноновых производных:

|
| Шикимовая кислота |
Имеются данные, показывающие значение сукцинилбензойной кислоты в синтезе менадионов. Схема превращения сукпинилбензойной кислоты в менадион представлена следующим рядом реакций:

| 
| 
| + | 
|
| Сукцинилбензойная кислота | 1,4-дигидрокси-3-карбокси-нафтогидрохинон (нафтоевая кислота) | Метионин | ||

| 
| |||
| 2-метилнафтоевая кислота |
К 2-метилнафтоевой кислоте присоединяется в дальнейшем пирофосфорный эфир соответствующего изопреноида.
Интересно отметить, что независимо от того, из каких объектов (растительных или микробных) поступает витамин К в организм человека и животных, в печени все они отщепляют изопреноидную цепь в положении 3 и превращаются в менадион (витамин К3). Затем происходит реакция присоединения свойственного для витамина К2(20) изопреноида, содержащего 20 углеродных атомов.
Авитаминоз
Как отмечено выше, недостаточное поступление в организм витамина К вызывает подкожные и внутримышечные кровоизлияния – геморрагии, возникшие в результате снижения скорости свертывания крови.
Уже упоминалось, что витамин К не является непосредственным участником процесса образования фибрина. Он необходим для синтеза в печени белков протромбина (фактор II), проконвертина (фактор VII), фактора Проуэра – Стюарта (фактор X) и фактора Кристмаса (антигемофильный глобулин В – фактор IX).
При К-авитаминозе оказываются сниженными содержание протромбина в крови и концентрация плазменных факторов свертывания крови.
Известен ряд заболеваний, сопровождающихся повышенной свертываемостью крови и образованием тромбов в сосудах (например, инфаркт, тромбофлебит). В этих случаях применяются различные препараты антивитаминов К. Следует отметить также, что для усвоения витамина К необходимо нормальное поступление желчи в кишечный тракт (последнее важно также и для других жирорастворимых витаминов).