1.В изотермическом процессе объем идеального газа, масса которого постоянна, увеличился на ∆v=3 л. Если при этом давление газа изменилось в четыре раза, то его конечный объем V2 равен 1)4 л 2)5 л 3)6 л 4)7 л 5)8 л
2.При изобарном нагревании идеального газа, масса которого постоянна, его объем изменился в два раза. Если в результате этого процесса температура газа изменилась на ∆t=3000С, то его первоначальная температура t1 была равна
1)27,00С 2)1600С 3)2100С 4)2700С 5)3000С
3.При нагревании идеального газа в герметически закрытом баллоне его температура изменилась в три раза. Если первоначальное давление газа р1=50 кПа, то в ходе процесса давление газа изменилось на ∆р, равное
1)100 кПа 2)150 кПа 3)200 кПа 4)250 кПа 5)300 кПа
4.В результате изотермического процесса давление идеального газа, масса которого постоянна, уменьшилось на ∆р=40 кПа. Если при этом объем газа изменился в пять раз, то его первоначальное давление р1 было равно
1)50 кПа 2)100 кПа 3)150 кПа 4)200 кПа 5)250 кПа
5.Если при нагревании идеального газа в герметически закрытом баллоне на ∆Т=160 К его давление изменилось в k=1,5 раза, то конечная температура Т2 газа равна 1)245 К 2)280 К 3)320 К 4)400 К 5)480 К
 6.Изобарному процессу для данной массы идеального газа, протекающему при максимальном значении его давления, соответствует участок графика 1)1-2 2)2-3 3)3-4 4)4-5 5)5-1
6.Изобарному процессу для данной массы идеального газа, протекающему при максимальном значении его давления, соответствует участок графика 1)1-2 2)2-3 3)3-4 4)4-5 5)5-1
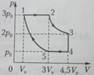
 7.Изотермическому процессу для данной массы идеального газа, протекающему при минимальной температуре, соответствует участок графика 1)1-2 2)2-3 3)3-4 4)4-5 5)5-1
7.Изотермическому процессу для данной массы идеального газа, протекающему при минимальной температуре, соответствует участок графика 1)1-2 2)2-3 3)3-4 4)4-5 5)5-1
8.Изохорному процессу для данной массы идеального газа, протекающему при максимальном значении объема, соответствует участок графика 1)1-2 2)2-3 3)3-4 4)4-5 5)5-1
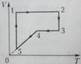
 9.Идеальный газ, количество вещества которого постоянно. Переводят из состояния 1 в состояние 3. В процессе перевода газ подвергся 1)сначала изобарному сжатию, затем изохорному нагреванию 2)сначала изотермическому расширению, затем изохорному нагреванию 3)сначала изотермическому сжатию, затем изохорному охлаждению 4)сначала изохорному нагреванию, затем изотермическому расширению
9.Идеальный газ, количество вещества которого постоянно. Переводят из состояния 1 в состояние 3. В процессе перевода газ подвергся 1)сначала изобарному сжатию, затем изохорному нагреванию 2)сначала изотермическому расширению, затем изохорному нагреванию 3)сначала изотермическому сжатию, затем изохорному охлаждению 4)сначала изохорному нагреванию, затем изотермическому расширению
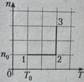
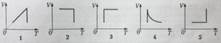 10. Идеальный газ, количество вещества которого постоянно, переводят из состояния 1 в состояние 3 так, что зависимость концентрации n его молекул от температуры Т имеет вид, изображенный на рисунке слева. Этой зависимости в V-T-координатах, где V- объем газа, соответствует график справа, обозначенный цифрой 1)1 2)2 3)3 4)4 5)5
10. Идеальный газ, количество вещества которого постоянно, переводят из состояния 1 в состояние 3 так, что зависимость концентрации n его молекул от температуры Т имеет вид, изображенный на рисунке слева. Этой зависимости в V-T-координатах, где V- объем газа, соответствует график справа, обозначенный цифрой 1)1 2)2 3)3 4)4 5)5
11.Если при изобарном нагревании идеального газа, начальная температура которого t1=7,00С, его объем увеличился в k=1,2 раза, то конечная температура t2 газа равна 1)8,40С 2)140С 3)240С 4)400С 5)630С
12.При изотермическом сжатии давление идеального газа изменилось от р1=0,15 МПа до р2=0,18 МПа. Если конечный объем газа V2=5,0 л, то начальный объем V1 газа равен 1)6,0 л 2)6,2 л 3)7,0 л 4)7,5 л 5)8,2 л
13.В ходе изобарного процесса температуру идеального газа, количество вещества которого постоянного, понизили до t=27,00С. Если объем газа при этом уменьшился в два раза, то начальная температура t0 газа была равна
1)3270С 2)3000С 3)2730С 4)54,00С
14.Если при изохорном нагревании идеального газа его абсолютная температура повысилась на ∆Т=45 К, а давление увеличилось на 15%, то начальная температура t1 газа была равна 1)170С 2)270С 3)540С 4)730С 5)990С
 15.На рисунке изображена зависимость концентрации n молекул от давления р для пяти процессов с идеальным газом, количество вещества которого постоянно. Изохорное нагревание газа происходит в процессе 1)0-1 2)0-2 3)0-3 4)0-4 5)0-5
15.На рисунке изображена зависимость концентрации n молекул от давления р для пяти процессов с идеальным газом, количество вещества которого постоянно. Изохорное нагревание газа происходит в процессе 1)0-1 2)0-2 3)0-3 4)0-4 5)0-5
 16.На р-V-диаграммах изображены зависимости давления р от объема V для идеального газа, количество вещества которого постоянное. Изохорному охлаждению соответствует график на рисунке, обозначенном буквой
16.На р-V-диаграммах изображены зависимости давления р от объема V для идеального газа, количество вещества которого постоянное. Изохорному охлаждению соответствует график на рисунке, обозначенном буквой
1)А 2)Б 3)В 4)Г 5)Д
17.ЦТ-13 На р-т –диаграмме изображены различные состояния одного моля идеального газа. Состояние, соответствующее наименьшему давлению р газа обозначено цифрой 1)1 2)2 3)3 4)4 5)5 