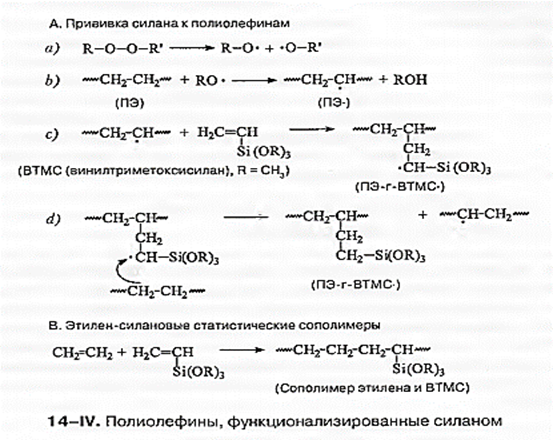
Сшивка и контролируемая деструкция полиолефинов
При модификации полиолефинов после синтеза используются различные химические реакции для усиления свойств полиолефина и даже для достижения новых свойств, которые могут расширить потенциальный круг областей применения. На основе исходной более или менее линейной структуры цепи могут наблюдаться два противоположных модифицирующих эффекта, влияющих на молекулярную массу полиолефина: сшивка, при которой термопластичный полимер преобразуется в трехмерную структуру; деструкция, при которой средняя молекулярная масса уменьшается в результате разрыва полимерной цепи.
Сшивка и деструкция зачастую являются нежелательны в течение всего цикла производства, переработки, эксплуатации и возможной повторной переработки (рециклинга) полимера. Однако, как сшивка, так и деструкция в контролируемых условиях могут стать ценными инструментами целенаправленного изменения структуры и свойств полимеров.
Сшивка — это общий термин для процесса образования ковалентных связей или относительно коротких последовательностей химических связей для соединения вместе двух полимерных цепей. Сшивка (образование поперечных связей между цепями) происходит за счет различных химических реакций, в которых участвуют реакционноспособные центры полимерных цепей.
Трехмерная структура, образуемая в результате сшивки, не только значительно улучшает многие свойства, такие как высокотемпературные, механические, химическая стойкость и стойкость к растрескиванию под нагрузкой, но также и придает полиолефинам новые полезные свойства, такие как эффект памяти формы. Насыщенные углеводородные цепи полиолефинов, не имеющих функциональных групп, сшиваются поперечными С-С-связями в результате рекомбинации полиолефиновых макрорадикалов, образованных под действием радиации или химических реагентов (пероксидов). Введение в структуру полиолефина гидролизуемых алкоксисилановых групп как за счет присоединения ненасыщенных органосиланов после синтеза, так и за счет рэндом-сополимеризации в реакторе этилена с такими винилсиланами приводит к протеканию альтернативных процессов, при которых возможно соединение полиолефиновых цепей с введенными функциональными группами в трехмерную сетку за счет образования силоксановых (Si-0-Si) связей в присутствии микроколичеств влаги и катализатора поликонденсации.
Некоторые полиолефины склонны к реакциям разрыва цепи в присутствии свободных радикалов. Использование органических пероксидов для контролируемой деструкции ПП является самым важным коммерческим применением процесса разрыва цепи полиолефиновых цепей.
I. Принципы сшивки и контролируемой деструкции полиолефинов
Радиационная или пероксидная сшивка, контролируемая деструкция и силанольная прививка — это процессы модификации полиолефинов, основанные на радикальных реакциях.
Все эти процессы модификации начинаются с образования полиолефиновых макрорадикалов на некоторой стадии процесса.
Образование и гибель макрорадикалов в полиолефинах.
1. Свободно-радикальные системы свободных радикалов в полиолефинах.
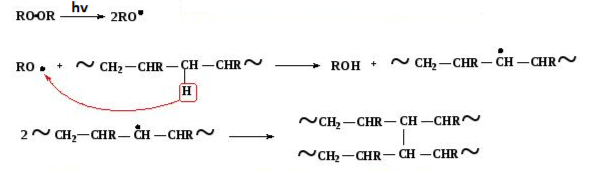
Обычной в промышленности практикой является получение макрорадикалов вследствие термического разложения органических пероксидов или под действием жесткой радиации с высокой энергией. Практический способ инициирования включает образование макрорадикала на полиолефиновой цепи за счет разрыва С-Н-связи под действием излучения с высокой энергией (у- или β-лучи) или за счет отрыва атомов водорода первичными свободными радикалами (RO •), полученными при термическом разложении органических пероксидов ROOR' (схема 1).
| R – O – O – R’ | ––––––––→ | RO• + •OR’ |
| PH + •OR | ––––––––→ | P• + ROH |
| ~ CH2 – CH (CH3) – CH2 – CH (CH3) ~ | +hυ | ~ CH2 – C• (CH3) – CH2 – CH (CH3) ~ |
| ––––––––→ | ||
| ~ CH2 – CH2 – CH2 – CH2 ~ | + RO• | ~ CH2 – CH• – CH2 – CH2 ~ |
| ~ CH2 – CH = CH2 | ~ CH = CH ~ | ~ CH2 – C(CH2) – CH2 ~ |
| Концевая винильная группа | Транс- винилен | Винилиден |
Схема 1. Образование макрорадикалов в полиолефинах под действием радиации и первичных свободных радикалов.
Независимо от способа инициирования (радиационный или пероксидный), образование макрорадикалов зависит от структуры полиолефина. Энергия диссоциации связи с водородом, т. е. энергия, необходимая для гомолитического разрыва ковалентных С-Н-связей, отражает стабильность и реакционную способность радикала и его исходного соединения. Таким образом, оторвать атом водорода от массивного третичного алкана (R3C-H) легче, чем от менее габаритного вторичного алкана (R2CH-H), который, в свою очередь, является менее стабильным и более реакционно-способным, чем первичный алкан (RCH2-H), самый нереакционно-способный из всех этих структур.
Полиолефиновые макрорадикалы могут быть полностью или частично ингибированы кислородом, особенно на поверхности изделий. Кислород чрезвычайно быстро реагирует с полиолефиновыми макрорадикалами (Р • + 0 2 —* РОО •), в то время как получающиеся пероксидные макрорадикалы реагируют сравнительно медленно. Таким образом, выход инициирующих макрорадикалов и, следовательно, общее количество продуктов реакции уменьшается.
2. Разрыв цепи.
Образованные полиолефиновые макрорадикалы могут участвовать в двух типах реакций с противоположным влиянием на молекулярную массу полимера, т. е. происходит разрыв цепи или разветвление и сшивка. Разрыв цепи происходит в том случае, если С-С-связь около макрорадикала склонна разрываться на два меньших фрагмента. Это типично для ПП, в котором соответствующий макрорадикал является радикалом с центром на третичном атоме С, а такой радикал менее реакционноспособен, чем радикал с центром на вторичном атоме С ПЭ (см. схему 14-1). Следовательно, макрорадикалы ПП склонны к фрагментированию на радикалы с центром на вторичном атоме С и на более мелкие ненасыщенные цепи в результате так называемого β-разрыва (схема 14—2а). 

Схема 14-2. Разрыв цепи и сшивка полиолефинов
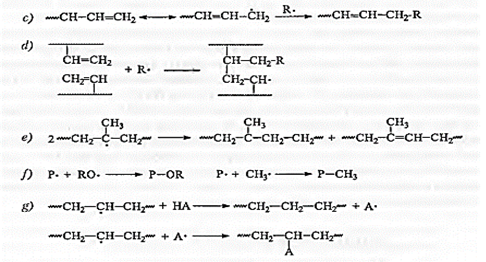
Схема 14-2. Разрыв цепи и сшивка полиолефинов. Продолжение.
Однако в случае ПЭ соответствующий макрорадикал, скорее всего, соединяется с другим макрорадикалом, образуя структуру с длинными разветвленными цепями (см. схему 14—26). Если продолжается бимолекулярный обрыв за счет рекомбинации макрорадикалов, то в конечном счете получается трехмерная сетка с различными степенями сшивки. Если макрорадикалы ПЭ образуются за счет отрыва аллильного атома Н (см. схему 14—1), то сшитая структура может содержать также транс-виниленовые двойные С=С-связи (см. схему 14—2с). Присутствие в полиолефине ненасыщенных структур, особенно винильных групп, увеличивает эффективность сшивки, потому что макрорадикалы за счет ненасыщенности присоединяются к полимерной цепи (см. схему 14— 2d).
В сополимерах этилена и пропилена, которые имеют среднюю структуру между двумя крайними случаями (ПЭ и ПП), результаты конкуренции процессов разрыва цепи и сшивки зависят от молекулярного состава, т. е. эффективность сшивки значительно увеличивается при увеличении содержания этиленовых остатков. Полиолефиновые макрорадикалы могут быть вовлечены в некоторые побочные реакции, как показано на схеме 14—2, в том числе: диспропорционирование (е); рекомбинация с радикалами, полученными при разложении пероксидов (f); реакция с антиоксидантами (g). По сравнению со сшивкой, при увеличении температуры роль как реакций β-разрыва, так и реакций диспропорционирования значительно увеличивается.
3. Прививка функциональных мономеров.
Мономеры с реакционноспособными свободными радикалами (с ненасыщенной двойной С=С-связью) могут быть присоединены (или привиты) к полиолефиновой цепи либо как индивидуальные единицы, либо как более длинные прививаемые участки. Прививаемая свободнорадикальная система обычно состоит из полимера; ненасыщенного соединения, такого как виниловый мономер; источника свободных радикалов, из которых самыми важными являются пероксиды. Хотя имеется множество способов инициирования реакции прививки, но только свободнорадикальная прививка, в частности прививка мономеров к полимерам при реакционной экструзии, практикуются широко и в значительных объемах, что объясняется доступностью и дешевизной этого процесса.
Прививка зачастую является единственной необходимой реакцией, однако прививаемая система является очень сложной, что обусловлено наличием большого количества возможных конкурирующих реакций, как представлено на схеме 14—3. Первичные свободные радикалы RO •, образованные в результате термического разложения пероксида ROOR' (а), образуют полиолефиновые макрорадикалы Р • за счет отрыва атома Н (6), но также могут реагировать с мономером М (с). Если полученный мономерный радикал RM • продолжает реагировать с другими молекулами мономера (RMxM •), то, в конечном счете, образуется олигомер или высокомолекулярный полимер (d), при этом нежелательная гомополимеризация мономера конкурирует с его прививкой. Прививка мономерного макрорадикала RMJVI • к полиолефиновому скелету PH (е) практически исключена, потому что растущие макрорадикалы имеют лишь небольшую способность отрывать атомы Н, если, конечно, мономер не является очень реакционноспособным, например, винилацетатом.
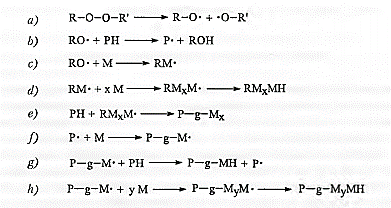
Схема 14-3. Свободнорадикальная прививка мономеров к полиолефинам.
Полиолефиновые макрорадикалы Р•, образованные на стадии инициирования (b), могут быть вовлечены в реакции разрыва цепи и сшивки, как рассматривалось ранее (см. схему 14—2). Однако они могут также принимать участие и в реакции с мономером М (f), образуя, таким образом, разветвленный макрорадикал P-g-M •, который открывает дополнительный путь прививки. Такой разветвленный макрорадикал может подвергнуться передаче атома Н той же самой или другой полимерной цепи, с образованием нового полиолефинового макрорадикала Р • (g), который повторяет цикл, повышая степень прививки. В получающейся структуре (P-g-MH) остатки мономера присоединены к полиолефиновой цепочке в виде индивидуальных единиц. Если разветвленный макрорадикал продолжает реагировать с другими молекулами мономера, то образуется растущая боковая цепь P-g-MyM • (h), а конечная структура содержит длинные привитые цепи.
Для практического применения требуется высокая степень прививки. Для этой цели доля первичных радикалов и макрорадикалов, которые отрывают атомы Н от полиолефиновой цепи (b), должна быть намного больше, чем доля первичных радикалов, которые реагируют с мономером (с). Образованный полиолефиновый макрорадикал Р • не должен быть вовлечен в реакции разрыва цепи или сшивки, а его способность инициировать прививку мономера (f) должна быть намного выше, чем способность растущего мономерного радикала инициировать гомополимеризацию (d).
Свободнорадикальная прививка мономеров в расплаве на полимеры стала одним из самых важных применений технологии реакционной экструзии.
Виды сшивки
1. Радиационная сшивка.
В начале 1950-х гг. Чальзби (Charlesby) и Лоутон (Lawton)] сделали вывод, что все формы высокоэнергетического излучения способны обеспечить процесс сшивки ПЭНП. Когда излучение атома проходит через материалы, большая часть энергии рассеивается за счет ионизации и возбуждения электронов. Этот процесс может вызывать несколько эффектов, но для полимеров важнее всего является разрыв химических связей, что приводит к образованию свободных радикалов (см. схему 1). Для ПЭ, в котором доминирует реакция рекомбинации образованных алкилрадикалов, результатом облучения является образование поперечных С-С-связей, в то время как в ПП происходит разрыв цепи (см. схему 14—2). Степень сшивки в облученном полимере пропорциональна дозе поглощенного излучения, отнесенной к единице массы облученного объекта. Единицей измерения этой дозы является рад (поглощенная доза излучения, 1 Мрад = 10 кДж/кг). Типичные дозы (Мрад), необходимые для сшивки полиолефинов (представлены на слайде), составляют ПЭ: 20-30 Мрад; сополимеры этилена и винилацетата, этилена и метакрилата, этилена и этилакрилата и этилена и бутилакрилата: < 20 Мрад; СКЭП(этилен пропиленовый каучук): 15-20 Мрад; СКЭПТ (тройной сополимер этилен-пропиленового каучука): 10 Мрад.
Полимеры, склонные к реакциям разрыва цепи, такие как ПП, ПВХ, ПИБ и ПММА, не могут подвергаться радиационной сшивке, а при облучении деструктируются. Продукты разложения ПЭ в основном состоят из Н2 (результат отрыва атома Н) и летучих углеводородов, таких как СН4 и С2Н6 (результат разложения боковых ветвей), например, на 1 Мрад из 1 г ПЭНП образуется 0,06 см3 газа, 75—85% которого состоит из Н2.
Радиационная сшивка используется в основном при изоляции кабелей и проводов низкого напряжения.
2. Пероксидная сшивка.
Пероксидная сшивка, как правило, является двухстадийным процессом:
1. Способный к сшивке полимер первоначально получается на перерабатывающем оборудовании за счет введения в расплав полимерной матрицы соответствующего пероксида, после чего производится переработка материала в конечные изделия, такие как изоляция кабелей и трубы, при таких условиях, которые позволяют не допустить нежелательной преждевременной сшивки (отверждения, предвулканизации).
2. Затем сшитая структура получается термообработкой готовых изделий, обычно выполняемой на той же линии непосредственно после стадии экструзии.
Пероксид является ключевым элементом в этой технологии, поэтому он должен удовлетворять множеству требований:
- смеси пероксида и полиолефина при температурах переработки должны медленно разлагаться (т. е. при температурах выше температуры плавления полиолефина — например, при 110 °С для ПЭНП и 135 °С — для ПЭВП);
- для достижения высоких скоростей сшивки необходимо быстрое разложение при термообработке;
- пероксид должен разлагаться с образованием первичных радикалов, которые могут образовать полиолефиновые макрорадикалы за счет отрыва атома Н (см. схему 1);
- необходимо выполнение дополнительных требований относительно физической формы, стабильности при хранении, охраны здоровья и безопасности использования, необходимости получения разрешения для применения в изделиях, контактирующих с пищевыми продуктами, а также других факторов.
Поэтому из множества различных пероксидов только ограниченное количество подходит для сшивки.
Органические пероксиды можно рассматривать как производные пероксида водорода (Н-О-О-Н) с общей формулой R 1 -О -О –R2, характеризуемой наличием пероксидной группы —О-О—, которая за счет гомолитического разрыва ее ковалентной связи может разлагаться с образованием двух радикалов (R1OOR2 → R1 О• + • OR2). Пероксиды являются жидкими или твердыми соединениями. Органические пероксиды можно разделить на несколько классов в зависимости от природы органических радикалов R1 и R2:
· Гидропероксиды R-О-ОH (Н.п. Трет-бутилгидропероксид),
· Алкил-арил пероксиды R1-O-O- R2,(Н.п. Ди-трет-бутилпероксид, R: СН3, 2,2 -бис-(трет-бутилперокси)бутан)
· Сложные пероксиэфиры R1- CО - О - О – R2 (Эти пероксиды являются производными перокси-кислот (R-CO-O-O-H), в которых кислотный атом Н заменен на алифатический радикал, обычно трет-бутил. Н.п. Треш-бутилпероксибензоат, R: С6Н5).
· Перокси-карбонаты R1- О - C О - О - О – R2 (Эти пероксиды могут расцениваться как производные угольной кислоты; они похожи по структуре на сложные пероксиэфиры.)
· Диацилпероксиды (Так же, как и алкил-арил пероксиды, радикалы R1 и R2 могут быть алифатическими и/или ароматическими. Однако только среди диароилпероксидов (оба радикала являются ароматическими группами) имеются соединения, пригодные для сшивки.
· Перокси-кетали (Эти пероксиды можно расценивать как производные соответствующих кеталей, в котором атомы О эфирной связи замещены на пероксидные группы.)
· Циклические пероксиды (Некоторые пероксиды содержат две или три пероксидные группы, включенные в циклические структуры)
Полная реакция сшивки полиолефинов органическими пероксидами может быть разделена на три последовательных стадии:
- гемолитическое разложение пероксида на первичные свободные радикалы;
Органические пероксиды являются источником свободных радикалов за счет гемолитического разрыва неустойчивых О-О-связей при соответствующих температурах. Эти первичные свободные радикалы имеют неспаренный (свободный) электрон и являются очень реакционноспособными интермедиатами с коротким временем жизни (период полураспада менее 10-3 с).
Разложение пероксида на первичные радикалы может сопровождаться различными побочными реакциями, что показано на схеме 14—5 для промышленно важного ДКУП. Первичный кумилокси-радикал (14—5a), необходимый для обеспечения отрыва атомов Н от полиолефиновой цепи (14—5b), может также привести к образованию метального радикала и ацетофенона (14—5c). Метальный радикал также участвует в отрыве атома Н (14—5b), в то время как его рекомбинация (14—5d, е) происходит в незначительной степени.
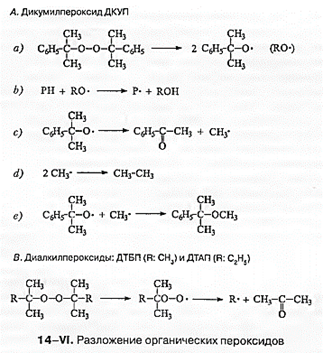
Более быстрый отрыв атомов Н протекает с участием менее стабильных и более реакционноспособных свободных радикалов, которые соответствуют менее избирательному поведению радикала. Метальные радикалы более активны, чем другие первичные алкильные радикалы, и примерно так же активны, как и алкоксильные радикалы. Поэтому и метальные, и алкоксильные радикалы пригодны для реакций сшивки, деструкции и прививки.(эффективными для отрыва атомов Н являются метальные, фенильные, треяг - бути л о кси л ьн ые, кумилоксильные и бензоильные или замещенные бензоильные радикалы.) Однако замещенные углеродные радикалы, такие как этильный радикал, неэффективны для отрыва атома Н.,тк они более стабильные.
Молекулы пероксида могут разлагаться также от действия первичных и вторичных радикалов, образованных непосредственно из пероксида, из растворителя или из какого-либо реакционно-способного вещества, присутствующего в системе.
- отрыв свободными радикалами атомов Н от полиолефиновой цепи, с образованием устойчивых продуктов разложения пероксида и полиолефиновых макрорадикалов;
- рекомбинация двух макрорадикалов с образованием поперечных С-С-связей.
В то время как первая стадия определяет общую скорость реакции (является лимитирующей стадией), ее эффективность зависит в основном от образованных типов первичных свободных радикалов, а также от типов полиолефиновых макрорадикалов, образующихся на второй стадии. Химические структуры как пероксида, так и полиолефина играют решающую роль в процессе сшивки. Почти все коммерческие полимеры несут в основной цепи полимера вторичные или третичные атомы Н. Поэтому почти все термопласты, а также природные и синтетические эластомеры, могут быть сшиты с помощью пероксидов по механизму отрыва Н. Только для нескольких полимеров, таких как ПП, ПВХ и гомо- и сополимеры бутена-1 или изобутена, склонных к разрыву цепи, пероксидная сшивка без дополнительной помощи не типична или невозможна.
3. Силанольная сшивка.
Попытки улучшения технологии привели к разработке методов силанольной сшивки, при которой не только преодолеваются некоторые недостатки радиационной и пероксидной сшивки, но также и обеспечиваются новые области применения.
При силанольной сшивке в материал вводятся соответствующие органофункциональные силаны.
Органофункциональные силаны обычно описываются общей формулой Y-(CH2)n-SiX3 (n обычно равно 0—3). Центральное кремниевое звено связано с двумя различными функциональными группами. Органофункциональная группа Y прочно связана с кремнием либо напрямую, либо за счет стабильной, нереакционной углеродной цепи, и ее структура допускает возможность адгезии и связывания с полимерами за счет различных механизмов. Три одинаковые кремнийфункциональные группы X, в основном алкоксильные группы, непосредственно соединенные с кремнием, относительно легко гидролизуются. После их гидролиза до силанольных групп они могут реагировать с активными участками полимеров и неорганическими материалами (обычно с группами ОН), тем самым образуя стабильные связи за счет реакций конденсации. Типы силанов, способные к действию в качестве сшивающих агентов для полиолефинов, должны иметь полимеризуемые органофункциональные группы, обычно винильную группу. Различные кремнийфункциональные группы X гидролизуются с различной скоростью, убывающей в следующем ряду: ацетокси > метокси > 2-метоксиэтокси > этокси.
Таблица 1. Органофункциональные силаны.
| Тип силана | Химическое название и структурная формула | Молекулярная масса | Плотность при 20 ◦С, г/см3 | Температура плавления, ◦С | Температура воспламенения, ◦С |
| ВТМС | Винилтриметоксисилан | 148,3 | 0,968 | ||
| ВТЭС | Винилтриэтоксисилан | 190,3 | 0,900 | ||
| ВМЭС | Винил-трис-(2-метоксиэтокси)силан | 280,4 | 1,045 | ||
| ВТАС | Винилтриацетоксисилан | 230,0 | 1,164 | ||
| МТМС | 3-метакрилооилоксипро-пилтриметоксисилан | 248,1 | 1,047 | ||
| ВДМС | Винилметилдиметокси- силан | 132,3 | 0,880 |
У основных поставщиков доступны коммерческие марки технически чистых силанов (табл. 2). Эти жидкие силаны могут использоваться для производства сшиваемых под действием влаги статистических сополимеров этилена и графт-полиолефинов (привитых) в сочетании с другими необходимыми добавками, такими как пероксидные инициаторы, катализаторы сшивки и стабилизаторы.
Таблица 2. Производители и торговые названия коммерческих марок силанов.
| Тип силана | Momentive P.M. Silquest | Evonik Dynasylan | Dow Corning Designation |
| ВТМС | А-171 | VTMO | – |
| ВТЭС | А-151 | VTEO | – |
| ВМЭС | А-172 | VTMOEO | Z-6082 |
| ВТАС | А-188 | – | Z-6075 |
| МТМС | А-174 | MEMO | Z-6030 |
| ВДМС | А-2171 | – | – |
· Жидкие силановые композиции
Введение некоторых или всех добавок в силан обеспечивает получение жидких композиций для использования в процессах силанольной прививки. В процессе инициатор прививки обычно вводится в силан. Жидкие силановые композиции для одностадийного процесса прививки представляют собой смесь силана, инициатора прививки и катализатора конденсации, например, марки Dynasylan Silfln.
С точки зрения транспортировки и хранения эти многокомпонентные системы имеют более серьезные и строгие ограничения, чем технически чистые силаны. Присутствие катализатора конденсации делает силан еще более чувствительным к действию влаги. Из-за присутствия пероксидов силаны могут экзотермически реагировать с гомополимеризацией. Часто используются специальные ингибиторы для предотвращения преждевременной полимеризации.
· Сухие силановые композиции
Жидкие добавки могут дозироваться насосом с очень высокой степенью точности, но это преимущество сопровождается многими недостатками, среди которых дополнительные капиталовложения для приобретения относительно дорогого дозирующего оборудования, потенциальная возможность разлива, проскальзывание шнека в экструдере и длительная чистка оборудования. Многие потребители предпочитают использовать не жидкие или пастообразные добавки, а свободно сыпучие твердые частицы, потому что обращаться с твердыми частицами намного легче, а дозировать их можно более простыми методами, такими как объемные и гравиметрические (весовые) дозаторы.
Также при обычном смешении в расплаве нельзя получить концентраты с содержанием добавки более 10—20% из-за ограниченной способности введения в полимеры жидкостей. Другим способом превращения жидкости в твердые частицы является использование пористых, подобных губке полимеров-носителей; набухающих полимеров. На практике только первый вариант принят в промышленности. Вначале подготавливаются частицы полимера с большим объемом (до 75%) мелких открытых микропор. Эти микропористые структуры действуют как крошечные губки и поглощают массу жидкости в несколько раз больше собственного веса. Если жидкие или легкоплавкие твердые частицы смешиваются с пористым полимером, то пустоты в полимере микронных размеров заполняются капиллярной абсорбцией. Поскольку смешение производится при комнатной температуре периодически, то этот процесс особенно пригоден для термочувствительных добавок, таких как пероксиды и силаны. В носитель может вводиться фактически неограниченное количество добавок, которые могут быть преднамеренно объединены. При полном вводе жидких добавок система остается сухой, в виде свободно сыпучих порошков или гранул с очень высокой концентрацией добавки (до 70 %масс).
Для производства таких микропористых материалов полиолефин смешивается с инертным порообразователем для увеличения пустот. Затем растворитель экстрагирует агент из полимерных частиц. После сушки форма частицы остается прежней, не набухая при введении жидкой добавки
Большинство сухих силановых композиций (концентраты, суперконцентраты) являются материалами, изготовленными под заказ. Однако доступны также и стандартные коммерческие марки материалов. Например, Rex-Master Sil С-В компании Polyrex Additives, Швейцария, представляет собой полиолефиновый порошок (объемная плотность 0,4 г/см3), содержащий приблизительно 20% смеси силана, пероксида и катализатора конденсации. Silcat DSE 40-735 компании Momentive Performance Materials, США, является сухим концентратом силана на основе полностью стабилизированной рецептуры с жидким силаном и содержит 40% сшивающих химических соединений. Компания Wilson Color of Hanna поставляет сухие силановые концентраты DS (трех- и пятикомпонентные системы) с концентрацией силана 70% на ПП носителе.
Сухие силановые композиции обычно более стабильны и безопасны, чем жидкие силаны, при транспортировке и хранении. Срок годности составляет 6—12 месяцев при температурах ниже 30—40 °С в невскрытой стандартной транспортной упаковке.
В ходе силанольной сшивки вводят в основном винилтриалкоксисиланы CH2=CH-Si(OR)3 (R: СН3, С2Н5). Эти соединения имеют как свободнорадикальную активность (полимеризуемые С=С-связи), так и химическую функциональность, состоящую из относительно легко гидролизуемых алкоксисилановых групп. Введенные в структуру полиолефина с помощью прививки (14-4А) или статистической сополимеризации (14-4В), силаны функционируют как сшивающие агенты. В отсутствие воды модифицированные полиолефины все еще остаются термопластичными материалами, которые могут быть переработаны обычным способом в конечные изделия. Если готовые изделия подвергаются действию микроколичеств воды, то алкоксисилановые группы гидролизуются в силанольные группы, которые далее конденсируются, образуя при этом трехмерную сетку с силоксановыми поперечными связями между различными полиолефиновыми цепями. (14-5) Реакция сшивки медленно продолжается без добавления какого-либо катализатора. Следовательно, отличительной чертой этих полимеров является их чувствительность к влаге при хранении, т. е. имеется риск преждевременной сшивки. Для уменьшения этого риска используется влагонепроницаемая упаковка.
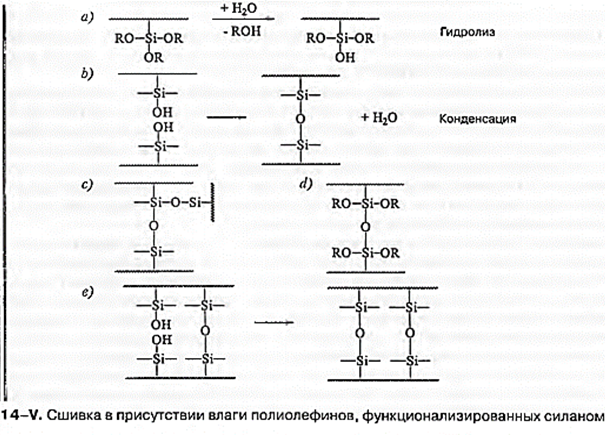
Химизм силанольной сшивки намного более сложен, чем химизм пероксидной и радиационной сшивки. Цепь модифицированного силаном полиолефина способна к реакции с двумя или большим количеством подобных цепей с образованием сетки с поперечными связями —Si-0-Si— (с). Однако имеются и дополнительные возможности образования силоксановых мостиков, такие как:
· реакция между полиолефиновыми цепями только с одной силанольной группой, в результате которой образуется разветвленная, но не сшитая структура (d);
· полиолефиновые цепи, которые уже являются частью сетки, могут образовать еще больше поперечных связей, тем самым увеличивая плотность сшивки внутри гельфракции (е);
· образование циклических силоксанов; менее вероятно, поскольку при этом используется четырехатомное кольцо со значительным напряжением, которое из-за этого было бы термодинамически нестабильным.
Нежелательная термическая сшивка при переработке модифицированных силанами полиолефинов еще более усложняет механизмы сшивки, потому что в результате нее происходит образование С-С-связей вместо необходимых мостиков Si-O-Si, образуемых при сшивке под действием влаги.
Поскольку реакция прививки не является концевой реакцией (представлено ранее на схеме 14—3), то до того момента, когда присутствующие в реакционной смеси радикалы станут неактивными, происходит рекомбинация и другие реакции. Хотя количество пероксида, используемое для прививки, приблизительно в 20 раз меньше, чем используемое для пероксидной сшивки, образованные пероксидом полиолефиновые макрорадикалы могут рекомбинировать, образуя при этом С-С-связи, которые приводят к росту молекул (во время прививки всегда наблюдается снижение ПТР исходного полиолефина) и реакциям сшивки (предварительное отверждение в экструдере.