| Вопрос №1 |
Укажите давление, при котором должна быть определена термодинамическая величина, чтобы считаться стандартной:
| a)p | 1 атм |
| b)p | 0,1 атм |
| c)p | 0,5 атм |
| d)p | 2,5 атм |
| e)p | 2 атм |
| Вопрос №2 |
Укажите температуру, для которой в справочниках приводятся стандартные термодинамические величины:
| a)p | 310К |
| b)p | 273К |
| c)p | 298К |
| d)p | 293К |
| e)p | 278К |
| Вопрос №3 |
Вставьте пропущенное слово: «Энергия не возникает из ничего и не исчезает, она может только переходить из одной формы в другую в …… количествах»:
| a)p | больших |
| b)p | небольших |
| c)p | эквивалентных |
| d)p | максимальных |
| e)p | минимальных |
| Вопрос №4 |
Закончите определение: «Степень нагретости тела, определяемая распределением молекул по энергетическим уровням, называется ….. »
| a)p | работой |
| b)p | теплоёмкостью |
| c)p | теплотой |
| d)p | тепловым эффектом |
| e)p | температурой |
| Вопрос №5 |
Укажите экстенсивный параметр термодинамической системы:
| a)p | температура |
| b)p | концентрация |
| c)p | объём |
| d)p | давление |
| Вопрос №6 |
Укажите интенсивный параметр термодинамической системы:
| a)p | температура |
| b)p | внутренняя энергия |
| c)p | масса |
| d)p | объём |
| Вопрос №7 |
Термодинамическая функция называется функцией состояния, если её изменение
| a)p | определяется только начальным состоянием |
| b)p | определяется только начальным и конечным состояниями |
| c)p | зависит от пути процесса |
| Вопрос №8 |
Укажите величину, не являющуюся функцией состояния:
| a)p | энтропия |
| b)p | энтальпия |
| c)p | внутренняя энергия |
| d)p | работа |
| e)p | энергия Гиббса |
| Вопрос №9 |
Тело или группа тел, находящихся во взаимодействии, мысленно обособленные от окружающей среды и имеющие поверхности раздела – это:
| a)p | вариантность |
| b)p | фаза |
| c)p | составная часть |
| d)p | термодинамическая система |
| e)p | компонент |
| Вопрос №10 |
Система, способная к обмену с окружающей средой веществом и энергией, называется
| a)p | изолированной |
| b)p | идеальной |
| c)p | закрытой |
| d)p | открытой |
| e)p | гомогенной |
| Вопрос №11 |
Система, способная к обмену с окружающей средой только энергией, называется
| a)p | открытой |
| b)p | изолированной |
| c)p | закрытой |
| d)p | идеальной |
| e)p | гетерогенной |
| Вопрос №12 |
Система, неспособная к обмену с окружающей средой ни веществом, ни энергией, называется
| a)p | закрытой |
| b)p | многофазной |
| c)p | изолированной |
| d)p | однофазной |
| e)p | открытой |
| Вопрос №13 |
Закончите определение: «Изобарным называется процесс, протекающий при постоянном...... »
| a)p | объёме |
| b)p | значении концентрации |
| c)p | давлении |
| d)p | значении температуры |
| e)p | количестве теплоты |
| Вопрос №14 |
Закончите определение: «Изохорным называется процесс, протекающий при постоянном...... »
| a)p | давлении |
| b)p | значении энтальпии |
| c)p | количестве теплоты |
| d)p | значении температуры |
| e)p | объёме |
| Вопрос №15 |
Как называется процесс, идущий при постоянном количестве теплоты?
| a)p | адиабатическим |
| b)p | самопроизвольным |
| c)p | изобарным |
| d)p | изотермическим |
| e)p | изохорным |
| Вопрос №16 |
Закончите формулировку: «В изолированной системе сумма всех видов энергии …… »
| a)p | отрицательна |
| b)p | равна нулю |
| c)p | непостоянна |
| d)p | постоянна |
| Вопрос №17 |
Закончите определение: «Отношение количества поглощённой телом теплоты к изменению температуры, вызванному этим поглощением, называется …… »
| a)p | теплотой растворения |
| b)p | энтропией |
| c)p | тепловым эффектом |
| d)p | внутренней энергией |
| e)p | теплоёмкостью |
| Вопрос №18 |
Вставьте пропущенное слово: «Количество теплоты, затрачиваемой на нагревание одного моля вещества на один градус, называется..... теплоёмкостью»
| a)p | удельной |
| b)p | истинной |
| c)p | изохорной |
| d)p | мольной |
| e)p | изобарной |
| Вопрос №19 |
Вставьте пропущенное слово: «Количество теплоты, затрачиваемой на нагревание одного килограмма вещества на один градус, называется.... теплоёмкостью»
| a)p | удельной |
| b)p | изохорной |
| c)p | истинной |
| d)p | изобарной |
| e)p | мольной |
| Вопрос №20 |
Укажите обозначение и размерность внутренней энергии в системе СИ:
| a)p | U, Дж/моль |
| b)p | Q, Дж |
| c)p | G, кДж/моль |
| d)p | Н, Дж/моль |
| e)p | S, Дж/моль·К |
| Вопрос №21 |
Какое начало термодинамики формулируется так: «Система находится в термодинамическом равновесии, если температура во всех её частях одинакова»?
| a)p | первое |
| b)p | второе |
| c)p | третье |
| d)p | нулевое |
| Вопрос №22 |
Вставьте пропущенное слово: «Термодинамическое равновесие – это состояние системы, которое характеризуется ….. значением всех параметров в любой части системы»:
| a)p | малым |
| b)p | отрицательным |
| c)p | одинаковым |
| d)p | равным нулю |
| e)p | большим |
| Вопрос №23 |
Закончите фразу: «Все части системы, находящейся в термодинамическом равновесии, имеют одну и ту же …… »:
| a)p | энтропию |
| b)p | плотность |
| c)p | концентрацию |
| d)p | температуру |
| e)p | теплоёмкость |
| Вопрос №24 |
Какой прибор используется для определения тепловых эффектов химических реакций?
| a)p | поляриметр |
| b)p | потенциометр |
| c)p | калориметр |
| d)p | колориметр |
| e)p | вискозиметр |
| Вопрос №25 |
Вставьте пропущенное слово: «Тепловой эффект реакции образования вещества из простых веществ, отвечающих наиболее................ состоянию элементов, называется теплотой образования».
| a)p | твёрдому |
| b)p | простому |
| c)p | мягкому |
| d)p | устойчивому |
| e)p | неустойчивому |
| Вопрос №26 |
Теплота образования какого из приведённых веществ в стандартных условиях равна нулю?
| a)p | CO 2 |
| b)p | H 2 O |
| c)p | HCl |
| d)p | CuSO 4 |
| e)p | H 2 |
| Вопрос №27 |
Вставьте пропущенное слово: «Теплота сгорания – это тепловой эффект реакции …… вещества с образованием высших оксидов элементов, входящих в состав соединения».
| a)p | нейтрализации |
| b)p | гидролиза |
| c)p | восстановления |
| d)p | окисления |
| e)p | разложения |
| Вопрос №28 |
Теплота сгорания каких из веществ-участников реакции CO2 + 4H2 = CH4 + 2H2O(ж) равна нулю:
| a)p | CH 4 |
| b)p | H 2 |
| c)p | CO 2 и H 2 O |
| Вопрос №29 |
Выберите выражение, соответствующее тепловому эффекту экзотермических реакций.
| a)p |  + +
|
| b)p | 
|
| c)p | 
|
| d)p | 
|
| e)p | 
|
| Вопрос №30 |
Выберите выражение, соответствующее тепловому эффекту эндотермических реакций:
| a)p | 
|
| b)p | 
|
| c)p |  + +
|
| d)p | 
|
| e)p | 
|
| Вопрос №31 |
Выберите правильное соотношение между тепловыми эффектами реакции при постоянном давлении и при постоянном объёме:
| a)p | D H = D UR - D nT |
| b)p | D H = D U + D nRT |
| c)p | D H = D URT - D n |
| d)p | D H = D U - D nRT |
| e)p | D H = D UT - D nR |
| Вопрос №32 |
Вставьте пропущенное выражение в формулировке закона Гесса:
“Тепловой эффект химической реакции................. от пути, по которому протекает реакция; он определяется только видом и состоянием исходных веществ и продуктов”
| a)p | зависит |
| b)p | не зависит |
| c)p | отличается |
| d)p | не отличается |
| Вопрос №33 |
Закончите формулировку: «Тепловой эффект химической реакции не зависит от пути процесса, а определяется только видом и состоянием ……»
| a)p | исходных веществ |
| b)p | продуктов реакции |
| c)p | исходных веществ и продуктов реакции |
| Вопрос №34 |
Вставьте пропущенное слово: «Тепловой эффект разложения сложного вещества на более простые равен по абсолютной величине, и …… по знаку тепловому эффекту его образования»:
| a)p | противоположен |
| b)p | не равен |
| c)p | равен |
| Вопрос №35 |
Вставьте пропущенное слово: «Тепловой эффект химической реакции равен разности сумм теплот …… продуктов реакции и сумм теплот …… исходных веществ»
| a)p | плавления |
| b)p | сгорания |
| c)p | нейтрализации |
| d)p | образования |
| e)p | диссоциации |
| Вопрос №36 |
Как изменяется тепловой эффект химической реакции с ростом температуры?
| a)p | увеличивается, если D С > 0 |
| b)p | уменьшается, если 
|
| c)p | увеличивается, если D С < 0 |
| d)p | увеличивается, если 
|
| e)p | не изменяется |
| Вопрос №37 |
Укажите правильное уравнение Кирхгоффа
| a)p | 
|
| b)p | 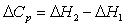
|
| c)p | 
|
| d)p | 
|
| e)p |  + +
|
| Вопрос №38 |
Укажите составляющую интегральной теплоты растворения:
| a)p | энтальпия сгорания |
| b)p | энтальпия разрушения кристаллической решётки |
| c)p | энтропия плавления |
| d)p | энтальпия образования |
| Вопрос №39 |
Укажите правильное математическое выражение второго начала термодинамики:
| a)p | 
|
| b)p | 
|
| c)p | 
|
| d)p |  = h = h
|
| e)p | Q 1 × Q 1 = T 1 × T 2 |
| Вопрос №40 |
Для какого начала термодинамики справедливо утверждение: «Невозможен процесс, единственным результатом которого было бы превращение теплоты в работу»?
| a)p | нулевого |
| b)p | третьего |
| c)p | второго |
| d)p | первого |
| Вопрос №41 |
Какое начало термодинамики формулируется так: «Теплота не может самопроизвольно переходить от более холодного тела к более тёплому»?
| a)p | второе |
| b)p | нулевое |
| c)p | первое |
| d)p | третье |
| Вопрос №42 |
Закончите определение: «Со статистической точки зрения энтропия является мерой..... в системе»
| a)p | беспорядка |
| b)p | количества вещества |
| c)p | порядка |
| d)p | массы |
| e)p | количества теплоты |
| Вопрос №43 |
Закончите определение: «С термодинамической точки зрения энтропия является мерой.....при самопроизвольном процессе»
| a)p | числа компонентов |
| b)p | концентрирования теплоты |
| c)p | рассеяния теплоты |
| d)p | количества вещества |
| e)p | количества теплоты |
| Вопрос №44 |
Вставьте пропущенное выражение: «Энтропия изолированной системы возрастает в необратимом процессе и …… в обратимом процессе»
| a)p | возрастает |
| b)p | уменьшается |
| c)p | не изменяется |
| Вопрос №45 |
Закончите формулировку закона возрастания энтропии: «В системе, не получающей энергии извне, самопроизвольные процессы всегда идут …… »
| a)p | с уменьшением энтропии |
| b)p | до конца |
| c)p | с выделением теплоты |
| d)p | с увеличением энтропии |
| e)p | в обратном направлении |
| Вопрос №46 |
Вставьте пропущенное выражение: «Во всяком самопроизвольном процессе в изолированной системе энтропия при переходе от начального к конечному состоянию ……»
| a)p | стремится к минимуму |
| b)p | уменьшается |
| c)p | стремится к нулю |
| d)p | возрастает |
| e)p | не изменяется |
| Вопрос №47 |
Выберите правильное математическое выражение для расчета энергии Гиббса:
| a)p | G = HS - T |
| b)p | G = HT + S |
| c)p | G = H + TS |
| d)p | G = HS + T |
| e)p | G = H - TS |
| Вопрос №48 |
Выберите правильное математическое выражение для расчета энергии Гельмгольца:
| a)p | A = UT + S |
| b)p | A = US - T |
| c)p | A = US + T |
| d)p | A = U - TS |
| e)p | A = U + TS |
| Вопрос №49 |
Укажите критерий самопроизвольного протекания процесса при изобарно-изотермических условиях:
| a)p | 
|
| b)p | 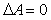
|
| c)p | 
|
| d)p |  + +
|
| e)p | 
|
| Вопрос №50 |
Укажите критерий самопроизвольного протекания процесса при изохорно-изотермических условиях:
| a)p |  + +
|
| b)p | 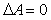
|
| c)p | 
|
| d)p | 
|
| e)p | 
|
| Вопрос №51 |
Укажите условие самопроизвольного протекания процесса в прямом направлении:
| a)p |  G > 0 G > 0
|
| b)p |  G < 0 G < 0
|
| c)p |  G = G =  A= 0 A= 0
|
| d)p |  G = 0 G = 0
|
| Вопрос №52 |
К какому значению стремится энтропия идеального кристалла при приближении температуры к абсолютному нулю?
| a)p | к бесконечно малому |
| b)p | к бесконечно большому |
| c)p | к максимуму |
| d)p | к нулю |
| e)p | к минимуму |
| Вопрос №53 |
Закончите формулировку постулата Планка: «При абсолютном нуле температуры энтропия любого вещества в виде идеального кристалла …… »
| a)p | максимальна |
| b)p | больше нуля |
| c)p | меньше единицы |
| d)p | минимальна |
| e)p | равна нулю |
| Вопрос №54 |
Для какой термодинамической функции можно определить абсолютное значение?
| a)p | внутренняя энергия |
| b)p | энтропия |
| c)p | энтальпия |
| d)p | энергия Гельмгольца |
| e)p | энергия Гиббса |
| Вопрос №55 |
Что должно находиться в числителе выражения для константы равновесия реакции, идущей при постоянном давлении?
| a)p | сумма парциальных давлений продуктов |
| b)p | произведение парциальных давлений исходных веществ |
| c)p | произведение парциальных давлений продуктов |
| d)p | произведение концентраций исходных веществ |
| e)p | произведение концентраций продуктов |
| Вопрос №56 |
Что должно находиться в числителе выражения для константы равновесия реакции, идущей при постоянном объёме?
| a)p | сумма парциальных давлений продуктов |
| b)p | произведение концентраций продуктов |
| c)p | произведение концентраций исходных веществ |
| d)p | произведение парциальных давлений исходных веществ |
| e)p | произведение парциальных давлений продуктов |
| Вопрос №57 |
Какие реакции называются обратимыми?
| a)p | идущие с полным расходованием исходных веществ |
| b)p | идущие одновременно в обоих направлениях |
| c)p | идущие с образованием газообразных веществ |
| d)p | идущие с образованием осадка |
| e)p | идущие с неполным расходованием исходных веществ |
| Вопрос №58 |
Укажите соотношение констант равновесия при постоянном давлении и при постоянном объёме для реакций, идущих без изменения числа молей газообразных веществ:
| a)p | К р = К с |
| b)p | К р < К с |
| c)p | К р > К с |
| d)p | К р ¹ К с |
| e)p | К р = 2К с |
| Вопрос №59 |
Укажите соотношение констант равновесия при постоянном давлении и при постоянном объёме для реакций, идущих с изменением числа молей газообразных веществ:
| a)p | К р = К с (RT) D n |
| b)p | К р = К с (RT) -D n |
| c)p | К р = - К с (RT) D n |
| d)p | К р < К с (RT) D n |
| e)p | К р > К с (RT) D n |
| Вопрос №60 |
Укажите реакции, для которых значения констант равновесия Кс и Кр равны друг другу:
| a)p | идущие без изменения числа молекул |
| b)p | идущие с образованием осадка |
| c)p | идущие до конца |
| d)p | идущие с постоянной скоростью |
| e)p | идущие с изменением числа молекул |
| Вопрос №61 |
Как изменится выход продуктов экзотермической обратимой реакции при нагревании?
| a)p | уменьшится |
| b)p | увеличится |
| c)p | не изменится |
| Вопрос №62 |
Как изменится выход продуктов эндотермической обратимой реакции при нагревании:
| a)p | увеличится |
| b)p | не изменится |
| c)p | уменьшится |
| Вопрос №63 |
Укажите значение изменения энергии Гиббса, отвечающее состоянию равновесия обратимой реакции:
| a)p | максимальное |
| b)p | минимальное |
| c)p | равное нулю |
| Вопрос №64 |
В каком направлении возможно протекание обратимой химической реакции, если работа процесса положительна, а изменение энергии Гиббса отрицательно?
| a)p | в обратном |
| b)p | в прямом |
| c)p | реакция невозможна |
| Вопрос №65 |
В каком направлении возможно протекание обратимой химической реакции, если работа процесса отрицательна, а изменение энергии Гиббса положительно?
| a)p | в обратном |
| b)p | в прямом |
| c)p | реакция невозможна |
| Вопрос №66 |
Укажите практически нерастворимую в воде жидкость:
| a)p | этиловый спирт |
| b)p | серная кислота |
| c)p | уксусная кислота |
| d)p | диэтиловый эфир |
| e)p | ацетон |
| Вопрос №67 |
Укажите неограниченно растворимые друг в друге жидкости:
| a)p | уксусноэтиловый эфир и вода |
| b)p | бензол и вода |
| c)p | ртуть и вода |
| d)p | этиловый спирт и вода |
| e)p | вода и бензин |
| Вопрос №68 |
Какие жидкости ограниченно растворимы друг в друге?
| a)p | вода и анилин |
| b)p | уксусная кислота и вода |
| c)p | масло и вода |
| d)p | ртуть и вода |
| e)p | этанол и вода |
| Вопрос №69 |
Какая система состоит из 3-х компонентов:
| a)p | вода + пар + сахароза |
| b)p | вода + лед + глюкоза + сахароза |
| c)p | вода + лед + глюкоза |
| d)p | вода + лед + пар + сахароза |
| e)p | вода + лед + пар |
| Вопрос №70 |
Сколько фаз присутствует в системе, состоящей из раствора NaOH, льда и водяного пара? (n = 2)
| a)p | |
| b)p | 3 |
| c)p | |
| d)p | |
| e)p |
| Вопрос №71 |
Система состоит из водного раствора КBr в присутствии льда. Укажите для этого случая верный ответ:
| a)p | 1 фаза, 2 компонента |
| b)p | 3 фазы, 1 компонент |
| c)p | 1 фаза, 3 компонента |
| d)p | 2 фазы, 1 компонент |
| e)p | 2 фазы, 2 компонента |
| Вопрос №72 |
Какую величину позволяет вычислить правило фаз Гиббса?
| a)p | внутреннюю энергию |
| b)p | термодинамическую вероятность |
| c)p | температуру |
| d)p | давление |
| e)p | вариантность системы |
| Вопрос №73 |
С помощью правила фаз Гиббса укажите нонвариантную систему (при n = 2):
| a)p | водный раствор KCl + лед |
| b)p | водный раствор NaCl и KCl + водяной пар + лед + кристаллы NaCl и KCl |
| c)p | водный раствор NaCl + кристаллы NaCl |
| d)p | водный раствор NaCl + водяной пар |
| Вопрос №74 |
С помощью правила фаз Гиббса укажите моновариантную систему (при n = 2):
| a)p | водный раствор NaCl + кристаллы NaCl |
| b)p | водный раствор KCl + лед + водяной пар |
| c)p | водный раствор KCl + лед |
| d)p | водный раствор NaCl + водяной пар |
| e)p | водный раствор NaCl и KCl + водяной пар + лед + кристаллы NaCl и KCl |
| Вопрос №75 |
В каких координатах строится диаграмма состояния однокомпонентных систем?
| a)p | V - Т |
| b)p | р - Т |
| c)p | р - состав |
| d)p | Т - состав |
| e)p | р - V |
| Вопрос №76 |
Какой процесс не является фазовым переходом?
| a)p | плавление |
| b)p | химическая реакция |
| c)p | конденсация пара |
| d)p | кристаллизация |
| e)p | испарение |
| Вопрос №77 |
Как в совокупности называются процессы кипения, испарения, возгонки, конденсации пара?
| a)p | химические реакции |
| b)p | охлаждение |
| c)p | нагревание |
| d)p | работа |
| e)p | фазовые переходы |
| Вопрос №78 |
Как в совокупности называются процессы плавления, кристаллизации, отвердевания, конденсации пара, растворения?
| a)p | нагревание |
| b)p | фазовые переходы |
| c)p | охлаждение |
| d)p | работа |
| e)p | химические реакции |
| Вопрос №79 |
Как называется точка на диаграмме состояния воды, отвечающая одновременному существованию льда, воды и пара?
| a)p | точка кипения |
| b)p | точка отвердевания |
| c)p | точка плавления |
| d)p | тройная точка |
| e)p | точка конденсации |
| Вопрос №80 |
Какие фазовые поля разделяет линия плавления на диаграмме состояния воды?
| a)p | воды и пара |
| b)p | льда и пара |
| c)p | льда и воды |
| Вопрос №81 |
Какие фазовые поля разделяет линия кипения на диаграмме состояния воды?
| a)p | воды и пара |
| b)p | льда и воды |
| c)p | льда и пара |
| Вопрос №82 |
Какие фазовые поля разделяет линия возгонки на диаграмме состояния воды?
| a)p | воды и пара |
| b)p | льда и воды |
| c)p | льда и пара |
| Вопрос №83 |
Укажите уравнение закона Рауля для неограниченно смешивающихся жидкостей:
| a)p | p B = p o A X B |
| b)p | p A = p o A X A |
| c)p | p A = p o A X B |
| d)p | p A = p o B X A |
| e)p | p B = p o A X A |
| Вопрос №84 |
Дополните формулировку закона Рауля для растворов нелетучих веществ: “Относительное понижение давления пара растворителя над раствором равно..... растворённого вещества”:
| a)p | массовой доле |
| b)p | молярности |
| c)p | молярной доле |
| d)p | массе |
| e)p | объёмной доле |
| Вопрос №85 |
Вставьте пропущенное слово: «Если растворы двух жидкостей образуются с выделением теплоты, это приведёт к.... отклонениям от закона Рауля»
| a)p | отрицательным |
| b)p | положительным |
| Вопрос №86 |
Вставьте пропущенное слово: «Если растворы двух жидкостей образуются с поглощением теплоты, это приведёт к.... отклонениям от закона Рауля»
| a)p | отрицательным |
| b)p | положительным |
| Вопрос №87 |
Вставьте пропущенное выражение в формулировку закона Дальтона: “Общее давление газа или пара над раствором..... парциальных давлений компонентов”
| a)p | вычитается из |
| b)p | меньше |
| c)p | больше |
| d)p | не зависит от |
| e)p | равно сумме |
| Вопрос №88 |
В каких координатах строится диаграмма кипения?
| a)p | р - V |
| b)p | V - Т |
| c)p | р - Т |
| d)p | Т - состав |
| Вопрос №89 |
Вставьте пропущенное выражение в формулировку первого закона Коновалова: «С увеличением содержания компонента в растворе..... его содержание в парах»
| a)p | остаётся постоянным |
| b)p | увеличивается |
| c)p | уменьшается |
| Вопрос №90 |
Вставьте пропущенное выражение в формулировку первого закона Коновалова: «Пар по сравнению с равновесным раствором обогащён..... компонентом»
| a)p | менее летучим |
| b)p | более летучим |
| Вопрос №91 |
Вставьте пропущенное выражение в формулировку второго закона Коновалова: “Экстремальным точкам на диаграммах состояния бинарных растворов соответствуют растворы, состав которых.... от состава равновесного пара”.
| a)p | заметно отличается |
| b)p | отличается |
| c)p | не отличается |
| d)p | не зависит |
| e)p | мало отличается |
| Вопрос №92 |
Укажите свойство, присущее азеотропам:
| a)p | одинаковые составы пара и раствора |
| b)p | изменение температуры кипения при перегонке |
| c)p | изменение состава пара при перегонке |
| d)p | изменение состава раствора при перегонке |
| Вопрос №93 |
На каком законе основана перегонка жидкостей?
| a)p | Авогадро |
| b)p | Дальтона |
| c)p | 1-м Коновалова |
| d)p | Бойля – Мариотта |
| e)p | 2-м Коновалова |
| Вопрос №94 |
Для чего используется перегонка смесей жидкостей?
| a)p | для концентрирования |
| b)p | для разбавления |
| c)p | для выпаривания |
| d)p | для экстракции |
| e)p | для разделения на компоненты |
| Вопрос №95 |
Какой вид перегонки позволяет выделить из смеси жидкостей в чистом виде оба компонента?
| a)p | простая |
| b)p | перегонка с водяным паром |
| c)p | сложная |
| d)p | фракционная |
| Вопрос №96 |
Каким способом азеотроп можно разделить на составляющие компоненты?
| a)p | простой перегонкой |
| b)p | перегонкой с водяным паром |
| c)p | фракционной перегонкой |
| d)p | химическим связыванием одного из компонентов |
| e)p | ректификацией |
| Вопрос №97 |
Вставьте пропущенное слово: «Отношение концентраций третьего компонента в двух несмешивающихся ж