Классификация
- по числу остатков простейших углеводов – моносахариды - глюкоза (С6Н12О6), фруктоза (С6Н12О6), рибоза (С5Н10О5);
- олигосахариды – сахароза (С12Н22О11), мальтоза (С12Н22О11);
- полисахариды- крахмал(С6Н10О5)n, целлюлоза(С6Н10О5)n,
-по числу атомов углерода – пентозы - рибоза (С5Н10О5);
- гексозы - глюкоза и фруктоза (С6Н12О6),
- по функциональным группам – альдозы (содержат альдегидную группу) – глюкоза
- кетозы (содержат кетонную группу) - фруктоза
ХАРАКТЕРИСТИКА МОНОСАХАРИДА - ГЛЮКОЗЫ
Глюкоза (виноградный сахар) - С6Н1206
- гексоза,
- альдегидоспирт,
- молекулы могут существовать в циклических (α- и β-формах) и линейной формах.
СН2ОН СН2ОН
О О ОН
ОН О
НО ОН ОН НО ОН СН2-СН-СН-СН-СН-С
ОН ОН ОН ОН Н
ОН ОН
α-форма β-форма линейная форма
Химические свойства
| Взаимодействие | Уравнение реакций | Примечание |
| I. Реакции с участием гидроксильных групп (свойства подобные многоатомным спиртам). | 1. Взаимодействие с Сu(ОН)2 на холоде:
O O
СН2ОН-СНОН-СНОН-СНОН-СНОН-С +Сu(ОН)2 → СН2ОН-СНОН-СНОН-СН-СН-С + 2Н2О
H O O Hглюконат меди (II) Cu
темно-синий р-р
2.Реакция этерификации:
О O
СH2ОН-(СНОН)4-С + 5СН3СООН 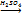 СH2 ─ СН ─С─H + 5Н20
H O O O O
C C
CH3 CH3 4 СH2 ─ СН ─С─H + 5Н20
H O O O O
C C
CH3 CH3 4
| Эту реакцию используют для обнаружения сахара в моче. |
| II. Реакции с участием альдегидной группы (свойства подобные альдегидам). | 1. Окисление - реакция «серебряного зеркала»:
О
СH2ОН-(СНОН)4-С-H + Ag2О 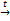 СН2ОН-(СНОН)4-СООН + 2Ag↓
аммиачн. р-p глюконовая кислота
2. Окисление гидроксидом меди (II):
О
СH2ОН-(СНОН)4-С-H + 2Cu(OH)2 СН2ОН-(СНОН)4-СООН + 2Ag↓
аммиачн. р-p глюконовая кислота
2. Окисление гидроксидом меди (II):
О
СH2ОН-(СНОН)4-С-H + 2Cu(OH)2 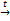 СН2ОН-(СНОН)4-СООН + Сu2O↓ + H2O
красный
3. Восстановление (гидрирование) с образованием шестиатомного спирта (сорбит):
О ОН ОН ОН ОН ОН ОН
СH2ОН-(СНОН)4-С-H + Н2 СН2ОН-(СНОН)4-СООН + Сu2O↓ + H2O
красный
3. Восстановление (гидрирование) с образованием шестиатомного спирта (сорбит):
О ОН ОН ОН ОН ОН ОН
СH2ОН-(СНОН)4-С-H + Н2 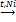 СН2 – СН –СН –СН –СН –СН2
сорбит СН2 – СН –СН –СН –СН –СН2
сорбит
| Качественные реакции - реакции окисления, которые позволяют отличить глюкозу от её изомера - фруктозы |
| III. Специфические свойства глюкозы | 1. реакции брожения (расщепление):
а) спиртовое брожение: С6Н12О6 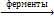 2С2Н5ОН + 2СО2↑
б) молочнокислое брожение: С6Н12О6 2С2Н5ОН + 2СО2↑
б) молочнокислое брожение: С6Н12О6 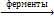 2СН3-СНОН-СООН
молочная к-та
в) маслянокислое брожение: С6Н12Об 2СН3-СНОН-СООН
молочная к-та
в) маслянокислое брожение: С6Н12Об 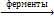 С3Н7-СООН + 2СО2↑ + 2Н2↑
масляная к-та
2. Одна из функций глюкозы в живых организмах — обеспечение их энергией, которая выделяется при ее окислении:
С6Н12О6 + 6О2 → 6СО2 + 6Н2О + 2920 кДж С3Н7-СООН + 2СО2↑ + 2Н2↑
масляная к-та
2. Одна из функций глюкозы в живых организмах — обеспечение их энергией, которая выделяется при ее окислении:
С6Н12О6 + 6О2 → 6СО2 + 6Н2О + 2920 кДж
| Брожение происходит под действием биологических катализаторов — ферментов, вырабатываемых микроорганизмами |
Получение
В природе глюкоза образуется в процессе фотосинтеза:
6СО2 + 6Н2О 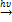 С6Н12О6 + 6О2
С6Н12О6 + 6О2
ХАРАКТЕРИСТИКА ДИСАХАРИДА - САХАРОЗЫ
Сахароза (тростниковый или свекловичный сахар) - С12Н22О11 состоит из остатков глюкозы и фруктозы
СН2ОН ОН
Н О СН2 О
НО ОН О ОН СН2ОН
ОН ОН
Химические свойства сахарозы
1. Сахароза, как и многоатомные спирты, реагирует с гидроксидом меди (II).
2. Сахароза не реагирует с аммиачным раствором оксида серебра, т.к. молекула сахарозы состоит из взаимно связанных остатков циклической глюкозы и циклической фруктозы.
3. Гидролиз протекает в кислой среде:
С12Н22О11 + Н2О 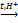 С6Н12О6 + С6Н12О6
С6Н12О6 + С6Н12О6
глюкоза фруктоза (образовавшаяся смесь называется инвертным сахаром, содержится в мёде)
В живых организмах гидролиз идет под действием ферментов.
ХАРАКТЕРИСТИКА ПОЛИСАХАРИДОВ – КРАХМАЛА и ЦЕЛЛЮЛОЗЫ
Крахмал и целлюлоза (клетчатка) – биополимеры, состоящие соответственно из остатков α- и β-форм глюкозы.
Общая формула крахмала и целлюлоза - (С6Н10О5)n, степень полимеризации крахмала 1000-6000, а целлюлозы – 10 000 -14 000.
Получение. В природе крахмал и глюкоза образуется в процессе фотосинтеза: 6nСО2 + 5nН2О 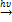 (C6H10O5)n + 6nO2
(C6H10O5)n + 6nO2
Химические свойства
| Взаимодействие | Крахмала | Целлюлозы |
| 1. Горение -реакция полного окисления | (С6Н10О5)n + 6nO2 → 6nСO2 ↑ + 5nH2O | (С6Н10О5)n + 6nO2 → 6nСO2 ↑ + 5nH2O |
| 2. Гидролиз | - протекает легко под действием ферментов или кислот.
(С6Н10О5)n + nH2О 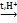 nС6Н12О6
α-глюкоза nС6Н12О6
α-глюкоза
| - протекает в более жестких условиях:
(С6Н10О5)n + nH2О 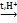 nС6H12О6.
β -глюкоза nС6H12О6.
β -глюкоза
|
| 3. Особые взаимодействия | 1. Качественная реакция на крахмал – Взаимодействие с раствором иода): (С6Н10О5)n + I2 → комплексное соединение интенсивно синего цвета 2. Крахмал не дает реакции «серебряного зеркала». | 1. Реакция этерификации:
[С6Н702(ОН)3]n+3nСН3СООН 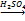 O-CO-CH3
C6H7O2-O-CO-CH3 +3nН2O
O-CO-CH3 n
триацетат целлюлозы
[С6Н702(ОН)3]n+3nНNO3 O-CO-CH3
C6H7O2-O-CO-CH3 +3nН2O
O-CO-CH3 n
триацетат целлюлозы
[С6Н702(ОН)3]n+3nНNO3 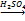 O- NO2
C6H7O2-O-NO2 +3nН2O
O- NO2 n
тринитрат целлюлозы
2. Термическое разложение без доступа воздуха:
(С6Н10О5)n O- NO2
C6H7O2-O-NO2 +3nН2O
O- NO2 n
тринитрат целлюлозы
2. Термическое разложение без доступа воздуха:
(С6Н10О5)n 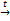 древесный + Н2O + летучие органические
уголь вещества
3. Целлюлоза не дает реакции «серебряного зеркала». древесный + Н2O + летучие органические
уголь вещества
3. Целлюлоза не дает реакции «серебряного зеркала».
|