ТЕМА: КЛАССЫНЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ.
ОКСИДЫ.
Оксиды - это сложные вещества, состоящие из двух элементов, один из которых – кислород.
Классификация оксидов.
1. Несолеобразующие оксиды.
Это оксиды, которые не взаимодействуют ни с кислотами, ни с основаниями и поэтому солей не образуют. Например: CO; NO; N2O
2. Солеобразующие оксиды.
2.1 Основные оксиды.
Это оксиды, которым в качестве гидроксидов соответствуют основания.
Например: Na2O ® NaOH; CaO ® Ca(OH)2.
Как правило, основные оксиды - это оксиды металлов, но есть исключения: ZnO; Al2O3.
2.2 Кислотные оксиды.
Это оксиды, которым соответствуют кислоты. например: SO3 ® H2SO4; P2O5 ® H3PO4.
Как правило, кислотные оксиды - это оксиды неметаллов или металлов в высокой степени окисления.
2.3 Амфотерные оксиды.
Это оксиды, которым соответствуют амфотерные гидроксиды, например: ZnО®Zn(ОН)2; Al2O3 ® Al(OH)3.
Номенклатура оксидов.
СО - оксид углерода (2)
СО2- оксид углерода (4)
Химические свойства оксидов.
1. Химические свойства основных оксидов.
а) с водой, если образуется растворимый гидроксид.
Na2O + H2O ® 2NaOH
б) с кислотами
CaO + 2HCl ® CaCl2 + H2O
в) с кислотными оксидами
СаО + CO2 ® CaCO3
УПРАЖНЕНИЯ:
| CaO + H2O ® | |
| MgO + HNO3 ® | |
| BaO + CO2 ® |
2. Химические свойства кислотных оксидов.
а) с водой
СО2 + Н2О ®Н2СО3
б) со щелочами
CO2 + 2NaOH ® Na2CO3 + H2O
в) с основными оксидами.
СО2 + Na2O®Na2CO3
УПРАЖНЕНИЯ:
| 1 | |
| SО3 + Н2О → | |
| SO3 + NaOH → | |
| SiO2 + MgO → |
3. Химические свойства амфотерных оксидов.
а) с кислотами
ZnO + 2НNO3 → Zn(NO3)2 + Н2О
б) со щелочами
ZnO + 2NaOH → Na2ZnO2 + H2O
ОСНОВАНИЯ.
Основания - это сложные вещества, состоящие из атома металла и одной или нескольких гидроксогрупп.
Номенклатура оснований.
КОН - гидроксид калия
Ва(ОН)2 - гидроксид бария
Fe(OH)2 - гидроксид железа (2)
Fe(OH)3 - гидроксид железа (3)
Классификация оснований.
1. Растворимые основания (щелочи). Например: КОН, Ва(ОН)2
2. Нерастворимые основания. Например: Cu(OH)2, Мn(ОН)2.
Химические свойства щелочей.
1. Взаимодейсвие с кислотами.
2NaOН + H2SO4 ® Na2SO4 + 2H2O
2. Взаимодействие с кислотными оксидами.
2NaOН + СО2 ® Na2СО3 + H2O
3. Взаимодействие с растворами солей.
2NaOН + CuSO4 ® Cu(OH)2↓ + Na2SO4
Химические свойства нерастворимых оснований.
1. Взаимодействие с кислотами.
Cu(OH)2 + 2HNO3 → Cu(NO3)2 + 2H2O
2. Разложение нерастворимых оснований.
Cu(OH)2 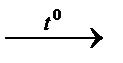 CuO + H2O
CuO + H2O
Взаимодействие амфотерных гидроксидов со щелочами.
H2ZnO2 + 2NaOH → Na2ZnO2 + 2H2O
Zn(OH)2 + 2NaOH → Na2[Zn(OH)4]
УПРАЖНЕНИЯ:
| Ba(OH)2 + HNO3 → | |
Fe(0H)3 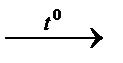
| |
| Ca (OH)2 + CO2 → | |
| КOH + FeCl2 → |
КИСЛОТЫ.
Кислоты - это сложные вещества, состоящие из атомов водорода и кислотного остатка.
Классификация кислот.
1. Кислородсодержащие.
H2SO4 - серная, H2SO3 - сернистая, HNO3 - азотная, Н3РО4 - фосфорная, Н2СО3 - угольная, Н2SiО3 -кремниевая.
2. Бескислородные.
HF -фтороводородная, HCl - соляная, НBr - бромоводородная, НI - иодоводородная, H2S - сероводородная.
Химические свойства кислот.
1. Взаимодействие растворов кислот с металлами (металл должен находиться в ряду напряжений левее водорода).
2HCl + Zn → ZnCl2 + H2↑
2. Взаимодействие с оксидами металлов.
2HCl + MgO → MgCl2 + H2O
3. Взаимодействие с основаниями.
3НCl + Fe(OH)3 → FeCl3 + 3H2О
4. Взаимодействие с солями (если в результате реакции образуется осадок или газ).
2НСl + MgCO3 → MgCl2 + C02↑ + H2О
УПРАЖНЕНИЯ:
| H2SO4 + Al → | |
| HNO3 + Cu(OH)2 → | |
| H3PO4 + CaCl2 → | |
| HCl + Fe2O3 → |
СОЛИ.
Соли - это сложные вещества, состоящие из атомов металла и кислотных остатков.
Классификация солей.
1. Средние (продукт полного замещения атомов водорода в кислоте на металл), например: Na2CO3
2. Кислые (продукт неполного замещения атомов водорода в кислоте на металл), например: NaHCO3
3. Основные (продукт неполного замещения гидроксогрупп в основании на кислотный остаток), например: ZnOHCl.
Химические свойства солей.
1. Взаимодействие с кислотами (если в результате реакции образуется осадок или газ).
К2СО3 + 2НСl → 2KCl + CO2↑ + H2O
2. Взаимодействие со щелочами (если в результате реакции образуется осадок).
FeСl3 + 3NaОН → Fe(ОН)3↓ + 3NaCl
3. Взаимодействие с металлами (металл должен находиться в ряду напряжений левее металла, образующего соль).
CuSО4 + Zn → ZnSO4 + Сu
4. Взаимодействие с другими солями (если в результате реакции образуется осадок).
Ba(NO3)2 + Na2SO4 → BaSO4↓ + 2NaNO3
УПРАЖНЕНИЯ:
| CaCl2 + H3PO4 → | |
| CuSО4 + NaOH → | |
| AlCl3 + AgNO3 → | |
| Zn + Pb(NO3)2 → |