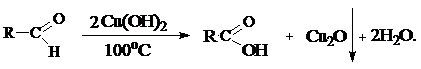Альдегиды
Альдегиды и кетоны представляют собой производные углеводородов, в молекулах которых имеется карбонильная группа (>С=О). Альдегидами называют соединения, у которых карбонильная группа связана с одним или двумя Н–атомами. У кетонов при С-атоме карбонильной группы находятся два углеводородных остатка. Строение альдегидов и кетонов можно представить следующим общими формулами:
 .
.
Общая формула СnH2nO.
Наиболее употребительны тривиальные названия альдегидов, происходящие от соответствующих названий кислот, в которые альдегиды переходят при окислении. Простейший альдегид содержит один атом углерода, он называется муравьиным или формальдегидом (formiga – муравей, лат.).
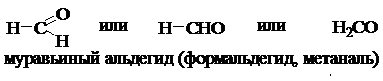
Это единственный альдегид, в котором карбонильная группа связана с двумя H-атомами. Тривиальные и международные названия других альдегидов образуются аналогично:
 По номенклатуре IUPAC названия альдегидов производят от названий нормальных углеводородов, добавляя суффикс «– аль». Выбирая в формуле родовую структуру (главную углеродную цепь), в нее включают С-атом альдегидной группы. Нумерацию цепи начинают с этого С-атома, опуская цифру 1 в названии соединения, поскольку альдегидная группа всегда находится в начале цепи. Например:
По номенклатуре IUPAC названия альдегидов производят от названий нормальных углеводородов, добавляя суффикс «– аль». Выбирая в формуле родовую структуру (главную углеродную цепь), в нее включают С-атом альдегидной группы. Нумерацию цепи начинают с этого С-атома, опуская цифру 1 в названии соединения, поскольку альдегидная группа всегда находится в начале цепи. Например:
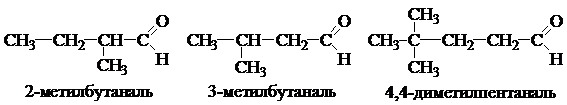
Физические свойства
Первый представитель альдегидов формальдегид – газообразное вещество, ацетальдегид – уже летучая жидкость, следующие гомологи – жидкости. Высшие по числу углеродных атомов – альдегиды – твердые вещества. Формальдегид и ацетальдегид хорошо растворяются в воде, растворимость последующих гомологов постепенно уменьшается. Низшие альдегиды обладают резкими характерными запахами.
Химические свойства
Благодаря наличию в молекулах альдегидов карбонильной группы эти вещества очень активны в химических реакциях.
Восстановление альдегидов (присоединение водорода) возможно при действии молекулярного водорода на твердофазном катализаторе (Ni, Pt, Pd). В зависимости от реагента и его концентрации восстановление может идти либо до спиртов, либо до углеводородов, при этом альдегиды восстанавливаются в первичные спирты.
Реакции окисления альдегидов протекают уже при действии мягких окислителей (и даже кислорода воздуха), образуя карбоновые кислоты без изменения числа углеродных атомов:
[ 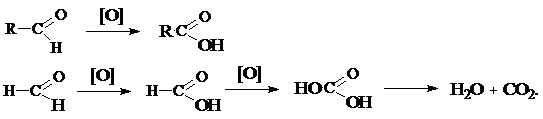
Муравьиный муравьиная угольная
альдегид кислота кислота
Качественная реакция на альдегиды с аммиачным раствором оксида серебра:
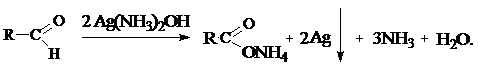
В качестве реактива берут бесцветный раствор оксида серебра в водном аммиаке, содержащий комплексное соединение [Ag(NH3)2]OH. При нагревании его с альдегидом, а иногда и на холоде, выпадает серебро, образующее на поверхности стеклянного сосуда зеркальный слой (реакция серебряного зеркала).
Другим широко применяемым для анализа альдегидов реагентом является гидроксид меди (II) голубого цвета – Cu(OH)2, который при нагревании окисляет альдегиды, восстанавливаясь до закиси меди, выпадающей в виде кирпично-красного осадка: