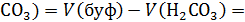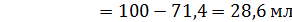1. Значение рН внеклеточной среды 7,4, а внутриклеточной – 6,9. Где больше концентрация Н+ и во сколько раз?
Краткое изложение задачи:
рНover7,4
рНinter6,9
Решение: Уже из условий задачи понятно, что концентрация Н+ внутри клетки больше, чем внеклеточная: [Н+]inter > [Н+]over. Убедимся в этом с помощью расчетов. Исходя из определения рН, выведем формулу для расчета [Н+].
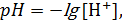 отсюда
отсюда 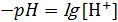 и
и 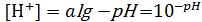
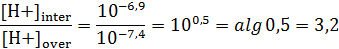
Ответ: концентрация Н+ внутри клетки больше внеклеточной в 3,2 раза.
2. Рассчитать рН буферного раствора, состоящего из 50 мл 0,1э раствора СН3СООН и 100 мл 0,2э СН3СООNa. рКа(СН3СООН/СН3СОО−)=4,8.
Краткое изложение задачи: Решение:
|
V(СН3СООН)=50 мл
Сэ(СН3СООН)=0,1 моль/л
V(СН3СООNa)=100 мл
Сэ(СН3СООNa)=0,2 моль/л
рКа(СН3СООН/СН3СОО−)=4,8.
Ответ: рНацетатного буфера=5,4
3. Какие объемы компонентов бикарбонатного буфера с одинаковой исходной концентрацией нужно взять, чтобы получить 100 мл буферного раствора с рН 6,0. 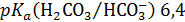 при 25℃.
при 25℃.
|
V(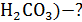
V(NaH 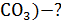 )
)
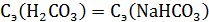
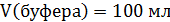
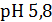
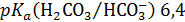
Ответ: V(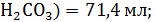 V(NaHC
V(NaHC 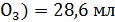
4. К 25 мл ацетатного буфера с рН 4,3 прибавили 5,0 мл 0,1э HCl, что привело к снижению рН до 3,7. Рассчитать буферную емкость по кислоте.
Краткое изложение задачи:
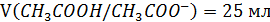
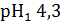
V(HCl)=5,0 мл
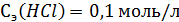
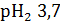 Решение:
Решение:
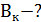

Ответ: Вк = 0,033 моль/л
5. 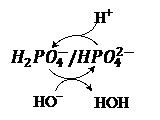 Показать механизм действия фосфатного буфера.
Показать механизм действия фосфатного буфера.
Ответ:
Защита от кислоты:
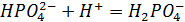 (в ионном виде)
(в ионном виде)
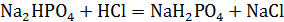
Защита от щелочи:
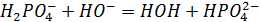 (в ионном виде)
(в ионном виде)
Na 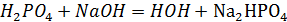
6. Какое нарушение КОР у больного, если рНкрови7,1 а 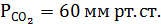 Каковы причины такого нарушения?
Каковы причины такого нарушения?
Ответ: Сравним: в норме рНкрови7,4, а 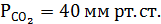
Понижение рНкрови до 7,1 при нарушенном парциальном давлении свидетельствует о респираторном ацидозе. Причем, исходя из уравнения Гендерсона-Гассельбаха для бикарбонатного буфера (см. выше), мы видим четкую причинно-следсвенную связь: повышение парциального давления углекислого газа приводит к снижению рН. Дальнейшие действия врача – дифференцировать патологию органов дыхания и угнетение дыхательного центра.
|
|
7. Какое нарушение КОР у больного, если рНкрови7,1 а 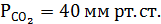
Каковы причины такого нарушения?
Ответ: Сравним: в норме рНкрови7,4, а 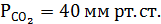
Понижение рНкрови до 7,1 при нормальном парциальном давлении свидетельствует о метаболическом ацидозе. Причем, исходя из буферного уравнения Гендерсона-Гассельбаха (см. выше), можно предположить, что причиной ацидоза, по всей видимости является снижение щелочного резерва крови, в частности – бикарбонатов, гидрофосфатов. Дальнейшие действия врача – дифференцировать патологию органов пищеварения, кровообращения и почек.
8. Какое нарушение КОР можно предположить, если рНкрови7,4,
а 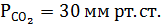
Ответ: Сравним: в норме рНкрови7,4, а 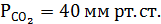
Отсутствие изменений рНкрови при пониженном парциальном давлении свидетельствует о компенсированном ацидозе. По-видимому, за счет увеличения вентиляции легких и, таким образом, снижения содержания кислых компонентов удается компенсировать недостаток бикарбонатов, дигидрофосфатов. Тем самым, соотношение основных и кислых компонентов крови поддерживается постоянным. Дальнейшие действия врача – выяснить причину снижения щелочного резерва организма (дифференцировать патологию органов пищеварения, кровообращения и почек).
Тестированный контроль
|
|
1. Гидрокарбонатный буфер представлен сопряженной кислотно-основной парой
1) H2CO3/CO2
2) H2CO3/HC 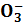
3) H2CO3/C 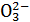
4) HC 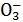 / C
/ C 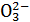
2. Фосфатный буфер представлен сопряженной кислотно-основной парой
1) H2P 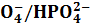
2) 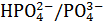
3) 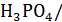 H2P
H2P 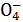
4) H2P 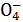 /
/ 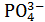
3. Для поддержания нейтральной среды лучше приготовить буфер
1) ацетатный, рКа4,75
2) гидрокарбонатный, рКа6,4
3) фосфатный, рКа6,8
4) аммиачный, рКа9,2
4. Буфер, приготовленный смешением равных объемов 0,1М растворов ацетата натрия и уксусной кислоты (Ка=1,8∙ 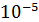 ) поддерживает рН
) поддерживает рН
1) 4,0
2) 4,75
3) 5,0
4) 5,34
5. Для изменения рН от 7,36 до 7,0 потребовалось к 100 мл буфера прилить 36 мл 0,05э раствора HCl. Буферная емкость по кислоте составила в моль/л
1) 0,05
2) 0,5
3) 0,25
4) 0,01
6. При разбавлении водой буфера в 10 раз его буферная емкость
1) увеличилась в 5 раз
2) уменьшилась в 5 раз
3) не изменилась
4) уменьшилась в 10 раз
5) увеличилась в 10 раз
7. При разбавлении водой буфера в 10 раз его значение рН
1) увеличилось в 5 раз
2) уменьшилось в 5 раз
3) не изменилось
4) уменьшилось в 10 раз
5) увеличилось в 10 раз
8. Значение рН буферной смеси, приготовленной из 5 мл 0,1э NH3∙H2O и
9 мл 0,1 э NH4Cl (Кb1,8∙ 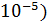 равно
равно
1) 8,7
2) 5,0
3) 13,2
4) 9,0
9. Чтобы получить буферный раствор с рН 7,4, надо смешать 0,5М растворы дигидрофосфата натрия и гидрофосфата натрия (рКа6,8) в соотношении
1) 4:1
2) 1:4
3) 2:1
4) 1:2
10. Чтобы получить 2,6 л фосфатного буфера с рН7,0, надо смешать 0,1М растворы NaH2PO4 и Na2HPO4 в объемах
1) 1,6л и 1л
2) 1,3л и 1,3л
3) 1л и 1,6л
4) 2л и 0,6л
11. Если значение рН крови 7,4 при 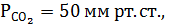 то у больного можно предположить нарушение КОР
то у больного можно предположить нарушение КОР
1) компенсированный алкалоз
2) компенсированный ацидоз
3) метаболический алкалоз
|
|
4) метаболический ацидоз
12. Если у больного значение рН крови 7,0, а 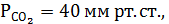 то можно предположить нарушение КОР
то можно предположить нарушение КОР
1) дыхательный ацидоз
2) метаболический ацидоз
3) метаболический алкалоз
4) дыхательный алкалоз
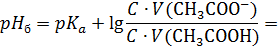 = 4,8 +
= 4,8 + 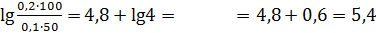
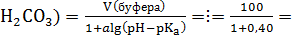

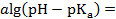
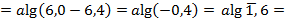
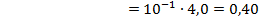 V(NaH
V(NaH