Средства коррекции иммунных реакций.
Из большой группы гипериммунных реакций или заболеваний наиболее обстоятельно изучен патогенез и определены подходы к лечению остро протекающих а л л е р г и й н е м е д л е н н о г о т и п а, связанных с гуморальным иммунитетом. При иммунных реакциях замедленного типа за симптомами гипериммунного ответа обычно скрываются нарушения внутрисистемной регуляции на уровне клеточного иммунитета и дефицит какого-либо из механизмов. Реакцию системы рассматривают как патологическую, если она ведет к различным острым и хроническим заболеваниям, аутоиммунной агрессии, отторжению трансплантата. С практической точки зрения целесообразно выделить три группы средств, применяемых для лечения иммунных заболеваний:
1) противоаллергические средства;
2) иммунодепрессанты (иммуносупрессоры);3) иммуностимулирующие средства.
Последние две группы предназначены в основном для лечения реакций замедленного типа.
Противоаллергические средства
Конкурентные или функциональные антагонисты медиаторов аллергии, а также вещества, способные тормозить высвобождение медиаторов аллергии тучными клетками; имеют особое значение в терапии острых аллергических реакций немедленного типа.
Гипериммунные реакции немедленного (анафилактического) типа вызываются антигенами и представляют собой патологически измененную форму гуморального иммунного ответа. В качестве антигена могут выступать многие вещества. В крови вполне здоровых людей обнаруживаются антитела ко многим антигенам, создающие потенциальную возможность возникновения аллергии немедленного типа при встрече с этими или химически близкими антигенами. Причины превращения защитной реакции в патологическую неизвестны; определенное значение имеют наследственные факторы.
Взаимодействие фиксированных на тучных клетках антител с циркулирующими антигенами включает механизм «взрывного» освобождения медиаторов аллергии (рис.1).
В наибольшем количестве тучные клетки (они называются так из-за большого количества гранул) обнаруживаются в окружающей вены соединительной ткани легких, кожи, миндалин, в слизистой носоглотки, кишечника. Именно эти органы обычно являются «воротами» для экзогенных антигенов, и в них чаще всего возникают проявления аллергии немедленного типа: бронхоспазм и бронхиальная астма, ринит, конъюнктивит, дерматит, крапивница и различные сыпи, отек Квинке, понос, энтерит, колит, спазм желудка и кишечника и др. Наиболее опасное для жизни и стремительно нарастающее проявление аллергии — анафилактический шок, сопровождающийся падением АД, ослаблением сердечной деятельности, затруднением дыхания из-за бронхоспазма. Все эти патологические состояния обусловлены либо прямым действием медиаторов аллергии на гладкомышечные клетки органов, сосудистую стенку, либо индукцией ими аллергического воспаления.
Лекарственные средства, предназначенные для лечения и профилактики аллергий немедленного типа, могут оказывать действие несколькими путями:
— вступать в конкуренцию с основными медиаторами аллергии — гистамином и лейкотриенами — за их рецепторы на клеточных мембранах (антигистаминные и антилейкотриеновые средства); антагонисты к другим медиаторам аллергии (брадикинину и др.) находятся в стадии разработки;
— тормозить высвобождение из тучных клеток медиаторов аллергии (стабилизаторы мембран тучных клеток);
— активировать физиологические реакции организма, противоположные тем, которые вызываются медиаторами аллергии (функциональные антагонисты медиаторов аллергии).
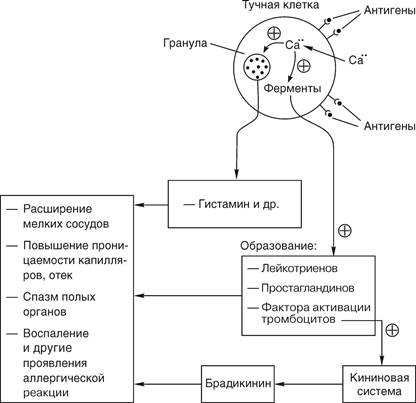
Рис. 1. Схема патогенеза аллергической реакции немедленного типа
ГИСТАМИН. АНТИГИСТАМИННЫЕ СРЕДСТВА
Гистамин относится к числу наиболее активных биологических веществ, и его участие в аллергических реакциях немедленного типа довольно универсально. По этой причине, а также потому, что на пути создания его антагонистов был достигнут наибольший успех, антигистаминные средства нашли широкое применение в практике.
H1-антигистаминные средства. Многочисленные препараты этой группы различаются по силе и продолжительности противогистаминного действия, способности проникать в ЦНС и оказывать седативный эффект, наличию сопутствующей М-холиноблокирующей активности. По этим свойствам они разделяются на препараты I и II поколения. Новые препараты II поколения отличаются от препаратов I поколения большей активностью, более избирательным действием на H1-гистаминовые рецепторы, отсутствием влияния на ЦНС, более длительным действием.
Фармакологические эффекты H1-антигистаминных средств многогранны и определяются ролью гистамина в патогенезе расстройств.
1. Н1-антигистаминные препараты обладают частичным антагонизмом по отношению к сосудорасширяющему действию гистамина — полный антагонизм наблюдается лишь при комбинировании Н1- и Н2-антигистаминных средств. Антагонизм проявляется в большей мере к местным сосудистым реакциям на гистамин при аллергии, воспалении, чем к системным (например, к острому снижению АД при анафилактическом шоке, которое не поддается достаточно быстрой и надежной коррекции антигистаминными препаратами, так как в развитии гипотонии участвуют и другие сосудорасширяющие факторы аллергии).
2. Препараты стабилизируют проницаемость сосудистой стенки, в частности капиллярной, уменьшают выход жидкой части крови в ткани. Это их свойство более выражено при местном применении (например, в каплях) и при повышенной проницаемости аллергической или воспалительной (меньше) природы.
3. Препараты этой группы предупреждают и снимают бронхоспазм, индуцированный гистамином. Вместе с тем они не проявляют заметного лечебного действия при бронхоспазме аллергической природы, так как в его происхождении ведущая роль принадлежит другим медиаторам аллергии (особенно лейкотриенам).
4. Многим препаратам группы присуща дополнительно местноанестезирующая и М-холиноблокирующая активность. Последняя может стать причиной тахикардии, сухости во рту, задержки отделения мокроты, затруднения мочеотделения у больных с гипертрофией простаты, повышения внутриглазного давления. Способность антигистаминов снимать зуд и боль при укусах кровососущих насекомых отмечается как при местном нанесении препаратов в виде мази, так и при пероральном приеме. Противозудное действие препаратов обусловлено не местноанестезирующим эффектом, а антигистаминными свойствами.
5. Центральное действие противогистаминных средств носит (в терапевтических дозах) угнетающий характер. Оно проявляется особенно сильно у препаратов I поколения (прометазин, дифенгидрамин, хлоропирамин и др.) в виде умеренного седативного и снотворного эффектов, что может иметь самостоятельное терапевтическое значение. Хлоропирамин, прометазин и дифенгидрамин назначают в качестве «легких» снотворных средств, используют в успокаивающих микстурах, в составе премедикации перед наркозом. Однако при амбулаторном назначении большинства антигистаминов с целью лечения аллергических заболеваний нужно учитывать возможность замедления психомоторных реакций, ухудшения пространственной координации движений, появления сонливости. Поэтому людям, профессия которых требует непрерывного внимания и быстрой реакции (водители, операторы, рабочие высотных профессий), амбулаторное лечение такими противогистаминными препаратами противопоказано. С осторожностью можно назначать лишь мебгидролин, хифенадин ипрепараты II поколения — лоратадин и др.
Показания к применению Н1-антигистаминных препаратов:
1) аллергические реакции немедленного типа, в патогенезе которых гистамину принадлежит важная роль, — крапивница, аллергические риниты, ангионевротический отек (совместно с альфа-адреномиметиками), кожный зуд, аллергические сыпи, нейродермит. Применять можно любой препарат с учетом противопоказаний, связанных с седативным и М-холиноблокирующим действием;
2) затруднение засыпания, беспокойство; прометазин, дифенгидрамин можно назначать либо каждый отдельно, либо в комбинации со снотворными (в сниженной дозе), с растительными седативными средствами в микстурах;
3) как составной элемент премедикации перед наркозом и операцией — дифенгидрамин, хлоропирамин, прометазин;
4) для профилактики кинетозов — дифенгидрамин, реже (из-за более выраженного седативного эффекта) — прометазин;
5) как элемент комплексного лечения бронхиальной астмы, анафилактического шока, острого отека легких;
6) для предупреждения нежелательных эффектов гистамина, освобождающегося при использовании лекарственных веществ — его либераторов («высвободителей») — морфина и др., особенно у больных с имеющейся сенсибилизацией к каким-либо средствам; лечение лекарственных аллергий;
7) для предупреждения и устранения нежелательных гистаминовых эффектов при обширных травмах кожи и мягких тканей — ожогах, размозжениях и т. п.;
8) для потенцирования действия неопиоидных анальгетиков (метамизола натия и др.) при болевом синдроме в послеоперационном периоде — применяют димедрол или другие препараты.
Побочные эффекты антигистаминных препаратов связаны с их М-холиноблокирующими свойствами (сухость во рту, запоры, тахикардия, нарушение зрения и др.) или седативным действием (сонливость, ухудшение внимания и работоспособности). Дифенгидрамин проявляет несильное ганглиоблокирующее действие, которое при парентеральном введении у людей с дефицитом ОЦК ведет к снижению АД или усиливает имеющуюся гипотонию. Прометазин (производное фенотиазина) также понижает АД, но за счет дополнительного альфа1-адреноблокирующего действия. Многие препараты (особенно мебгидролин, прометазин) при приеме внутрь раздражают желудок и вызывают диспептические явления (тошноту, рвоту). У детей при передозировке антигистаминных препаратов I поколения (дифенгидрамин) могут возникать возбуждение и судороги. Дифенгидрамин повышает судорожную готовность мозга, вследствие чего может провоцировать судорожный припадок у пациентов, страдающих эпилепсией, энцефалопатией, и поэтому противопоказан таким больным. Иногда наблюдается аллергия к антигистаминным препаратам (особенно при их местном применении).
Препараты II поколения (цетиризин, лоратадин) в терапевтических дозах практически не обладают седативным и М-холиноблокирующим действием, их можно назначать в тех случаях, когда угнетающее действие на ЦНС не является желательным (небольшое снижение внимания и слабый седативный эффект наблюдаются у 5—7 % пациентов). Лоратадин и дезлоратадин являются высокоэффективными и продолжительно действующими препаратами, применяются 1 раз в день, хорошо переносятся больными.
СТАБИЛИЗАТОРЫМЕМБРАН ТУЧНЫХ КЛЕТОК
К современным средствам систематической терапии ряда аллергических реакций немедленного типа относятся средства, стабилизирующие мембраны тучных клеток и тормозящие высвобождение из них медиаторов аллергии (гистамина, лейкотриенов, простагландинов и др.), участвующих в развитии аллергических явлений и воспаления. Таким свойством обладают кромоглициевая кислота (интал), недокромил (тайлед) и кетотифен (задитен). Действие препаратов основано на предупреждении входа кальция в тучную клетку, в результате чего тормозится дегрануляция и выброс медиаторов аллергии. Эффект препаратов исключительно профилактический.
Кромоглициевая кислота (интал) плохо всасывается (не более 10 %) из ЖКТ, ее применяют для лечения бронхиальной астмы (но не купирования приступа) ингаляционным способом с помощью особого ингалятора (спинхалера). Ингалятор заряжается специальной капсулой, содержащей 20 мг тонкодисперсного порошка (на 1 ингаляцию). Выпускается также в виде дозированного аэрозоля. Лечебный эффект развивается постепенно — через 2 нед. и более при четырехкратной ингаляции в сутки. Препарат предупреждает 90 % приступов в течение 2 ч после каждой ингаляции и порядка 50 % через 5 ч. При тяжелом течении астмы делают 6—8 ингаляций в сутки. Достоинством препарата является хорошая переносимость, хотя сама процедура ингаляции неприятна для многих больных (нередко возникает кашель и кратковременный бронхоспазм).
Кромоглициевая кислота применяется также для лечения аллергических ринитов (назальный спрей), конъюнктивитов (глазные капли), энтеритов и других кишечных проявлений аллергии.
Недокромил (тайлед) по своим свойствам близок к кромоглициевой кислоте. Применяется для профилактики приступов бронхоспазма у больных бронхиальной астмой ингаляционно в виде аэрозоля. В начале лечения назначают 4 ингаляции в сутки, при достижении терапевтического эффекта переходят на поддерживающую дозу — 2 ингаляции в сутки. Переносится лучше, чем кромоглициевая кислота.
Кетотифен (задитен), кроме торможения выброса из тучных клеток медиаторов аллергии, обладает умеренным прямым Н1-антигистаминным действием и подавляет реакцию на уже высвободившийся гистамин. Препарат хорошо всасывается из ЖКТ и проникает во все ткани; назначается чаще внутрь в виде капсул или таблеток. Применяется не только при бронхиальной астме (для предупреждения приступов), но и при аллергических ринитах, конъюнктивитах, дерматитах, пищевой аллергии и т. п. Стойкий терапевтический эффект наступает только через 10—12 нед. ежедневного приема (по 1 мг 2 раза в день). Переносится хорошо, иногда наблюдается сонливость, повышение аппетита.
Тормозящее влияние на высвобождение медиаторов аллергии (помимо других фармакологических свойств) оказывают также теофиллин и его пролонгированные препараты (теопэк и др.), ингаляционные глюкокортикоиды (будесонид, беклометазон, флутиказон), бета2-адреномиметики (сальбутамол). Их назначение для систематического лечения бронхиальной астмы позволяет защитить бронхи от спазмогенного действия медиаторов аллергии.
Иммунодепрессанты
Препараты, угнетающие вызванные антигеном коопертивные реакции иммунных клеток, пролиферацию лимфоцитов, синтез антител; применяются для лечения тяжелых аутоиммунных заболеваний и подавления реакции отторжения трансплантата.
Иммунодепрессанты (иммуносупрессоры) применяются в качестве средств патогенетической терапии тяжелых проявлений гипериммунных реакций, связанных с к л е т о ч н ы м и м м у н и т е т о м. Основная область их использовния — лечение ревматических заболеваний (коллагенозов): ревматоидного артрита, системной красной волчанки, узелкового периартериита, склеродермии; иммунных поражений ЦНС, почек и других аутоиммунных заболеваний; ряд препаратов применяется в хирургии для профилактики отторжения трансплантата при пересадке органов и тканей.
Действие иммунодепрессивных препаратов направлено на ключевые этапы клеточного иммунного ответа замедленного типа, поэтому они дают ощутимый терапевтический эффект.
Умеренное иммунодепрессивное действие оказывают следующие препараты («малые иммунодепрессанты»):
1) хлорохин (хингамин) и гидроксихлорохин (плаквенил);
2) пеницилламин (купренил). Применявшиеся ранее в качестве иммунодепрессантов препараты золота в настоящее время не используются.
Более сильным иммунодепрессивным эффектом («большие иммунодепрессанты») обладают:
1) цитостатики — азатиоприн (имуран), метотрексат, циклофосфамид;
2) циклоспорин (сандиммун);
3) глюкокортикоиды (преднизолон и др.);
4) моноклональные антитела — базиликсимаб, инфликсимаб и др.
Иммунодепрессанты весьма токсичны и используются лишь при гипериммунных реакциях (различных аутоиммунных заболеваниях и др.) с тяжелым и средней тяжести течением, когда возможности иной терапии исчерпаны, а риск прогрессирования болезни превосходит риск иммуносупрессии. Назначение иммунодепрессантов производится только специалистом в соответствующей области медицины.
«Малые иммунодепрессанты» — хлорохин и гидроксихлорохин (описаны как противомалярийные средства в соответствующем разделе) — препараты успешно применяются для лечения ревматоидного артрита, системной красной волчанки и других коллагенозов. Высокая эффективность препаратов при вялотекущих хронических воспалительных заболеваниях соединительной ткани аутоиммунной природы (коллагенозах) определяется их способностью подавлять клеточный и гуморальный иммунный ответ на разных этапах, а также воспалительный процесс преимущественно в фазе пролиферации.
Хлорохин и гидроксихлорохин стабилизируют лизосомальные и клеточные мембраны, подавляют фагоцитарную функцию макрофагов, уменьшают секрецию ИЛ-1 макрофагами и ИЛ-2 Т-лимфоцитами-помощниками, угнетают пролиферацию Т-лимфоцитов, а также клеток соединительной ткани в ревматических очагах, нарушают образование коллагена.
Пеницилламин способен прямо взаимодействовать с ревматоидным фактором и разрушать его; кроме того, он нарушает созревание коллагена, замедляет пролиферацию Т-лимфоцитов, образует комплексы с двухвалентными металлами (медь, железо, цинк, марганец и др.). Комплекс с медью нейтрализует активные радикалы кислорода, поддерживающие аутоиммунные процессы и воспаление. Многое в механизме иммунодепрессивного и противовоспалительного действия препаратов остается неясным.
При ревматоидном артрите хлорохин и гидроксихлорохин несколько уступают по эффективности пеницилламину, но они менее токсичны и применяются при широком спектре ревматических заболеваний. Назначают их внутрь в таблетках. Терапевтический эффект развивается через 10—12 нед. ежедневного приема; лечение должно быть длительным (не менее 6 мес., обычно 1—2 года).
Пеницилламин — одно из наиболее активных базисных средств терапии ревматоидного артрита. Наилучшие результаты отмечены у больных с высокой скоростью синтеза коллагена и повышенным уровнем специфических антител в плазме. Назначается внутрь в капсулах по индивидуальным схемам; эффект достигает терапевтического пика спустя 9—15 мес. Пеницилламин относится к токсичным препаратам — может вызывать нарушение вкуса, тошноту, рвоту, понос, зуд, покраснение кожи, повышение температуры, нарушение функции почек.
«Большие иммунодепрессанты» применяются для лечения тяжелых, не поддающихся лечению другими препаратами форм ревматоидного артрита, системной красной волчанки, других коллагенозов и аутоиммунных заболеваний; некоторые препараты используются для предупреждения реакции отторжения трансплантата после пересадки органов.
Препараты из группы цитостатиков (азатиоприн, метотрексат, циклофосфамид) блокируют клеточное деление, в том числе Т- и В-лимфоцитов, тормозят синтез белков, включая антитела. Эти эффекты достигаются:
— в результате конкуренции с естественными пуриновыми основаниями ДНК и РНК (азатиоприн) и вытеснением их из биосинтеза;
— в результате антагонизма по отношению к фолиевой кислоте (метотрексат), принимающей участие в синтезе пуриновых и пиримидиновых нуклеотидов;
— «сшивками» спиралей ДНК в клетках (циклофосфамид) с нарушением процесса редупликации ДНК и клеточного деления.
Влияние препаратов этого ряда на разные этапы клеточного и гуморального иммунных ответов несколько различается. Лечебный эффект при лечении ревматических и других аутоиммунных заболеваний развивается довольно медленно и достигает пика спустя 1/2—2 года от начала терапии.
Принципиальными недостатками этих иммунодепрессантов являются:
1) общий цитотоксический эффект в отношении тканей с высоким темпом физиологической регенерации — они подавляют кроветворение и вызывают лейкопению, тромбоцитопению, анемию; нарушают регенерацию слизистой ЖКТ
(изъязвление ЖКТ);
2) выраженное подавление иммунитета — противовирусного, противогрибкового, антибактериального и др. Довольно высока токсичность этих препаратов в отношении печени и почек.
Циклофосфамид, кроме того, чаще других препаратов вызывает бесплодие, обратимое выпадение волос, тошноту и рвоту.
Целесообразно сочетание таких иммунодепрессантов (со снижением дозировок) с НПВС (диклофенаком и др.), глюкокортикоидами, хлорохином. При этом удается добиться лучшей переносимости препаратов. Одновременно отмечается более сильное подавление местных иммуновоспалительных процессов в суставах, коже, почках.
Азатиоприн — наиболее эффективный и менее токсичный иммунодепрессант, в большей степени подавляет Т-лимфоциты, чем В-лимфоциты, иногда применяется для подавления реакции отторжения трансплантата (тканевой несовместимости) при пересадке органов.
К метотрексату более чувствительны В-лимфоциты, он сильнее нарушает образование антител, в малых дозах проявляет в большей степени противовоспалительный эффект, чем иммунодепрессивный. Метотрексат и циклофосфамид являются также активными противоопухолевыми средствами.
Циклоспорин (сандиммун) считается иммунодепрессантом нового поколения, представляет собой антибиотик — циклический полипептид, состоящий из 11 аминокислот. Особенностью препарата является обратимое и избирательное угнетение клеточного иммунного ответа на ранних этапах. Он подавляет способность Т-лимфоцитов-помощников продуцировать ИЛ-2. В результате этого Т-клетки остаются в состоянии покоя, не образуются активные клоны Т-лимфоцитов, в первую очередь цитотоксических Т-киллеров, убивающих чужеродные в иммунном отношении клетки пересаженных тканей. В отличие от цитостатиков, циклоспорин не подавляет кроветворение, пролиферацию клеток слизистой ЖКТ и других тканей. Применяется в основном для профилактики отторжения трансплантата после пересадки костного мозга, почки, печени, сердца и других органов; возможно использование и при аутоиммунных заболеваниях.
Препарат начинают вводить внутривенно капельно за 4—12 ч до операции трансплантации (при пересадке костного мозга исходную дозу вводят накануне операции). Продолжают внутривенные инъекции в течение 2 нед. Затем переходят на пероральную поддерживающую терапию. Дозировки устанавливают индивидуально. Иногда комбинируют с глюкокортикоидами или другими иммунодепрессантами. Циклоспорин обладает довольно высокой нефротоксичностью, может нарушать функцию печени.
Глюкокортикоиды. Гормоны надпочечников и их синтетические аналоги (преднизолон, дексаметазон и др.) обладают выраженным и многосторонним иммунодепрессивным действием, которое может быть целью применения препаратов или крайне нежелательной и опасной побочной реакцией.
Глюкокортикоиды подавляют функцию макрофагов, пролиферацию Т- (в большей степени) и В-лимфоцитов, тормозят их миграцию из мест формирования (тимус, костный мозг) в кровь. Слабее других иммунодепрессантов угнетают кооперативный иммунный ответ и продукцию ИЛ-2. Снижают цитотоксичность Т-киллеров. В больших дозах подавляют синтез иммуноглобулинов плазматическими клетками. Глюкокортикоиды обладают мощным и быстро развивающимся противовоспалительным действием, которое вносит существенный вклад в лечебный эффект при аутоиммунных процессах.
Применяют глюкокортикоиды в качестве иммунодепрессантов при ревматоидных и других аутоиммунных заболеваниях, при пересадке органов и тканей для предупреждения отторжения трансплантата.
В качестве средства, блокирующего реакцию отторжения при пересадке почки, разработан и используется в трансплантологии препарат базиликсимаб, представляющий собой моноклональные антитела, которые избирательно взаимодействуют с рецепторами ИЛ-2 на Т-лимфоцитах человека и инактивируют их, вследствие этого тормозятся пролиферация Т-лимфоцитов, образование и активация Т-киллеров. Применяется базиликсимаб для предупреждения отторжения трансплантата. Получение подобных препаратов достаточно сложно, и они слишком дороги для того, чтобы рассматривать их как средства широкого применения.