ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Измерения электрической проводимости растворов производят с помощью приборов, называемых кондуктометрами. Методика выполнения измерений описана в инструкции, прилагаемой к используемому прибору.
Любые исследования, основанные на измерении электрической проводимости, объединяются под названием кондуктометрии. Кондуктометрические методы применяются для изучения свойств как сильных, так и слабых электролитов.
РАБОТА № 1
ИЗМЕРЕНИЕ УДЕЛЬНОЙ ЭЛЕКТРОПРОВОДНОСТИ РАСТВОРОВ СИЛЬНЫХ ЭЛЕКТРОЛИТОВ
Цель работы: определение предельной молярной проводимости и коэффициентов проводимости сильных электролитов.
Электролит: CH3COONa
| Молярная концентрация раствора C, моль/м3 | 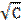
| Удельная проводимость σ* 104,См/м | Эквивалентная проводимость Λ*104, См*м2/моль | Λ0 | 
| A |
| 0,196 | ||||||
| 0,01 | 0,1 | 0,5535 | 55,35 | 0,00911 | 0,6076 | 0,0358 |
| 0,1 | 0,3162 | 1,439 | 14,39 | 0,1580 | 0,0243 | |
| 8,059 | 8,059 | 0,0885 | 0,0083 | |||
| 3,1623 | 51,65 | 5,165 | 0,0567 | 0,0027 | ||
| 270,5 | 2,705 | 0,0297 | 0,0009 |
1. Постройте график 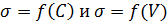 .
. 

2. Рассчитайте эквивалентную электрическую проводимость каждого раствора: 
3. Постройте график  . Путем экстраполяции определите Λ0.
. Путем экстраполяции определите Λ0.

 0,0079
0,0079
4. Рассчитайте значение  по закону независимого движения ионов исходя из предельных подвижностей.
по закону независимого движения ионов исходя из предельных подвижностей.

5. Сравните Λ0 найденное графически, с теоретическим.


6. Рассчитайте коэффициент проводимости для каждого раствора fΛ =Λ/Λ0
7. Сделайте вывод о влиянии концентрации на взаимодействие между ионами.
В растворах слабых электролитов, чем выше концентрация, тем ниже коэффициент проводимости.
По теории Дебая — Онзагера снижение эквивалентной электрической проводимости при переходе от бесконечно разбавленного раствора к растворам конечных концентраций связано с уменьшением скоростей движения ионов. Это объясняется появлением эффектов торможения движения ионов, возникающих за счет сил электростатического взаимодействия между ионом и его ионной атмосферой.
8. Установите область концентрации, для которой применимо уравнение Кольрауша.

Уравнение Кольрауша, в соответствии с графиком, применимо к области концентраций от 0,01 моль/м3 до 0,1 моль/м3
9. Найдите значение предельной электропроводности электролита и коэффициента А по уравнению Кольрауша.
y = -0,0005x + 0,0079
 где А = 0,0005;
где А = 0,0005;
10. Результаты измерений занесите в таблицу.
11. Рассчитайте значение углового коэффициента в уравнении Дебая-Хюккеля-Онзагера, если ε=78,25; η=0,894*10-3 Па*с;
Уравнение Дебая-Хюккеля-Онзагера (1,1 – электролит)

Электрофоретический коэффициент:

Релаксационный коэффициент:

Подставив значения, получим (q = 1/2, так как электролит симметричен):


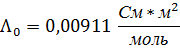
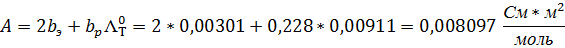
12. Сравните значения полученных угловых коэффициентов:
A (графическая) = 0,0005
А (аналитическая) = 0,008097
13. Определите подвижность катиона и аниона, если число переноса аниона дано в таблице.



14. Предельную электрическую подвижность катиона в водном растворе.

15. Скорость движения катиона при градиенте поля 100 В/м.

16. Стоксов радиус иона (для воды η = 0,894 *  Па*с).
Па*с).

17. Подвижность катиона при бесконечном разведении в ацетоне и нитрометане, вязкости которых при этой температуре соответственно равны 0,310∙  и 0,627∙
и 0,627∙  Па∙с.
Па∙с.





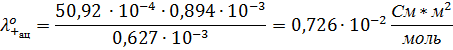
Работа №2
ИЗМЕРЕНИЕ УДЕЛЬНОЙ ЭЛЕКТРОПРОВОДНОСТИ РАСТВОРОВ СЛАБЫХ ЭЛЕКТРОЛИТОВ
Цель работы: определение степени диссоциации слабых электролитов при разных концентрациях и константы диссоциации.
Электролит: CH3COOH
| Молярная концентрация раствора C, моль/м3 | 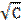
| Удельная проводимость σ*104,См/м | Эквивалентная проводимость Λ*104, См*м2/моль | Степень диссоциации α | Ка |
| 1,61 | 1,6116 | 0,004125 | 1,7086*10-5 | ||
| 2,2361 | 3,56 | 0,7119 | 0,001822 | 1,6629*10-5 | |
| 3,1623 | 5,13 | 0,5130 | 0,001313 | 1,7262*10-5 | |
| 4,4721 | 7,2 | 0,3602 | 0,000922 | 1,7017*10-5 | |
| 7,0711 | 11,37 | 0,2273 | 0,000582 | 1,6946*10-5 |
1. Рассчитать эквивалентную проводимость растворов.
2. Построить графики зависимости 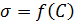 и
и  .
.


3. Пользуясь величинами предельных подвижностей ионов, по закону независимого движения ионов рассчитайте предельную молярную проводимость электролита.

4. Рассчитайте степень диссоциации слабого электролита в каждом исследуемом растворе.
5. Постройте график зависимости α от концентрации раствора. 
6. По закону разбавления Оствальда рассчитайте константу диссоциации для каждого раствора и найдите ее среднее значение.
7. По графикам в координатах  или
или  из угла наклона прямых найдите Λ0 и Ка
из угла наклона прямых найдите Λ0 и Ка





8. Сравните найденное значение константы диссоциации с табличным значением.
К(найденное) = 2,24*10-7
К(табличное) = 1,8*10-5
9. Сделайте вывод о влиянии концентрации раствора на величины α и Ка
У слабых электролитов степень и константа диссоциации понижаются с повышением концентрации раствора.
Работа №3