В норме процессы свободнорадикального окисления в клетках происходят с достаточно низкой скоростью и имеют определенное физиологическое значение, что будет обсуждаться далее. Однако при определенных ситуациях их интенсивность может существенно повышаться и при этом возникает состояние «окислительного стресса».
Окислительный стресс — это состояние, появление которого связано с возникновением дисбаланса между состоянием антиоксидантной и прооксидантной систем в клетках. Оно характеризуется резким повышением в них скорости свободнорадикальных процессов, а также увеличением концентрации свободных радикалов и продуктов их превращения.
Следует заметить, что перекисное окисление липидов представляет собой не единственный свободнорадикальный процесс, который происходит в клетках. Свободнорадикальному окислению могут подвергаться и другие органические молекулы, к числу которых относятся аминокислоты, нуклеотиды и углеводы. При окислительном стрессе происходит увеличение скорости всех этих процессов.
К причинам возникновения окислительного стресса относятся:
· тканевая гипоксия и, соответственно, ишемия тканей. Это связано с тем, что в условиях дефицита кислорода в митохондриях начинается усиленная генерация активных форм кислорода (перекиси водорода и супероксидного аниона-радикала);
· активация флавиновых дегидрогеназ – ксантионкcидазы и НАДФH-оксидазы, принимающих участие в образовании свободных радикалов;
· стимуляция симпатоадреналовой системы (стресс), в виду того, что адреналин подвергается спонтанному окислению кислородом, в результате чего образуется свободнорадикальный продукт, способный инициировать процессы свободнорадикального окисления;
· понижение мощности антиоксидантной системы (ограничение активности антиоксидантных ферментов в условиях метаболического ацидоза и их распада в катаболическую стадию стресса).
Все перечисленные выше причины имеют очень широкое распространение. Поэтому и окислительный стресс представляет собой широко распространенное состояние.
Возникновение окислительного стресса способствует развитию процессов альтерации в организме. Это связано с накоплением в клетках свободных радикалов и нерадикальных цитотоксических продуктов свободнорадикального окисления (т.н. карбонильных веществ).
Повреждающие эффекты свободных радикалов связаны с их высокой реакционной способностью. Они с большой скоростью окисляют молекулы аминокислот и, в том числе аминокислот, входящих в состав полипептидных цепей белков, а также жирнокислотные остатки мембранных фосфолипидов, моносахариды и азотистые основания нуклеиновых кислот. Следствием всего этого становится изменение каталитических свойств ферментов, понижение сродства мембранных рецепторов к их лигандам, изменение структуры нуклеиновых кислот и, как следствие того, нарушение процессов хранения и передачи генетической информации, изменение физических свойств липидного бислоя клеточных мембран, в результате чего нарушается их проницаемость и происходит разобщение окислительного фосфорилирования и понижение уровня энергетического обеспечения клеток, а также как следствие того – нарушение ионного гомеостаза. Все это первоначально приводит к угнетению функциональной активности клеток тканей внутренних органов, следствием чего становится нарушение их функции. Изменения могут достигнуть необратимого характера, что приведет к гибели клетки. Подобные представления лежат в основе свободно-радикальной теории гибели клеток. Современные представления о механизме повреждающих эффектов свободных радикалов представлены на рис. 7.
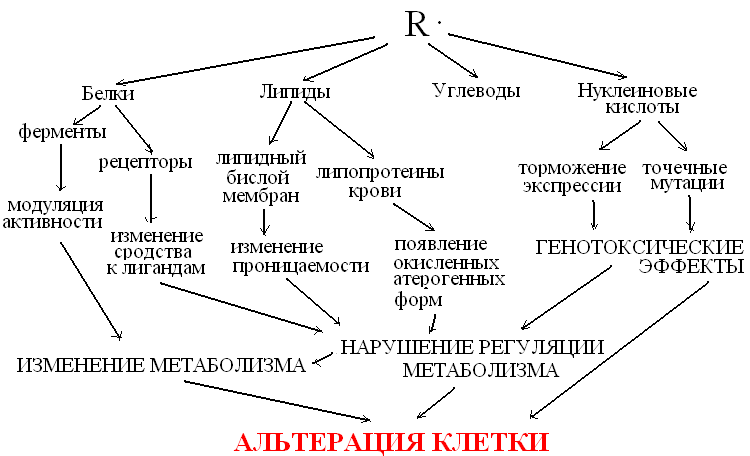
Рис. 7. Механизмы альтерации клетки свободными радикалами
Однако свободнорадикальное повреждение клеток при окислительном стрессе связано не только с эффектом свободных радикалов. Не менее важную роль в том приобретает эффект цитотоксических карбонильных продуктов свободно-радикального окисления. Все они представляют собой стабильное, но очень агрессивные молекулы. В отличие от свободных радикалов, для них характерно даже дистантное действие. Существует точка зрения, согласно которой эндогенные альдегиды представляют собой вторичные мессенджеры повреждения при окислительном стрессе.
Цитотоксическое действие эндогенных альдегидов обусловлено их способностью образовывать соединения (аддукты) с белками, азотистыми основаниями нуклеиновых кислот и другими органическими молекулами (рис. 8).
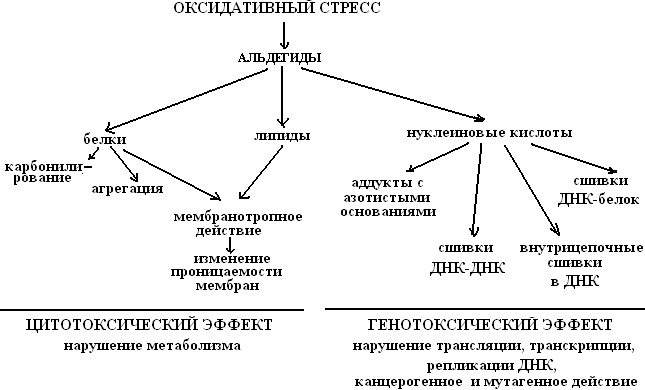
Рис. 8. Механизм проявления цитотоксического и генотоксического действия альдегидов
Как следствие того, в клетках происходит изменение каталитических свойств ферментов, конформации структурных белков, белков цитоскелета и мембранных белков, мембранных и цитоплазматических рецепторов и т.д. В результате появления всех этих сдвигов модулируется активность внутриклеточных энзимов, изменяется сродство рецепторов к лигандам, нарушается течение биоэнергетических процессов в митохондриях и пр. Все это предопределяет глубокое изменение обменных процессов и нарушение их регуляции.
Кроме того, карбонильные вещества обладают генотоксическими свойствами. Образуя соединения с нуклеиновыми кислотами, они вызывают нарушение процессов репликации ДНК, транскрипции и трансляции. В результате всего этого тормозится процесс деления клеток и синтеза внутриклеточных белков. Все это усугубляет повреждающие эффекты свободных радикалов и способствует повреждению клеток.
Помимо карбонильных продуктов обмена в реализации повреждающих эффектов окислительного стресса определенное значение играют активные формы азота (пероксинитрит и др.) и хлора (гипохлориты и др.). Все они обладают высокой реакционной способностью и реагируют с белками, драматически изменяя их свойства.
Окислительный стресс выступает в качестве фактора патогенеза при развитии большинства известных заболеваний. К ним относятся заболевания сердечно-сосудистой системы, желудочно-кишечного тракта, респираторной системы, ЦНС, эндокринные расстройства, хирургическая патология, гинекологические заболевания и др. Столь широкое распространение окислительного стресса в качестве неспецифического фактора патогенеза связано с тем, что в их острой стадии всегда происходит активация симпатоадреналовой системы, как одной из основных причин стимуляции свободно-радикальных процессов. В большей мере значение окислительного стресса, как фактора альтерации тканей проявляется при их ишемическом повреждении. Это характерно для острого инфаркта миокарда, ишемического инсульта, инфаркта почек и др. Это связано с тем, что при ишемии тканей в них в большей мере, чем при других состояниях происходит усиление генерации активных форм кислорода. Это обусловлено тем, что при ишемии:
· в условиях понижения парциального давления кислорода происходит повышение скорости его одноэлектронного восстановления (генерация супероксидного аниона-радикала);
· возникает активация ксантиноксидазы;
· формируется инфильтрация ткани нейтрофилами, что приводит к респираторному взрыву;
· усиливается секреция адреналина, который является мощным источником свободных радикалов в крови;
· происходит ингибирование антиоксидантных ферментов свободными радикалами.
Окислительный стресс играет важную роль при формировании стрессорных поражений внутренних органов (сердца, мозга, слизистой желудка и др.). Причиной того повышение интенсивности радикалообразования в условиях характерной для него тканевой гипоксии и усиления проявлений прооксидантных эффектов адреналина. Продукты ауоокисления адреналина представляют собой свободные радикалы, которые инициируют свободнорадикальные превращения. Поэтому усиление свободнорадикальных процессов приобретает важную роль в возникновении заболеваний стрессорного генеза (ишемической болезни сердца, язвенной болезни желудка, невротических расстройств, эндокринологических заболеваний и др.).
Принимая во внимание столь широкое распространение окислительного стресса в качестве неспецифического звена патогенеза разных заболеваний, можно легко предположить, что в качестве одного из патогенетических подходов к их лечению и профилактике может использоваться антиоксидантная терапия.
Следует вспомнить и свободно-радикальную теорию старения, предложенную Харманом Д. еще в 1954 году. Согласно этой теории, именно свободным радикалам отводится основная роль в развитии старения. Обнародование этой теории привело к всплеску энтузиазма в геронтологии в плане разработки подходов к увеличению продолжительности жизни.
Однако десятилетия использование антиоксидантов в терапии различных заболеваний и попытки их использования как геропротекторов не привели к ожидаемому результату. Каким же образом это можно объяснить исходя из современных представлений о повреждающем действии свободных радикалов и продуктов их внутриклеточных превращений?
Делая попытку ответить на этот вопрос, прежде всего, необходимо вспомнить, что свободнорадикальные процессы постоянно протекают и в здоровом организме. Скорость их невелика. Но они играют важную физиологическую роль.
Умеренное повышение концентрации свободных радикалов при окислительном стрессе имеет отношение в реализации его физиологических эффектов, направленных на адаптацию клетки к действию неблагоприятных факторов среды.
Участие свободно-радикальных процессов в формировании адаптивных процессов связано с тем, что они участвуют в:
· стимуляции внутриклеточных сигнальных путей;
· контроле экспрессии генов – активации факторов транскрипции;
· стимуляции синтеза стресс-белков;
· синтезе простаноидов и регуляции продукции цитокинов;
· антимикробной защите.
Это связано с тем, что некоторые АФК в качестве участников внутриклеточных сигнальных путей, принимают участие в активации факторов транскрипции и, там самым регуляции экспрессии генов. Поэтому при умеренном окислительном стрессе происходит повышение скорости экспрессии генов целого ряда белков, обладающих защитными свойствами. К ним относятся антиоксидантные ферменты, ферменты (СОД, пероксидазы), ферменты, обеспечивающие катаболизм карбонильных промежуточных продуктов обмена (альдегидредуктазы), белки теплового шока и др. В результате возникновения подобных сдвигов повышается устойчивость клеток к действию повреждающих факторов внешней среди. Более того, с эффектами свободных радикалов и активных форм кислорода связана регуляция клеточной пролиферации, дифференцировки, апоптоза и роста.
Процесс образования некоторых биологически активных веществ в клетках также происходит с участием свободнорадикальных процессов – образование простаноидов и лейкотриенов. В этой связи они принимают активное участие в формировании воспалительных и аллергических реакций.
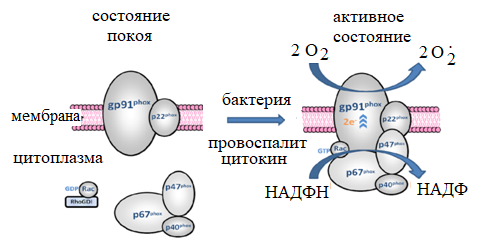
Физиологическая роль свободных радикалов связана и с их участием в антимикробной защите. Известно, что фагоциты (макрофаги), содержат в мембранах особый фермент – НАДФН-оксидазу (рис. 9). Он принимает участие в продукции супероксидного аниона радикала и его выделении в окружающую клетку среду или внутрь органеллы – фагосомы (лизосомы).

а
б
Рис. 9. Реакция, катализируемая НАДФН оксидазой (а), ее строение и механизм активации (б)
НАДФН-оксидаза представляет сложный белковый комплекс. В состоянии покоя, его компоненты частично диссоциированы и находятся в мембране клетки и ее цитоплазме. Однако при определенных условиях (появление бактерий или повышение концентрации провоспалительных цитокинов), компоненты НАДФН-оксидазы объединяются в единый комплекс. В результате этого в клетке начинается окисление восстановленного НАДФ, а на поверхности мембраны – генерация суперокcидного аниона радикала.
Образовавшийся супероксидный анион далее используется для образования других агрессивных веществ – активных форм кислорода, азота и хлора (перекиси водорода, пероксинитритов и гипохлорита). Все это предопределяет возникновение «респираторного взрыва»:
О2- + О2- + 2Н+ → Н2О2 + О2.
Н2О2 + Cl- + H+ → НОС1 + H2O (миелопероксидаза)
NO + О2- → ONOO- → ОН* + NO2
Образующиеся в процессе респираторного взрыва агрессивные вещества оказывают губительное воздействие на микробные клетки, вызывая повреждение их структурных компонентов (белков, мембранных липидов, нуклеиновых кислот). Все это лежит в основе механизма антимикробной защиты организма фагоцитами.
Врожденная недостаточность продукции НАДФН-оксидазы характерна для хронического грануломатоза. Это заболевание проявляется рецидивирующими инфекционными поражениями кожи, дыхательных путей, печени, незавершенным фагоцитозом и персистированием бактериальных возбудителей в лейкоцитах.
Таким образом, окислительный стресс может выступать в качестве неспецифического фактора адаптации организма к внешним неблагоприятным условиям. В этом случае, во-первых, становится понятным, почему он возникает в острой стадии большинства заболеваний и при различных физиологических состояниях (стрессе).
Во-вторых, становится очевидным, что использование антиоксидантной терапии должно иметь четкое обоснование и использоваться только в определенных ситуациях. Очевидно, именно этим можно объяснить результаты многочисленных многоцентровых исследований, в частности, о неэффективности лечения сердечно-сосудистых заболеваний антиоксидантными препаратами. Можно согласиться с высказываемым в литературе мнением, что широкое применение антиоксидантов может принести больше пользы, чем вреда.
И в-третьих, использование подходов, связанных с мягким прооксидантным воздействием на организм, может эффективно применяться для повышения неспецифической резистентности организма к неблагоприятным внешним воздействиям. Хорошей иллюстрацией того может быть использование дозированной физической нагрузки, как неспецифического подхода к адаптации организма.
Вместе с тем, окислительный стресс выступает в качестве мощного фактора альтерации тканей, механизм которого был описан выше. Очевидно, что для реализации физиологических или патологических механизмов окислительного стресса решающее значение приобретает его интенсивность (сила). При высокой интенсивности свободнорадикальных процессов, что сопровождается резким повышением уровня свободных радикалов и стабильных цитотоксических продуктов их превращений (карбонильных продуктов обмена), формируются предпосылки для повреждения тканей. В тоже время при умеренном окислительном стрессе, в виду параллельной стимуляции систем защиты от свободных радикалов и эндогенных альдегидов, возникают условия для проявления его физиологических эффектов.
Принимая во внимание роль эндогенных альдегидов в качестве мессенджера повреждения при окислительном стрессе и физиологическую роль активных форм кислорода, как компонентов сигнальных путей, возникает логичное предположение о перспективности использования для лечения и профилактики многих заболеваний мероприятий, направленных на связывание и увеличение скорости утилизации эндогенных альдегидов в организме. Подобное направление терапии и профилактики в настоящее время активно разрабатывается.
Как же можно количественно оценить состояние окислительного стресса? В настоящее время существуют представления о маркерах окислительного стресса. По их уровню в тканях и биологических жидкостях можно оценить выраженность этого процесса.
К маркерам окислительного стресса относятся промежуточные и конечные продукты, которые образуются в процессе свободнорадикальных превращений в организме. Среди них:
· карбонильные вещества. К ним относятся альдегидные продукты, которые возникают в процессе ПОЛ – малоновый диальдегид, 4-гидроксиноненаль, глиоксаль и др.;
· карбонилированные белки. Образуются в процессе свободнорадикального окисления белков;
· окисленные аминокислоты;
· 8-оксогуанозин, который является продуктом свободнорадикального окисления гуанина, входящего в состав нуклеиновых кислот;
Все эти показатели могут использоваться для оценки выраженности окислительного стресса в организме. Однако, до настоящего времени все еще отсутствуют четкие количественные критерии оценки окислительного стресса, при которых начинают проявляться его повреждающие эффекты. Вместе с тем определение указанных лабораторных показателей может быть полезным для:
· оценки тяжести патологического процесса;
· определения течения и возникновения осложнений заболевания;
· мониторинга лечения патологического процесса.
Резюмируя все выше изложенное, можно заключить, что свободнорадикальные процессы являются неотъемлемой частью метаболизма. Они играют важную роль в его регуляции и адаптации организма к существованию в изменяющихся условиях внешней среды. Вместе с тем окислительный стресс выступает в качестве неспецифического фактора патогенеза разных по этиологии заболеваний. Его интенсивность может быть оценена путем измерения уровня маркеров окислительного стресса в биологических жидкостях. Оценка динамики окислительного стресса может использоваться для мониторинга заболевания. Обоснованное ограничение окислительного стресса используется в качестве одного из патогенетических подходов в лечении внутренних заболеваний.