Тема: Классификация оксидов
Практически все простые вещества при окислении образуют оксиды. Атомы многих элементов, проявляя разную валентность, участвуют в образовании нескольких оксидов, например у азота есть пять оксидов: N2O, NO, N2O3, NO2, N2O5. Из-за такого большого разнообразия нужно уметь правильно называть и классифицировать оксиды.
Определение
Оксиды – сложные вещества, состоящие из атомов двух химических элементов, одним из которых является кислород.
Общая формула оксидов: ЭхОу, где Э – атомы химического элемента; О – атомы кислорода; х, у – индексы, указывающие число атомов элементов, образующих оксид.
Алгоритм составления названий оксидов
Слово «оксид» (им. падеж) + название элемента (род. падеж) + указание степени окисления, если она переменная, римскими цифрами в скобках
K2O – оксид калия
CaO – оксид кальция
Al2O3– оксид алюминия
SiO2 – оксид кремния (IV) (читается «оксид кремния четыре»)
N2O5 – оксид азота (V) (читается «оксид азота пять»)
SO3 – оксид серы (VI) (читается «оксид серы шесть»)
Cl2O7 – оксид хлора (VII) (читается «оксид хлора семь»)
Классификация оксидов
| Признак классификации | Группа оксидов | Примеры |
| Агрегатное состояние (при стандартных условиях) | Твёрдое | SiO2,Fe2O3,CaO,P2O5SiO2,Fe2O3,CaO, P2O5 |
| Жидкое | H2O,SO3H2O,SO3 | |
| Газообразное | CO2,SO2,N2OCO2,SO2,N2O | |
| Растворимость в воде | Растворимые | P2O5,CaO,K2O,SO2P2O5,CaO,K2O,SO2 |
| Нерастворимые | SiO2,Fe2O3,Cu2OSiO2,Fe2O3,Cu2O | |
| Химические свойства | Солеобразующие | Na2O,BaO,CO2,P2O5Na2O,BaO,CO2, P2O5 |
| Несолеобразующие | N2O,NO,CO,SiON2O,NO,CO,SiO |
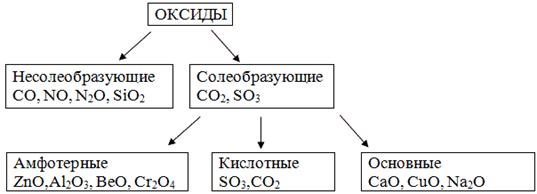
Как видно из таблицы, все оксиды подразделяют на солеобразующие и несолеобразующие.
Несолеобразующие оксиды – оксиды, которые не взаимодействуют ни с кислотами, ни с щелочами и не образуют солей. Несолеобразующих оксидов немного. В их состав входят элементы-неметаллы, например: N2O, NO, CO, SiO
Солеобразующие оксиды – оксиды, которые взаимодействуют с кислотами или основаниями с образованием солей и воды.
Среди солеобразующих оксидов различают оксиды оснóвные, кислотные и амфотерные.
Оснóвные оксиды – оксиды, которые соответствуют основания.
MgO соответствует Mg(OH)2;
Na2O – NaOH;
CaO – Ca(OH)2;
Mn+2O – Mn(OH)2
Оснóвные оксиды образуют только металлы и, как правило, с валентностью I и II. Исключениями являются: ZnO, BeO, SnO, PbO.
Кислотные оксиды – оксиды, которым соответствуют кислоты.
N2O3 соответствует HNO2;
SO2 – H2SO3;
P2O5 – H3PO4;
Cr+6O3 соответствует хромовая H2CrO4 и дихромовая H2Cr2O7 кислоты;
Mn+72O7 – марганцевая кислота HMnO4.
Кислотные оксиды образуют все неметаллы независимо от степени окисления (кроме несолеобразующих N2O, NO, CO, SiO), а также металлы с валентностью V и выше.
Амфотерные оксиды – это оксиды, которым соответствуют и основания, и кислоты. Амфотерные оксиды: Al2O3, PbO2, ZnO, BeO, SnO, PbO.
На основании вышеизложенного можно сделать вывод: свойства оксидов зависят от того, атомы какого элемента (металла, неметалла) и в какой валентности их образуют.

Даны формулы оксидов: MgO, CaO, CuO, Cu2O, Na2O, K2O, CO, SO2, SO3, NO, N2O, N2O5, Р2O5, Al2O3, BeO, Rb2O, MnO2, SiO2, FeO, Fe2O3, Fe3O4, ZnO. Распределите их по классам: несолеобразующие, кислотные, основные, амфотерные.
Домашнее задание:
1. Даны формулы веществ:
Cu, AI2O3, CO2, BaSO4,CI2O7, MgO, NaNO3, HCI, H2SO3, O2, CaO, HNO3, N2O5, AgCI, Fe. Выпишите формулы основных и кислотных оксидов. Дайте названия оксидам.
2. Определите валентность атомов химических элементов по формулам их оксидов: SO2, AI2O3, NO, Cu2O, NO2, Na2O.
3. Составьте формулы оксидов по их названиям:
а) Оксид алюминия, б) оксид серы(VI), в) оксид железа (III), г) оксид азота (IV), д) оксид натрия,е) оксид фосфора (V), з) оксид кальция.
4. Назовите оксиды по их формулам:
А) FeO, б) SO2 , в) BaO, г) NO2, д) K2O, е) Cu2O.
Выполните упражнения: (к классной работе)
1. Ряд веществ, являющихся оксидами.
| А) Na2O, Na2O2, CuO, Cu2S Б) FeO, Fe2O3, Fe3O4, FeCl2 | B) CO2, Cu2O, MgO, OF2 Г) LiOН, SO3, BeO, Cl2O7. |
2. Ряд основных оксидов.
| А), SO3, V2O5, CuO Б) CaO, K2O, MgO, Li2O | B) ZnO, Mn2O7, MnO, Al2O3 Г) P2O5, BeO, BaO, CO2. |
3. Ряд амфотерных оксидов:
| А) ZnO, BeO, Al2O3, Cr2O3 Б) ZnO, BeO, K2O, MgO | B) CO2, Cu2O, BaO, Al2O3 Г) CrO3, MnO, FeO, Na2O. |
4. Ряд кислотных оксидов:
| А) Al2O3, SO3, BeO, Cl2O7 Б) P2O5, Cl2O7, CrO3, Mn2O7 | B) Li2O, SO3, BeO, Cl2O7 Г) SO2, SO3, CuO, Mn2O3. |
5. Ряд несолеобразующих оксидов:
| А) Li2O, SO3, BeO, Cl2O7. Б) ZnO, Mn2O7, MnO, Al2O3 | В) CO, N2O, NO, SiO Г) CrO3, MnO, FeO, Na2O. |
Оксиды
1.Поиграйте в «крестики-нолики». Покажите выигрышный путь, которые составляют формулы. Выпишите и назовите, формулы которых составляют выигрышный путь.
а) оксидов
| HCl | NaOH | SO2 |
| O2 | Al2O3 | H2O2 |
| FeO | H2SO4 | NaBr |
б) оксидов металлов
| SO3 | Fe2O3 | SiO2 |
| CuO | BaO | CO2 |
| NO | K2O | MgO |
в) оксидов неметаллов
| Li2O | NO2 | P2O5 |
| Cl2O7 | N2O3 | FeO |
| CO | ZnO | H2O |