Муниципальное бюджетное общеобразовательное учреждение
«Лицей №7»
Исследовательский проект на тему:
«Адсорбция»
Исследовательский проект
по химии выполнен
обучающимся 9 В класса
МБОУ Лицей №7
Кириковым Михаилом
Научный руководитель:
учитель химии Круглова О. Н.
Кстово, 2020 г
Оглавление
| Стр. | |
| Введение | |
| Теоретическая часть. | |
| 1. Что такое адсорбция? | |
| 2. Теории адсорбции. | |
| 3. Практическое использование явления адсорбции. | |
| 3.1. Адсорбция на твердых поверхностях и её применение в пищевой промышленности. | |
| 3.2. Адсорбция в медицине. | |
| Практическая часть. | |
| 4. Исследование адсорбционных свойств некоторых лекарственных препаратов. | |
| 4.1. Характеристика объекта исследования. | |
| 4.2. Химический эксперимент. | |
| Заключение. | |
| Литература. |
Введение.
Адсорбционные явления чрезвычайно широко распространены в живой и неживой природе. Толщи горных пород и почвы являются огромными колоннами с адсорбентами, по которым перемещаются водные и газовые растворы. Легочная ткань подобно адсорбенту – носителю, на котором удерживается гомоглобин крови, обеспечивающий перенос кислорода в организм. Многие функции биологических мембран живой клетки связаны со свойствами их поверхности, так, например, общая площадь биологических мембран в организме человека достигает десятков тысяч квадратных метров. Даже такие наши чувства, как обоняние и вкус, зависят от адсорбции молекул соответствующих веществ в носовой полости и на языке.
Сегодня адсорбция составляет основу многих промышленных операций и научных исследований. Наиболее важные из них – очистка, выделение и разделение различных веществ, адсорбционная газовая и жидкостная хроматография. Адсорбция является важной стадией гетерогенного катализа и коррозии. Исследования поверхности тесно связаны с развитием полупроводниковой техники, медицины, строительства и военного дела. Адсорбционная терапия применяется для удаления токсинов и вредных веществ из пищеварительного тракта. Такие адсорбенты, как гидроксид алюминия, оксид магния, фосфат алюминия, входят в состав препаратов альмагель, фосфалюгель. Активированный уголь давно применяется как адсорбент газов (при метеоризме), токсинов (при пищевых токсикоинфекциях), алкалоидов и тяжелых металлов (при травлениях). Адсорбционные процессы играют ключевую роль при выборе стратегии защиты окружающей среды.
В начале работы мной была сформулирована гипотеза исследования.
Гипотеза: исследуемые сорбенты обладают одинаковой адсорбционной способностью.
Гипотеза определила цель работы, задачи, объект и предмет исследования.
Цель работы: изучение явления адсорбции и исследование адсорбционных свойств некоторых лекарственных препаратов.
Задачи:
1. Изучить теоретические основы явления адсорбции.
2. Рассмотреть применение явления адсорбции на практике.
3. Исследовать свойства некоторых лекарственных препаратов.
Объект исследования: адсорбционные процессы
Предмет исследования: адсорбционные свойства лекарственных препаратов: «Полисорб», «Энтеросгель», «Уголь активированный», «Смекта».
Актуальност ь определяется тем, что проект будет интересен обучающимся, интересующимся химией, медициной и может быть использован в качестве дополнительного материала на уроках и элективных занятиях.
Теоретическая часть.
- Что такое адсорбция?
Адсорбция (от лат. «ad» — на, при и «sorbeo» — поглощаю) - это поглощение какого-либо вещества из газообразной среды или раствора поверхностным слоем жидкости или твёрдого тела. Например, если поместить в водный раствор уксусной кислоты кусочек угля, то произойдёт адсорбция— количество кислоты в растворе уменьшится, молекулы кислоты сконцентрируются на поверхности угля.
Явление адсорбции стало изучаться со 2-й половины 18 в. (Шееле, 1773), хотя несомненно, что в практической деятельности человечества адсорбция использовалась с незапамятных времён. Учение об адсорбции является частью более общей теории многокомпонентных гетерогенных систем, основы которой заложены У. Гиббсом (1876).
Явление адсорбции тесно связано с особыми свойствами вещества в поверхностном слое. Например, молекулы, лежащие на поверхности раздела фаз жидкость — пар, втягиваются внутрь жидкости, т. к. испытывают большее притяжение со стороны молекул, находящихся в объёме жидкости, чем со стороны молекул пара, концентрация которых во много раз меньше концентрации жидкости. Это внутреннее притяжение заставляет поверхность сокращаться и количественно характеризуется поверхностным натяжением. По той же причине молекулы какого-либо другого вещества, оказавшиеся вблизи поверхности, притянутся к ней, и произойдёт адсорбция. После адсорбции внутреннее притяжение частично компенсируется притяжением со стороны адсорбционного слоя и поверхностное натяжение уменьшается. Гиббс вывел формулу, связывающую значение адсорбции с изменением поверхностного натяжения. Те вещества, адсорбция которых сильно уменьшает поверхностное натяжение, принято называть поверхностно-активными.
Вещество, на поверхности которого происходит адсорбция, называется адсорбентом, а поглощаемое из объёмной фазы — адсорбатом. В зависимости от характера взаимодействия между молекулой адсорбата и адсорбентом адсорбцию принято подразделять на физическую и хемосорбцию. Менее прочная физическая адсорбция не сопровождается существенными изменениями молекул адсорбата. Она обусловлена силами межмолекулярного взаимодействия, которые связывают молекулы в жидкостях и некоторых кристаллах и проявляются в поведении сильно сжатых газов. При хемосорбции молекулы адсорбата и адсорбента образуют химические соединения. Часто адсорбция обусловлена и физическими и химическими силами, поэтому не существует чёткой границы между физической адсорбцией и хемосорбцией.
Следует подчеркнуть, что явления физической и химической адсорбции чётко различаются в очень редких случаях. Обычно осуществляются промежуточные варианты, когда основная масса адсорбированного вещества связывается сравнительно слабо и лишь небольшая часть – прочно. Например, кислород на металлах или водород на никеле при низких температурах адсорбируются по законам физической адсорбции, но при повышении температуры начинает протекать химическая адсорбция. При повышении температуры увеличение химической адсорбции с некоторой температуры начинает перекрывать падение физической адсорбции, поэтому температурная зависимость адсорбции в этом случае имеет четко выраженный минимум (рис. 1).
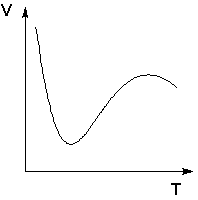
Рис. 1 Зависимость объема адсорбированного никелем водорода от температуры
Физически адсорбированные молекулы более или менее свободно перемещаются по поверхности, при этом их свойства часто аналогичны свойствам очень тонкого слоя газа, т. н. двухмерного газа. Они могут собираться группами, образуя слой двухмерной жидкости или двухмерного твёрдого тела. Адсорбированные молекулы рано или поздно покидают поверхность — десорбируются. Время, в течение которого молекула находится на поверхности, называется временем адсорбции. Времена адсорбции могут колебаться в очень широких пределах. Скоростью адсорбции (соответственно скоростью десорбции) называется количество молекул, адсорбирующихся (или десорбирующихся) за единицу времени, оба значения величин относят к единице поверхности или массы адсорбента. Скорость хемосорбции, как и скорость любого химического процесса, чаще всего увеличивается с повышением температуры. Если скорости адсорбции и десорбции равны друг другу, то говорят, что установилось адсорбционное равновесие. В состоянии равновесия количество адсорбированных молекул остаётся постоянным сколь угодно долго, если неизменны внешние условия (давление, температура и др.).
Теории адсорбции.
Единой теории, которая достаточно корректно описывала бы все виды адсорбции на разных поверхностях раздела фаз, не имеется; поэтому рассмотрим некоторые наиболее распространенные теории адсорбции, описывающие отдельные виды адсорбции на поверхности раздела твердое тело – газ или твердое тело – раствор.
Теория мономолекулярной адсорбции Лэнгмюра
Теория мономолекулярной адсорбции Лэнгмюра основывается на следующих положениях:
1) Адсорбция является локализованной и вызывается силами, близкими к химическим.
2) Адсорбция происходит не на всей поверхности адсорбента, а на активных центрах, которыми являются выступы либо впадины на поверхности адсорбента, характеризующиеся наличием т.н. свободных валентностей. Активные центры считаются независимыми (т.е. один активный центр не влияет на адсорбционную способность других), и тождественными.
3) Каждый активный центр способен взаимодействовать только с одной молекулой адсорбата; в результате на поверхности может образоваться только один слой адсорбированных молекул.
4) Процесс адсорбции является обратимым и равновесным – адсорбированная молекула удерживается активным центром некоторое время, после чего десорбируется; т.о., через некоторое время между процессами адсорбции и десорбции устанавливается динамическое равновесие. В состоянии равновесия скорость адсорбции равна скорости десорбции.
М.Поляни предложил теорию полимолекулярной адсорбции, основанную на следующих основных положениях:
1. Адсорбция вызвана чисто физическими силами.
2. Поверхность адсорбента однородна, т.е. на ней нет активных центров; адсорбционные силы образуют непрерывное силовое поле вблизи поверхности адсорбента.
3. Адсорбционные силы действуют на расстоянии, большем размера молекулы адсорбата. Иначе говоря, у поверхности адсорбента существует некоторый адсорбционный объем, который при адсорбции заполняется молекулами адсорбата.
4. Притяжение молекулы адсорбата поверхностью адсорбента не зависит от наличия в адсорбционном объеме других молекул, вследствие чего возможна полимолекулярная адсорбция.
5. Адсорбционные силы не зависят от температуры и, следовательно, с изменением температуры адсорбционный объем не меняется.
Практическое использование явления адсорбции.