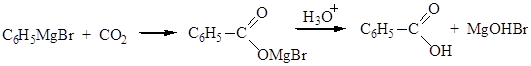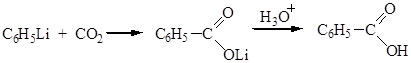Введение
Каркасным соединениями называют те, в которых ковалентные cвязи между атомами всей или части молекулы замыкают внутри себя некоторый объем. Среди каркасных углеводородов наиболее изучен ряд адамантана. Это углеводороды, которые содержат как минимум один фрагмент адамантана. Адамантан – трицикло – 3,3,1,1 – декан, его брутто формула C10H16, он состоит из трех циклогексановых колец в конформации «кресло». Атомы углерода в молекуле адамантана расположены в такой же последовательности, как в кристаллической решетке алмаза. Используются следующие изображения структурной формулы адамантана:
В отсутствии заместителей 4 третичных (узловых) атомов углерода в положениях 1,3,5,7 эквивалентны. Эквивалентными являются и 6 вторичных (мостиковых) атомов углерода (2,4,6,8,9,10). При одном заместителе возможно два структурных изомера.
Молекула адамантана обладает высокой степенью симметрии. Симметрия охраняется при введении одного или нескольких заместителей в узловые положения ядра. Производные адамантана, которые содержат только узловые заместители, из-за отсутствия в них ассиметричных атомов углерода, не имеют пространственных изомеров. Одновременно такие соединения могут обладать оптической активностью, если в молекуле адамантана имеются четыре разных заместителя.
Возможность образования пространственных изомеров появляется у производных адамантана только при наличии в молекуле мостиковых заместителей. С увеличением числа таких заместителей количество возможных стереоизомеров возрастает, но фактически их образуется много меньше, чем теоретически возможно, вследствие высокой симметрии молекулы.
Адамантан обладает необычно высокой температурой плавления (269°С) для такого сравнительно низкомолекулярного углеводорода. Это обусловлено высокой симметрией жесткой алмазоподобной молекулы адамантана. Вместе с этим относительно слабое межмолекулярное взаимодействие в кристаллической решетке приводит к тому, что углеводород легко возгоняется, частично – уже при комнатной температуре.
Химические свойства адамантана своеобразны. В отличие от алициклических и циклических соединений, взаимодействующих с большинством реагентов по радикальному механизму, для адамантана характерны реакции нуклеофильного замещения.
Адамантан впервые был получен С. Ландой и В. Махачеком в 1933 г. при исследовании нефти Годонинского месторождения (Чехословакия). Впоследствии были разработаны синтетические методы получения адамантана путем изомеризации гидрованного димера циклопентадиена, а также получения алкиладамантанов изомеризацией трициклических пергидроароматических углеводородов над галогенидами алюминия и над алюмоокисными и алюмосиликатными катализаторами.
Каркасные соединения, достаточно хорошо использующиеся в качестве лекарственных средств, не относятся к веществам, образующимся в организме теплокровных животных, однако, они синтезируются растениями. Адамантанкарбоновые кислоты используются в качестве сырья для производства лекарственных препаратов, таких как ремонтадин, редонтан. Производные адамантана имеют широкий спектр противовирусной активности и активности против болезни Паркинсона. [1].
На основе химии адамантана возникла и развилась химия органических полиэдранов.
Литературный обзор.
Синтез алифатических и ароматических кислот.
Промышленные способы получения ненасыщенных карбоновых кислот.[2].
1.Окисление углеводородов. Существует два способа: окисление низших алканов C4-C8 преимущественно в уксусную кислоту и окисление твердого парафина в синтетические жирные кислоты (СЖК) с прямой цепью углеродных атомов С10-С20, являющихся сырьем для синтеза ПАВ
2. Синтезы на основе оксида углерода (II). Карбоновые кислоты получают на основе оксида углерода по реакции карбонилирования:

Особый интерес данный метод представляет для синтеза кислот с третичным радикалом (неокислот) из изоолефинов (реакция Коха):

Механизм реакции состоит в предварительном протонировании алкена кислотой с образованием иона карбения, его взаимодействия с СО с получением ацилий – катиона и реакции последнего с водой с образованием карбоновой кислоты:
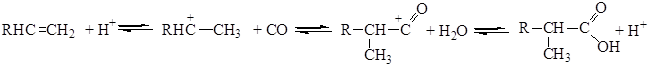
Неокислоты и их соли обладают очень высокой растворимостью и вязкостью, а их сложные эфиры - стабильностью к гидролизу, что обеспечивает им широкое применение в ряде отраслей.
Лабораторные способы получения карбоновых кислот
1.Окисление альдегидов и кетонов.

2.Гидролиз нитрилов.
 3. Синтез Гриньяра. При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:
3. Синтез Гриньяра. При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:

Под действием сильной кислоты (обычно НСl) соль превращается в кислоту:

4. Гидролиз жиров Жиры - сложные эфиры карбоновых кислот и глицерина (триглицериды). Карбоновые кислоты, входящие в состав жиров имеют углеродную цепь от 3 до 18 углеродных атомов. Кипячение жиров или масел с водными растворами щелочей (NaOH, КОН) приводит к получению солей карбоновых кислот и глицерина. Эта операция называется омылением, так как соли карбоновых кислот используют для изготовления мыла.
Методы получения ароматических карбоновых кислот.[3].
Превращение функциональных групп.
1. Окисление ароматических углеводородов.
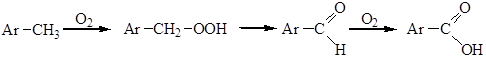
Жидкофазным окислением метилбензолов кислородом воздуха в промышленности получают моно- и дикарбоновые ароматические кислоты.
Окисление можно проводить перманганатом калия в кислой среде:

2. Окисление спиртов, альдегидов и кетонов. В качестве окислителя может выступать щелочной раствор перманганата калия, ароматические альдегиды окисляются аммиачным раствором оксида серебра
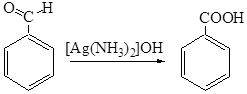

3. Реакция Канниццаро:

4. Гидролиз галогенпроизводных.

5. Гидролиз нитрилов

Введение карбоксильной группы в ароматическое ядро
1. Применение фосгена
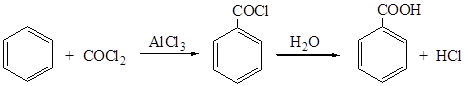
2. Ацилирование эфирами хлоругольной кислоты

3. Через стадию формилирования

4. Через стадию ацилирования ароматических углеводородов

5. Синтез на основе металлоорганических реагентов