Сложными эфирами карбоновых кислот называют продукты замещения гидроксила –ОН кислоты на остаток спирта –OR. Общая
формула сложных эфиров R – C = O. Сложные эфиры получают
|
OR'
при взаимодействии карбоновых кислот со спиртами в присутствии ионов водорода (реакция этерификации):

 О О
О О


 СН3 – С – ОН + Н – О – С2Н5
СН3 – С – ОН + Н – О – С2Н5 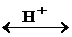 СН3 – С – О – С2Н5 + Н2О
СН3 – С – О – С2Н5 + Н2О
 Уксусная Метиловый Уксусноэтиловый эфир
Уксусная Метиловый Уксусноэтиловый эфир
кислота спирт (этилацетат)
Реакция обратима.
Названия сложных эфиров обычно производят из названий образующих их кислот и спиртов, а по номенклатуре ИЮ ПАК – из названий радикала спирта и радикалов (ацила), заменяя в последнем окончании «ил» на «ат».
Сложный эфиры – довольно активные соединения. Для них характерны реакции нуклеофильного замещения алкоксигруппы.
Сложные эфиры могут подвергаться гидролизу как в кислой, так и в щеочной среде. В кислой среде эта реакция обратима и образуются карбоновая кислота и спирт:

 О О
О О




 СН3 – С + Н – ОН
СН3 – С + Н – ОН 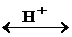 СН3 – С + С2Н5ОН
СН3 – С + С2Н5ОН
 О – С2Н5 ОН
О – С2Н5 ОН
Этилацетат Уксусная Этиловый
кислота спирт
Гидролиз в щелочной среде необратим. Продуктом щелочного гидролиза, называемого омылением, являются спирт и соль карбоновой кислоты:

 O O
O O
 СН3 – С – О – С2Н5 + NaOH → CH3 – C
СН3 – С – О – С2Н5 + NaOH → CH3 – C
ONa + C2H5OH
Ацетат натрия
Жирами называются сложенные эфиры, образованные трёхатомным спиртом глицерином и высшими жирными кислотами. Главными являются пальмитиновая (С15Н31СООН), стеариновая (С17Н35СООН) и непредельная олеиновая (С17Н33СООН) кислоты. Другие непредельные кислоты – линолевая и линоленовая - присутствуют в жирах в значительно меньшем количестве.
Строение жиров выражается общей формулой:
СН2 – ОСОR
|
CH - OCOR'
|
CH2 - OCOR'',
где: R, R', R'' – углеводородные радикалы.
Природные жиры являются полными эфирами глицерина, поэтому их называют глицеридами, или триацилглицеринами.
Образование глицерида стеариновой кислоты (тристеарина) можно изобразить уравнением: О О


 || ||
|| ||
СН2 – О – Н НО – С – С17Н35 СН2 – О – С – С17Н35 | || ||
 CH – O – H + HO – C – C17H35 CH – O – C – C17H35 + 3H2O
CH – O – H + HO – C – C17H35 CH – O – C – C17H35 + 3H2O
| O O
| || ||
CH2 – O – H HO – C – C17H35 CH2 – O – C – C17H35
 |
Глицерин Тристеарин
Глицериды называют простыми, если они содержат остатки одной кислоты, или смешанными, если остатки разных кислот. Природные жиры представляют собой смеси смешанных глицеридов.
По агрегатному состоянию различают твёрдые жиры, обычно это животные жиры, и жидкие – растительные масла. Твёрдые жиры содержат в основном остатки предельных кислот, а жидкие жиры (масла) – остатки непредельных кислот.
Жидкие жиры превращают в твёрдые путём реакции гидрогенизации – присоединения водорода в присутствии катализатора - никеля:
СН2–О–СО–(СН2)7–СН=СН(СН2)7–СН3 СН2–О–СО–(СН2)–СН2–СН2–(СН2)7–СН3
| |
 CH2–O–CO–(CH2)7–CH=CH–(CH2)7–CH3+3H2 CH–O–CO–(CH2)7–CH2–CH2–(CH2)7–CH3
CH2–O–CO–(CH2)7–CH=CH–(CH2)7–CH3+3H2 CH–O–CO–(CH2)7–CH2–CH2–(CH2)7–CH3
| |
CH2–O–CO–(CH2)7–CH=CH–(CH2)7–CH3 CH2–O–CO–(CH2)7–CH2–CH2–(CH2)7–CH3
Триолеин Тристеарин
Жиры, как сложные эфиры, способны подвергаться гидролизу в кислой или щелочной среде. При этом образуются глицерин и высшие жирные кислоты или их соли – мыла. Щелочной гидролиз жиров называют омылением:
СН2 – О – СО – С17Н35 СН2 – СН
| |
 CH – O – CO – C17H35 + 3NaOH CH–OH + 3 C17H35COONa
CH – O – CO – C17H35 + 3NaOH CH–OH + 3 C17H35COONa
| | Стеарат натрия
CH – O – CO – C17H35 CH2 – OH (мыло)
Тристеарин
Калиевые и натриевые мыла в воде частично гидролизуются с образованием свободных жирных кислот и гидроксида щелочного металла, поэтому их растворы имеют щелочную реакцию:
С17Н35СООNa + H2O ↔ C17H35COOH + NaOH
Стеарат Стеариновая
натрия кислота
При добавлении натриевого мыла к жёсткой воде ионы кальция и магния замещают ионы натрия, образуя нерастворимые и поэтому не обладающие моющим действием кальциевые и магниевые мыла:
2 С17Н35СООNa + CaCl2 → (C17H35COO)2 Ca + 2 NaCl
Стеарат натрия Стеарат кальция