Домашнее задание по химии №3 для специалистов ф-та «Э»
Коррозия металлов. Защита металлов от коррозии.
Примеры решения задач
Задача 1. Подтвердить термодинамическую возможность газовой коррозии (высокотемпературного окисления) железного изделия при Т = 800 К в газовой смеси, парциальное давление кислорода в которой равняется 0,01 атм, если она сопровождается образованием на поверхности изделия оксида FeO. Вычислить парциальное давление кислорода, ниже которого коррозия прекратиться при заданной температуре, а также определить температуру, выше которой коррозия станет невозможной при стандартных состояниях компонентов.
Решение. Для подтверждения возможности газовой коррозии, описываемой уравнением
2Fe(т) + O2 (г) D 2FeO(т) 
рассчитывают значение энергии Гиббса протекающего процесса при Т = 800 К. Для этого используют уравнение изотермы Вант−Гоффа, которое для рассматриваемого процесса выглядит как
Δ rG 800 = Δ rG 0800 + R ∙800∙ln  ,
,
где  =
=  = 0,01 – относительное значение неравновесного парциального давления кислорода.
= 0,01 – относительное значение неравновесного парциального давления кислорода.
В последнем стандартную энергию Гиббса Δ rG 0800 находят по приближенной форме уравнения Гиббса−Гельмгольца:
Δ rG 0800 ≈  − 800·
− 800· 
Значение  вычисляют по следствию из закона Гесса:
вычисляют по следствию из закона Гесса:
 кДж.
кДж.
Аналогично по справочным величинам  находят
находят  .
.
 Дж/K
Дж/K
В итоге
Δ rG 0800 = −529,6 − 800·(−137,84·10−3) = −419,33 кДж
а
Δ rG 800 = −419,33 − 8,31·800·10−3·ln 0,01 = −388,70 кДж
Так как Δ rG 800 < 0, то газовая коррозия железного изделия в данных условиях термодинамически возможна. Она не будет протекать, если
Δ rG 800 = Δ rG 0800 + R ∙800∙ln  > 0,
> 0,
т.е. когда
ln  <
<  и
и
 < exp(
< exp( ) или
) или 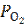 < 4,16∙10−28 атм.
< 4,16∙10−28 атм.
Температуру, выше которой коррозия будет невозможна при стандартных состояниях компонентов можно найти из неравенства

откуда, подставив конкретные значения  и
и  имеем, что при
имеем, что при
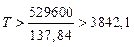 K.
K.
Задача 2. Расчетами ЭДС Е 298 коррозионного элемента и энергии Гиббса Δ rG 298 коррозионного процесса подтвердите возможность электрохимической коррозии при температуре 298,15 К изделия из никеля, находящегося в деаэрированной воде с рН = 7. Предполагается, что коррозия протекает в выделение водорода и образованием Ni(OH)2, произведение растворимости которого при Т = 298,15 К составляет 1,6·10−14.
Решение. Вначале уравнениями описывают возможные электродные процессы:
(−) А: Ni → Ni2+ + 2 e
(+) K: 2H2O + 2 e → H2↑ + 2OH−
Складывая эти уравнения получают суммарное уравнение, которое описывает коррозионный процесс в целом:
Ni + 2H2O = Ni(OH)2↓ + H2↑
Далее по адаптированному для Т = 298,15 К уравнению Нернста рассчитывают потенциал анода, т.е. как видно из приведенного уравнения, никелевого электрода:
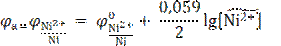
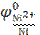 = −0,250 В – значение стандартного потенциала никелевого электрода (справочная величина). Относительное значение концентрации ионов Ni2+ есть
= −0,250 В – значение стандартного потенциала никелевого электрода (справочная величина). Относительное значение концентрации ионов Ni2+ есть
 ,
,
где [Ni2+] – абсолютное значение концентрации ионов Ni2+; С 0 = 1 моль/л – значение стандартной концентрации.
[Ni2+] находят по значению  . В водном растворе малорастворимого вещества, которым является Ni(OH)2, устанавливается равновесие, описываемое следующим уравнением:
. В водном растворе малорастворимого вещества, которым является Ni(OH)2, устанавливается равновесие, описываемое следующим уравнением:
Ni(OH)2 (т) ⇄ Ni2+(р) + 2ОН−(р)
С С 2 С
По определению
 = [Ni2+]∙[OH−]2 = C∙ (2 C)2 = 4C3,
= [Ni2+]∙[OH−]2 = C∙ (2 C)2 = 4C3,
где C – молярная концентрация насыщенного водного раствора Ni(OH)2 или растворимость последнего. Видно, что
[Ni2+] = С =  = 1,587∙10−5 моль/л
= 1,587∙10−5 моль/л
 = 1,587∙10−5
= 1,587∙10−5
[OH−] = 2 C = 3,174∙10−5 моль/л.
После подстановки найденного значения в уравнение Нернста получают
Из приведенного уравнения катодного процесса видно, что это уравнение водо  = −0,392 В.
= −0,392 В.
родного электрода, адоптированного для Т = 298,15 K форма уравнения Нернста для которого имеет вид
 .
.
Поскольку в процессе коррозии среда (вода) подщелачивается (см. уравнение катодного процесса) и таким образом ее рН становится большим 7, то его значение находят через ионное произведение воды  = 10−14 и рассчитанную из
= 10−14 и рассчитанную из  равновесную концентрацию OH− -ионов (см. выше).
равновесную концентрацию OH− -ионов (см. выше).
 = [H+]∙[OH−]
= [H+]∙[OH−]
[H+] =  = 3,151∙10−10 моль/л или
= 3,151∙10−10 моль/л или
 = 3,151∙10−10.
= 3,151∙10−10.
Отсюда
рН = −lg  = −lg(3,151∙10−10) = 9,50.
= −lg(3,151∙10−10) = 9,50.
Относительное значение парциального давления водорода  в атмосфере Земли составляет 5∙10−7. После подстановки значений рН и
в атмосфере Земли составляет 5∙10−7. После подстановки значений рН и  в адаптированную форму уравнения Нернста получают, что
в адаптированную форму уравнения Нернста получают, что
 −0,059∙9,5 – 0,0295∙lg(5∙10−7) = −0,375 В.
−0,059∙9,5 – 0,0295∙lg(5∙10−7) = −0,375 В.
Далее
Е 298 = 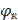 −
−  = −0,375 – (−0,392) = 0,017 В, а
= −0,375 – (−0,392) = 0,017 В, а
Δ rG 298 = − nFE = −2∙96485,3∙0,017 = −3280,50 Дж.
Так как Е 298 > 0, Δ rG 298 < 0, то коррозия изделия из никеля в данных условиях с выделением Н2 и образованием Ni(OH)2 возможна.
Задача 3. Изделие из оцинкованного железа подверглось электрохимической коррозии в водном растворе с рН = 10. При этом поглотилось 280 мл О2 и выделилось 112 мл Н2, измеренных при н.у. Приведите уравнения анодного и катодного процессов. Рассчитайте массы прокорродировавшего при этом металла и образовавшихся продуктов.
Решение. Так как φ0Zn2+/Zn = −0,763 B < φ0Fe2+/Fe = −0,440 B, то цинковое покрытие на железном изделии является анодным и защищает его электрохимически. В соответствии с механизмом защитного действия именно оно (покрытие) и будет разрушаться. Таким образом анодный процесс описывается уравнением
(−) А (Znпокр.): Zn → Zn2+ + 2 e | 3
В соответствии с условием задачи на катоде, которым является железная основа, протекают две реакции, одна с поглощением О2, т.е. с кислородной деполяризацией, другая с выделением Н2, т.е. с водородной деполяризацией

Число моль эквивалентов поглощенного О2 и выделившегося Н2 на катоде

где V 0 экв (О2) и V 0 экв (Н2) – молярный объемы химических эквивалентов при н.у. кислорода и водорода соответственно. Суммарное число моль эквивалентов газов, подвергшихся превращению на катоде: n экв Σ = 0,05 + 0,01 = 0,06 моль экв. Согласно закону эквивалентов, такое же число моль эквивалентов цинка прокорродировало. Тогда

где М экв (Zn) и Z экв (Zn) – молярная масса химического эквивалента цинка и его эквивалентное число соответственно.
Складывая уравнения анодного и катодного процессов, предварительно уравняв с помощью коэффициентов 3 и 1 число отдаваемых и принимаемых электронов, получаем уравнение, описывающее коррозионный процесс:
3Zn + O2 + 4H2O = 3Zn(OH)2↓ + H2↑
Видно, что вторым продуктом коррозии является Zn(OH)2. Согласно закону эквивалентов его масса:

где М экв (Zn(ОН)2) и Z экв (Zn(ОН)2) – молярная масса химического эквивалента Zn(OH)2 и его эквивалентное число соответственно.
Масса выделившегося водорода составила

где М экв (Н2) и Z экв (Н2) – молярная масса химического эквивалента водорода и его эквивалентное число соответственно.
Задачи для самостоятельного решения
Задачи 1–10. Определите термодинамическую возможность окисления металла М кислородом при стандартных условиях. Рассчитайте значение парциального давления кислорода, ниже которого невозможно окисление данного металла. Приведите уравнение соответствующей реакции.
| № | Металл M | Продукт окисления | № | Металл М | Продукт окисления |
| Ni | NiO | Mg | MgO | ||
| Fe | Fe2O3 | Со | СоО | ||
| Ag | Ag2O | Al | Al2O3 | ||
| Cu | CuO | Sn | SnO | ||
| Cr | Cr2O3 | Pb | PbO |
Задачи 11–22. Расчетами стандартных ЭДС Е ° коррозионного элемента и энергии Гиббса ΔrG0298 коррозионного процесса подтвердите возможность электрохимической коррозии при Т = 298 К изделия из данного металла в аэрированном растворе с указанными значениями рН и активностью ионов металла а MZ+. Приведите уравнения анодного и катодного процессов.
| № | Металл | рН | а MZ+·104, моль/л | № | Металл | рН | а MZ+·104, моль/л |
| Mg | 6,0 | Sn | 7,0 | ||||
| Zn | 8,0 | Pb | 6,0 | ||||
| Ag | 3,0 | Cu | 3,0 | ||||
| Fe | 4,0 | Cd | 5,0 | ||||
| Al | 8,0 | Co | 5,0 | ||||
| Ni | 6,0 | Mn | 6,0 |
Задачи 23–34. Контактирующие изделия, изготовленные из двух различных металлов (М 1 и М 2), находятся при 298 К в аэрированном растворе с указанными значениями рН и активности ионов коррозирующего металла а MZ+. Напишите уравнения электродных процессов и суммарной реакции, происходящих при данном виде электрохимической коррозии. Рассчитайте ЭДС Е0 коррозионного элемента и энергию Гиббса ΔrG0298 коррозионного процесса.
| № | М 1 | М 2 | рН | а MZ+·104, моль/л | № | М 1 | М 2 | рН | а MZ+·104, моль/л |
| Al | Fe | 8,0 | Ag | Ni | 5,0 | ||||
| Zn | Cd | 9,0 | Pb | Al | 7,0 | ||||
| Fe | Zn | 6,0 | Fe | Pb | 7,0 | ||||
| Sn | Mg | 7,0 | Cd | Mg | 5,0 | ||||
| Ni | Ag | 5,0 | Cu | Ag | 4,0 | ||||
| Cu | Sn | 4,0 | Sn | Zn | 9,0 |
Задачи 35–46. В результате атмосферной коррозии указанного металла за время t образовалось m грамм его гидроксида M(OH)n. Напишите уравнения электродных процессов и суммарной реакции данного вида коррозии. Вычислите массу прокорродировавшего металла, объем поглощенного при этом газа при н.у. и силу коррозионного тока.
| № | Металл | m (M(OH)2), г | t, мин | № | Металл | m (M(OH)2), г | t, мин |
| Sn | 0,018 | 12,5 | Fe | 0,125 | |||
| Pb | 0,112 | Zn | 0,262 | ||||
| Cd | 0,241 | Mn | 0,304 | ||||
| Co | 0,123 | Ti | 0,038 | 4,5 | |||
| Ni | 0,250 | Mg | 0,132 | 6,5 | |||
| Al | 0,015 | 2,5 | Cr | 0,212 |
Задачи 47 – 54. Рассчитайте массу прокорродировавшего металла за время t и силу коррозионного тока, если в коррозионном элементе катодный процесс протекает: а) с поглощением кислорода; б) с выделением водорода. Объемы газов приведены при Т = 298 К, р = 101,3 кПа.
| № | Металл анода | V О2, мл | V Н2, мл | t, мин |
| Al | 116,4 | 48,6 | 4,5 | |
| V | 48,6 | 3,0 | ||
| Mg | 108,6 | 48,4 | 2,5 | |
| Мn | 18,8 | 2,0 | ||
| Zn | 76,6 | 22,4 | 3,5 | |
| Fe | 36,4 | 5,0 | ||
| Сr | 56,4 | 24,8 | 3,5 | |
| Co | 84,2 | 11,2 | 2,0 |
Задачи 56–65. Приведите уравнения анодного и катодного процессов, протекающих при нарушении целостности покрытия железного изделия (jоFe2+/ Fe = -0,440 В): а) во влажной атмосферной (рН=7) и б) в кислотной деаэрированной (рН=3) средах. К какому типу (анодное, катодное) относится данное покрытие и каков механизм его защитного действия? Рассчитайте ЭДС Е0 коррозионного элемента и энергию Гиббса ΔrG0298 коррозионного процесса.
| № | ||||||||||
| Металл покрытия | Sn | Zn | Mg | Ag | Pb | Ni | Cd | Cu | Au | Cr |
Задачи 66–81. Какой металл коррозионной пары М1 − М2 является протектором? Напишите уравнения электродных процессов и суммарной реакции электрохимической коррозии указанной пары для случаев аэрированной и деаэрированной сред с указанным значением рН. Рассчитайте ЭДС Е0 коррозионного элемента и энергию Гиббса ΔrG0298 коррозионного процесса.
| № | Коррозионная пара М1−М2 | рН | № | Коррозионная пара М1−М2 | рН |
| Cu−Fe | 6,0 | Ag−Cu | 4,0 | ||
| Ni−Sn | 9,0 | Sn−Fe | 6,0 | ||
| Zn−Ag | 8,0 | Mg−Ni | 5,0 | ||
| Co−Pb | 5,0 | Fe−Zn | 8,0 | ||
| Cu – Ag | 2,0 | Au – Co | 5,0 | ||
| Ni – Au | 5,0 | Fe – Sn | 8,0 | ||
| Sn – Co | 6,5 | Zn – Cu | 4,0 | ||
| Cd – Fe | 7,0 | Pb – Ni | 3,5 |
Задачи 82–260. Определите вид (анодное, катодное) и механизм защитного действия (механический, электрохимический) металлического покрытия П на металлическом изделии М. Приведите уравнения электродных процессов влажной атмосферной коррозии (рН = 7) изделия с данным покрытием и рассчитайте значение ЭДС коррозионного элемента при Т = 298 К, если активность ионов корродирующего металла a.
| № | Изделие М | Покрытие П | a, моль/л | № | Изделие М | Покрытие П | a, моль/л |
| Al | Zn | 10−5 | Ni | Cd | 10−7 | ||
| Zn | Ni | 10−6 | Sn | Cu | 10−5 | ||
| Cr | Mg | 10−7 | Cu | Zn | 10−6 | ||
| Fe | Sn | 10−5 | Co | Pb | 10−5 | ||
| Cd | Ag | 10−6 | Fe | Zn | 10−4 | ||
| Fe | Cu | 10−5 | Zn | Sn | 10−7 | ||
| Ni | Sn | 10−7 | Cu | Al | 10−3 | ||
| V | V | 10−6 | Fe | Mn | 10−5 | ||
| Cd | Ni | 10−3 | Cr | Pb | 10−6 | ||
| Mg | Co | 10−7 | Be | Zn | 10−4 | ||
| Ag | Sn | 10−4 | Au | Ni | 10−3 |
Задачи 104–121. Приведите металлы, которые можно использовать в качестве материала для анодного и катодного типов покрытия для металлического изделия М. Уравнениями опишите возможные электродные процессы электрохимической коррозии изделий с этими покрытиями в случае нарушении целостности последних, если они попадают в среду: а) кислотную аэрированную (рН=6); б) нейтральную аэрированную. Рассчитайте ЭДС Е0 коррозионного элемента и энергию Гиббса ΔrG0298 коррозионного процесса.
| № | |||||||||
| Металл изделия М | Fe | Ni | Sn | Pb | Cu | Cd | Ag | Co | Zn |
| № | |||||||||
| Металл изделия М | Ag | Mn | Be | Ti | Mg | V | Al | Pd | Cr |