Химические элементы клетки
Все клетки сходны по своему химическому составу. Основу организма составляют 4 элемента – O, C, H, N, их называют органогенами.
Все элементы, входящие в состав организмов, называют элементами-биогенами. Их делят на три группы:
Химические элементы
| макроэлемнты | микроэлементы | ультрамикроэлементы |
| O, C, H, N P (фосфор) – входит в состав днк, рнк и атф K (калий) – участвует в проведении нервного импульса, угнетает работу сердца (уменьшает сердцебиение) S (сера) – входит в состав аминокислот Fe – входит в состав гемоглобина Mg – входит в состав молекулы хлорофилла Na – проведение нервного импульса Ca – крепкость костей, свертывание крови, мышечное сокращение, усиливает работу сердца Cl – входит в состав соляной кислоты | Бор Кобальт–компонент витамина В12 Медь Молибден Цинк – входит в состав инсулина Ванадий Йод – входит в состав гормона щитовидной железы Бром | Уран Радий Золото Ртуть Бериллий Цезий Селен |
Вода
Молекулу воды частенько называют диполью. Почему?
Молекула состоит из 2х положительно заряженных атомов водорода и отрицательно заряженного кислорода. Имея с одной стороны положительный, а с другой отрицательный заряд, мы можем смело сказать, что молекула имеет два полюса (диполь).
Свойства воды:
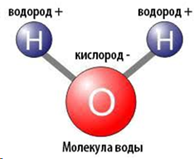 · Полярность молекулы
· Полярность молекулы
· Универсальный полярный растворитель (например, растворяет соли)
· Между молекулами образуются водородные связи (за счёт полярности молекулы и высокой электроотрицательности атома кислорода)
· Высокая теплопроводность – тепло быстро и равномерно распределяется по всему объёму воды, препятствует перегреванию или переохлаждению
· Высокие температуры кипения и плавления
· При замерзании вода расширяется (увеличивается длина водородных связей между её молекулами):
- Положительная роль: благодаря расширению уменьшается плотность воды – лёд при замерзании водоёмов выходит на поверхность, если бы такого не происходило, то водоёмы замерзали полностью, в результате чего могли погибнуть все населяющие его живые организмы.
- Отрицательное значение: При замерзании происходит образование кристалликов льда, приводящее к разрушению клеток и тканей в живых организмах.
· Капиллярные свойства (способность грунтов передвигать жидкость по порам) и высокое поверхностное натяжение(за счёт полярности и водородных связей) Значение:
1) Помогает некоторым насекомым (например: водомеркам) передвигаться по воде
2) Обеспечивает легкое впитывание воды в песок и движение веществ по ксилеме в растении (за счет эффекта капиллярности)
· Вода определяет объём и тургор клетки и тканей. Тургор – напряжённое состояние плазматической мембраны, создаваемое давлением внутриклеточной жидкости, которая на 70-90% состоит из воды.
Гомеостаз (поддержание постоянства внутренней среды) связано с растворимыми ионами и обеспечивается буферными системами, которые могут связывать избыточные ионы Н+ и ОН- и позволяют поддерживать рН н а одном уровне.
В клетке действуют три буферные системы: фосфатная, карбонатная и белковая.
Органические вещества клетки
· Белки (полимеры) - аминокислоты (мономеры)
· Нуклеиновые кислоты (полимеры) - нуклеотиды (мономеры)
· Углеводы (полисахариды – полимеры)
· Липиды (жиры)-не полимеры!!!!
 Белки
Белки
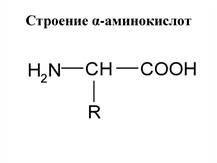
- биополимеры, состоящие из мономеров – аминокислот (всего 20)
Аминокислоты, входящие в состав белка бывают заменимые и незаменимые.
Незаменимые аминокислоты (8) – не могут синтезироваться самостоятельно (преимущественно у гетеротрофов), попадают в организм с пищей.
Заменимые аминокислоты (12) –могут попадать с пищей, но также способны синтезироваться из незаменимых аминокислот.
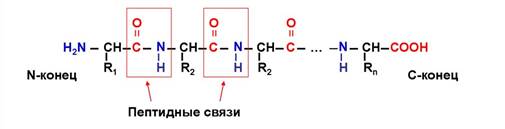
Аминокислоты соединены друг с другом в полипептидную цепь с помощью пептидной связи
Олигопептид: 2-20 аминокислот
Полипептид: > 10-20 аминокислот
Белки: >50 аминокислот
Рассмотрим некоторые белки и их функции:
| БЕЛОК | Функция | БЕЛОК | Функция |
| Гемоглобин | Транспортная (газы) | Казеин | Запасающая |
| Миоглобин | Запасающая | Фибрин (фибриноген) | Защитная |
| Пепсин (пепсиноген) | Каталитическая | Протромбин | |
| Трипсин(трипсиноген) | Альбумин | Транспортная | |
| Амилаза | Иммуноглобулин | Защитная | |
| Птиалин | Инсулин | Регуляторная | |
| Нуклеаза | Гистоны | Структурная | |
| Липаза | |||
| Сахараза | Муцин | Образование пищевого комка | |
| Мальтаза | Миозин | Двигательная | |
| Галактаза | Актин | ||
| Кератин | Структурная (волосы и их производные) | Тубулин | Структурная (микротрубочки) |
| Эластин | Структурная (соединительная ткань) | Родопсин | Рецепторная |
| Коллаген | Интерферон | Защитная |
Структуры белка
 Первичная структура белка – она представляет собой последовательность аминокислот, которые соединяются пептидной связью - это связь между аминогруппой одной аминокислоты и карбоксильной группой другой.
Первичная структура белка – она представляет собой последовательность аминокислот, которые соединяются пептидной связью - это связь между аминогруппой одной аминокислоты и карбоксильной группой другой.
 Вторичная структура белка – представляет собой уже закрученную спираль, которая удерживается благодаря водородным связям. На картинке внизу статьи есть α-спираль, но также имеется еще и β-спираль.
Вторичная структура белка – представляет собой уже закрученную спираль, которая удерживается благодаря водородным связям. На картинке внизу статьи есть α-спираль, но также имеется еще и β-спираль.
 Третичная структура белка – это глобула - пространственная конфигурация, иными словами, еще более закрученная спираль в виде «клубка». Здесь уже несколько связей: дисульфидная (s-s) связь, либо дисульфидный мостик – это соединение водорода и серы на «хвостиках» - радикалах аминокислот; а также гидрофобное взаимодействие – это когда аминокислоты, которые пытаются избежать контакта с водой, скручиваются в самый центр, а гидрофильные находятся снаружи.
Третичная структура белка – это глобула - пространственная конфигурация, иными словами, еще более закрученная спираль в виде «клубка». Здесь уже несколько связей: дисульфидная (s-s) связь, либо дисульфидный мостик – это соединение водорода и серы на «хвостиках» - радикалах аминокислот; а также гидрофобное взаимодействие – это когда аминокислоты, которые пытаются избежать контакта с водой, скручиваются в самый центр, а гидрофильные находятся снаружи.
 Четвертичная структура белка – здесь уже происходит объединение нескольких глобул вместе. В данном случае, аминокислоты удерживаются благодаря водородной связи, но большое значение уделяется ионной, например, когда вокруг иона железа скапливаются глобулы и образуется гемоглобин – белок, который переносит газы в нашем организме. Здесь железо является объединяющим звеном.
Четвертичная структура белка – здесь уже происходит объединение нескольких глобул вместе. В данном случае, аминокислоты удерживаются благодаря водородной связи, но большое значение уделяется ионной, например, когда вокруг иона железа скапливаются глобулы и образуется гемоглобин – белок, который переносит газы в нашем организме. Здесь железо является объединяющим звеном.

Функции белков
 Каталитическая(ферментативная)
Каталитическая(ферментативная)
Подавляющее большинство ферментов – белки. (Ферменты – это биологические катализаторы, т.е. вещества, ускоряющие хим. реакции). Ферменты катализируют практически все хим. реакции в клетке, поскольку сами по себе эти реакции либо не протекают вовсе, либо идут слишком медленно)
 Структурная(строительная)
Структурная(строительная)
Структурные белки цитоскелета (Цитоскелет - это клеточный скелет(каркас), находящийся в цитоплазме живой клетки) придают форму клеткам и многим органоидам и участвуют в изменении формы клеток. Коллаген и эластин — основные компоненты межклеточного вещества соединительной ткани (например, хряща), а из другого структурного белка кератина состоят волосы, ногти, перья птиц и некоторые раковины.
 Транспортная
Транспортная
 Прежде всего такую функцию выполняют белки мембран, которые осуществляют активный перенос веществ из окружающей среды в клетку и обратно.
Прежде всего такую функцию выполняют белки мембран, которые осуществляют активный перенос веществ из окружающей среды в клетку и обратно.
 Белки крови связывают и переносят различные вещества. Например, мы с вами знаем такой белок как гемоглобин. Он осуществляет перенос кислорода из легких в ткани.
Белки крови связывают и переносят различные вещества. Например, мы с вами знаем такой белок как гемоглобин. Он осуществляет перенос кислорода из легких в ткани.
 Двигательная(моторная)
Двигательная(моторная)
Целый класс моторных белков обеспечивает движения организма, например, актин и миозин обеспечивают сокращение мышц.
 Защитная
Защитная
 Защитную функцию, предупреждая инфекционный процесс и сохраняя устойчивость организма, выполняют иммуноглобулины(антитела) крови;
Защитную функцию, предупреждая инфекционный процесс и сохраняя устойчивость организма, выполняют иммуноглобулины(антитела) крови;
 При повреждении тканей работают белки свертывающей системы крови - например, фибриноген, протромбин, антигемофильный глобулин;
При повреждении тканей работают белки свертывающей системы крови - например, фибриноген, протромбин, антигемофильный глобулин;
 Физическую защиту организма обеспечивают коллаген и кератин(но обычно их рассматривают, как белки выполняющие структурную функцию)
Физическую защиту организма обеспечивают коллаген и кератин(но обычно их рассматривают, как белки выполняющие структурную функцию)
 Регуляторная
Регуляторная
Гормоны белков ой природы принимают участие в регуляции процессов обмена веществ. Например, инсулин – гормон поджелудочной железы, регулирует уровень сахара в крови, под его действием гормона в печени происходит превращение глюкозы крови в гликоген печени и т.д.
 Резервная(запасающая)
Резервная(запасающая)
К таким белкам относятся так называемые резервные белки, которые запасаются в качестве источника энергии и вещества в семенах растений и яйцеклетках животных. Ряд других белков используется в организме в качестве источника аминокислот.
Примеры: альбумин запасает воду в яичном желтке,белки семян растений семейства бобовых – источник питания для зародыша.
 Токсическая функция
Токсическая функция
Многие живые организмы выделяют белки-токсины, которые являются ядами для других организмов. Токсины синтезируются в организме ряда животных, грибов, растений, микроорганизмов. В свою очередь, некоторые организмы способны вырабатывать антитоксины, которые подавляют действие этих ядов.
Также существуют белки фибриллярные, глобулярные и сложные. Их основные различия можем пронаблюдать в третичной структуре.
Фибриллярные - третичная структура этих белков представлена нитями. Они не растворимы в воде, прочные, выполняют обычно структурную функцию.
Глобулярные - третичная структура имеет форму шара.
Сложные - образованы соединением белка с другим веществом.
| Хромопротеины | Окрашенные белки. Окраску придает металл (гемоглобин, хлорофилл) |
| Гликопротеины | Соединение белка с углеводом (фибриноген) |
| Липопротеины | Соединение белков и липидов(стероиды) |
| Фосфопротеины | Соединение белка с остатком фосфорной кислоты(казеин) |
Хочется проговорить: протеины (или простые белки) представляют собой белки, молекулы которых содержат только белковые компоненты, а протеиды (сложные молекулы) – белки, которые могут включать ионы металла, образовывать прочные соединения с липидами, нуклеиновыми кислотами и тд.
Важным свойством белков является их способность к денатурации.
Денатурация - изменение структуры и процесс потери белком его природных свойств под воздействием внешних факторов. Денатурация бывает обратимой и необратимой.
Необратимая денатурация – происходит под воздействием химических веществ, высоких температур, радиоактивного излучения. При этом разрушаются все структуры белка, восстановление исходной структуры белка становится невозможным.
Обратимая денатурация (ренатурация) – восстановление белка, если изменения не затронули его первичную структуру.
 Углеводы
Углеводы
Углеводы – это сахаристые вещества с общей формулой Сx(H2O)y
 ПРОСТЫЕ УГЛЕВОДЫ
ПРОСТЫЕ УГЛЕВОДЫ
К простым углеводам относятся моносахариды - растворяются в воде и имеют сладкий вкус. Они отличаются количеством атомов C в молекулах.
 5 атомов - это пентозы, к ним относятся:
5 атомов - это пентозы, к ним относятся:
— Рибоза - входит в состав АТФ и РНК
— Дезоксирибоза - в состав ДНК
 6 атомов - гексозы. Это глюкоза - главный источник энергии, фруктоза, манноза и галактоза
6 атомов - гексозы. Это глюкоза - главный источник энергии, фруктоза, манноза и галактоза
_ _ _ _ _ _ _ _ _ _ _ _ _ _
 СЛОЖНЫЕ УГЛЕВОДЫ
СЛОЖНЫЕ УГЛЕВОДЫ
Делятся на олигосахариды и полисахариды.
 Олигосахариды
Олигосахариды
— Входят в состав гликокаликса
— Из них нам нужны дисахариды (состоят из двух моносахаридов):
 Мальтоза = глюкоза + глюкоза
Мальтоза = глюкоза + глюкоза
Образуется при расщеплении крахмала
 Сахароза = глюкоза + фруктоза
Сахароза = глюкоза + фруктоза
Белый порошок для чая
 Лактоза = глюкоза + галактоза
Лактоза = глюкоза + галактоза
В молоке много
 Полисахариды
Полисахариды
К ним относятся:
— Целлюлоза (клетчатка) - входит в состав клеточной стенки растений
— Хитин - входит в состав клеточной стенки грибов и экзоскелет членистоногих
— Муреин - входит в состав клеточной стенки бактерий
— Крахмал - нужен как запас энергии, синтезируется у растений
— Гликоген - как крахмал, только у животных и грибов
Функции углеводов
Энергетическая. Глюкоза является основным источником энергии, высвобождаемой в клетках живых организмов в ходе клеточного дыхания (1 г углеводов при окислении высвобождает 17,6 кДж энергии).
Структурная. Целлюлоза входит в состав клеточных оболочек растений; хитин является структурным компонентом покровов членистоногих и клеточных стенок грибов.
Запасающая. Крахмал – запасное питательное вещество растений, гликоген – запасное питательное вещество животных и грибов.
Метаболическая. Пентозы участвуют в синтезе нуклеотидов (рибоза входит в состав нуклеотидов РНК, дезоксирибоза — в состав нуклеотидов ДНК), некоторых коферментов (например, НАД, НАДФ, кофермента А, ФАД), АМФ; принимают участие в фотосинтезе (рибулозодифосфат является акцептором СO2 в темновой фазе фотосинтеза).
 Нуклеиновые кислоты
Нуклеиновые кислоты
Нуклеиновые кислоты состоят из мономеров - нуклеотидов
| ДНК | РНК |
| АТГЦ | АУГЦ |
| дезоксирибоза | рибоза |
| Двухцепочечная | Одноцепочечная |
| Выполняет функцию хранения и передачи наследственной информации | тРНК- транспортирует аминокислоты иРНК – является матрицей для синтеза аминокислот рРНК- входит в состав рибосом |
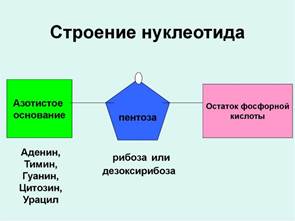
Амф, Адф, Атф – нуклеотиды, которые отличаются кол-вом остатков фосфорной кислоты.
Нуклеотиды соединяются друг с другом благодаря фосфодиэфирным (в 1 цепочке) и водородным связям (в 2 разных цепях).
Парные азотистые основания, между которыми возникают водородные связи, называют комплементарными, т.е. взаимодополняющими. Таким образом, в молекуле ДНК последовательность нуклеотидов в одной цепи комплементарна последовательности нуклеотидов в другой цепи. Расстояние между соседними нуклеотидами цепи составляет 0,34 нм. Полный оборот спирали (период идентичности) составляет 10 нуклеотидов, а шаг - 3,4 нм. Диаметр двойной спирали одинаков по всей длине и равен 2 нм.
 Липиды
Липиды
Липиды – органические вещества, состоящие из многоатомных спиртов и остатков карбоновых кислот (нерастворимы в воде). Не являются полимерами.
| Простые липиды | |||
| Триглицериды(животные жиры, растительные масла) | Состоят из глицерина и 3х остатков жирных кислот
- Жирами называют триглицериды, которые при 20 C остаются твердыми
- Маслами называют триглицериды, которые при 20 C остаются жидкими
Триглицериды запасают энергию в клетках организма, а накапливаясь, могут участвовать в терморегуляции (выполняют теплоизоляционную функцию). 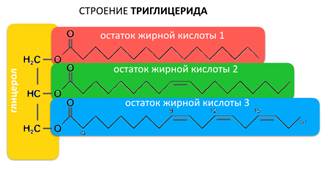
| ||
| Воски | Пчелиный и растительный. Сложные эфиры ВЖК и высокомолекулярных одноатомных спиртов. | ||
| Сложные липиды | |||
| Фосфолипиды | Измененная версия триглицерида: на место третьей жирной кислоты встает остаток фосфорной кислоты, и свойства молекулы изменяются. Остаток фосфорной кислоты совместно с глицерином образуют гидрофильную группу (гидрофильная - взаимодействующая с водой),а жирная кислота по-прежнему остается гидрофобной.
Фосфолипиды образуют каркас клеточной мембраны - структурная функция. 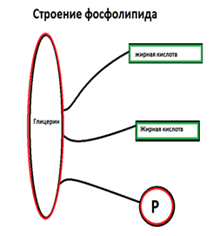 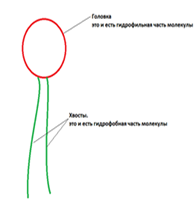
| ||
| Гликолипиды | Гликолипиды состоят из жиров и углеводов (широко распространены в нервной ткани, мозге). Находятся в гликокаликсе. | ||
Функции липидов:
Энергетическая. При окислении 1 г жира выделяется 38,9 кДЖ энергии.
Запасающая. Жиры как резерв энергии и источник метаболической воды.
Строительная. Фосфолипиды и гликолипиды плазмалеммы.
Защитная. Защита от переохлаждения, повреждения внутренних органов и тканей при механическом воздействии, амортизация ударов.
Терморегуляция. Защита от переохлаждения – сохранения тепла за счет подкожно-жировой клетчатки.
Регуляторная. Кортизон, тестостерон.