ФГАОУ ВПО «Уральский федеральный университет
Имени первого Президента России Б.Н. Ельцина»
Кафедра иммунохимии
Методические указания к лабораторному занятию по дисциплине
«Методы выделения и анализа биополимеров»
Для магистров 1 курса ХТИ, обучающихся по программе «Молекулярная биотехнология и биоинженерия»
(направление 19.014.01 «Биотехнология»)
Тема: Колориметрические методы определения концентрации белка
(лабораторное занятие)
Цель занятия: получить представление о количественных методах определения концентрации белка.
Работа № 1. Количественное определение концентрации белка
биуретовым методом
Биуретовый метод разработан в 1949 году А. Горналлом, К. Бардавиллом и М. Дэвидом. В этой реакции используется сильнощелочной раствор солей меди, в котором биурет (H2N-СО-МН-СО-NH2) образует комплексное соединение пурпурной окраски. Эта же реакция протекает и с пептидными связями белков и пептидов. Интенсивность окраски (сине-фиолетовая) пропорциональна числу пептидных связей.
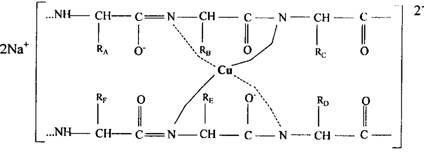
Комплексное соединение, образующееся в результате взаимодействия белков с биуретовым реактивом.
Приготовление биуретового реактива. 750 мг сульфата меди (CuSO4*5H2O) и 3 г виннокислого натрия-калия (NаКС4Н406) растворяют в 250 мл воды, затем при интенсивном перемешивании добавляют 150 мл 10 %-ного №ОН (свободного от углекислого натрия) и 1 г йодистого калия. Объем раствора доводят водой до 1000 мл. Раствор хранят в полиэтиленовой посуде. Стандартный раствор белка для построения калибровочного графика: водный раствор бычьего сывороточного альбумина концентрацией 0,5-10 мг/мл. Нужно иметь в виду, что в присутствии солей аммония могут образовываться окрашенные медно-аммиачные комплексы, мешающие определению. Трис, сахароза и глицерол влияют на развитие окраски; биуретовый реактив окрашивает желчные пигменты. Липиды и детергенты могут вызвать помутнение пробы и искажают результаты.
Недостатком данного метода является его низкая чувствительность - 500 мкг/мл.
Опыт 1. Определение концентрации белка биуретовым методом (пропорцией)
Принцип метода: пептидные связи белка образуют с ионами Cu2+ в составе биуретового реактива окрашенный комплекс с максимумом поглощения при 560 нм, интенсивность окраски пропорциональна концентрации белка и определяется спектрофотометрически.

Ход работы: в пробирку отбирают 5 мл биуретового реактива и 0,1 мл исследуемого препарата. Аналогично готовят контрольную пробу, в которой вместо препарата – стандартный раствор с концентрацией белка 60 г/л. Через 30 мин выдержки при комнатной температуре обе пробы фотометрируют против биуретового реактива при длине волны 560 нм.
Расчет концентрации общего белка производят по формуле:
Сбелка (г/л) = Еоп/Ест * 60,
где Еоп – оптическая плотность исследуемого раствора, Ест – оптическая плотность стандартного раствора, 60 (г/л) – концентрация белка в стандартном растворе.
Примечание: метод обеспечивает линейность от 10 до 100 г/л белка. Если концентрация белка в исследуемом препарате более 100 г/л, то разбавить его физиологическим раствором в 2-3 раза, результат умножить на коэффициент разбавления. Определению белка биуретовым методом может мешать мочевина, глицерин, декстраны и некоторые другие соединения.
Опыт 2. Количественное определение концентрации белка биуретовым методом (по калибровочно кривой).
Принцип метода. Метод основан на образовании в щелочной среде окрашенного в фиолетовый цвет комплекса пептидных связей белков с ионами двухвалентной меди. Существуют 2 разновидности метода: при одной из них определяют от 2 до 10 мг белка в пробе; при другой (микрометод) - от 0,1 до 2 мг. Для протекания этой реакции необходимо наличие, по крайней мере, двух пептидных связей.
Колориметрический анализ проводят сравнением поглощения света исследуемым раствором с поглощением проб стандартного ряда (калибровочная кривая). и качестве стандарта часто используют раствор бычьего сывороточного альбумина в воде или буферном растворе.
Ход работы.
1. Производят разбавление стандартного белкового раствора с концентрацией 2 мг/мл следующим образом:
| № пробы | Объем раствора белка, мл | Объем дист., воды, мл | Концентрация белка, мг/мл | Содержание белка в пробе, мг | Ед. поглощения (ОД) |
| (контроль) | - | 3,0 | - | - | |
| 0,3 | 2,7 | 0,2 | 0,6 | ||
| 0,6 | 2,4 | 0,4 | 1,2 | ||
| 0,9 | 2,1 | 0,6 | 1,8 | ||
| 1,5 | 1,5 | 1,0 | 3,0 | ||
| 2,0 | 1,0 | 1,32 | 4,0 | ||
| 3,0 | - | 2,0 | 6,0 | ||
| (инсулин) | 3,0 | - | X | X | |
| (Ig общий) | 3,0 | - | Х | Х |
Проба №1 содержит вместо белка воду и называется контрольной. Объем всех исследуемых проб должен быть одинаковым и в данном случае составляет 3 мл.
2. Во все пробы добавляют по 2 мл биуретового реактива, тщательно перемешивают и выдерживают 30 мин при комнатной температуре.
3. После этого пробы фотометрируют на фотоэлектроколориметре при длине волны 540 нм (500-560 нм, зеленый светофильтр) против фотометрического контроля, которым является проба № 1. Показания прибора (оптическая плотность, ОД, значения на нижней логарифмической шкале прибора) заносят в таблицу и затем строят калибровочную кривую, откладывая по оси ординат значения оптической плотности, а по оси абсцисс - концентрацию (или содержание) белка. Калибровочный график должен иметь вид прямой, выходящей из начала координат.
4. Параллельно с пробами для калибровочной кривой ставятся и опытные пробы. Объем исследуемого белка (опытной пробы) - 3 мл.
Необходимо помнить, что интенсивность окраски определяется концентрацией вещества, но зависит также от температуры и времени развития окраски. Поэтому опытные и стандартные пробы должны быть обработаны в одинаковых строго определенных условиях. Расчеты концентрации белка в опытных пробах проводят пользуясь калибровочным графиком. Если оптическая плотность пробы выходит за его пределы, необходимо заново приготовить образец белка таким образом, чтобы попасть на калибровочную кривую.