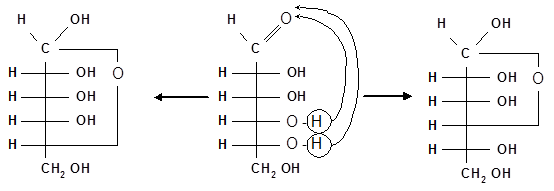2.1 Карбонильные формы моносахаридов.
Для выяснения строения и стереохимии моносахаридов химикам потребовалось более ста лет. В результате многолетних исследований было установлено, что моносахариды по химической природе являются полиоксиальдегидами или полиоксикетонами. Большинство моносахаридов имеет линейную цепь углеродных атомов. Важнейшими представителями моносахаридов являются гексозы - глюкоза (виноградный сахар) и фруктоза (фруктовый сахар), поэтому рассмотрим строение моносахаридов на примере этих соединений. Обе гексозы являются изомерами и имеют одну молекулярную формулу С6Н12О6 [C6(H2O)6]. Шесть атомов углерода глюкозы образуют прямую неразветвленную цепь:
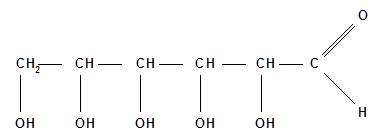
Это доказано восстановлением её в 2-иодгексан при действии йодистого водорода. Наличие альдегидной группы было доказано тем, что к глюкозе, так же как и к альдегидам, присоединяется синильная кислота (Килиани, 1887 г.):
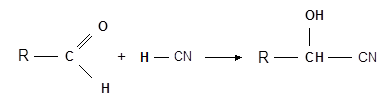 ,
,
где R – С5H11O5
Кроме этого, глюкоза дает качественные реакции на альдегидную группу: “серебряного зеркала“ при взаимодействии с [Аg (NH)2]OH и с фелинговой жидкостью. В обоих случаях альдегидная группа окисляется до карбоксильной и образуется глюконовая кислота:
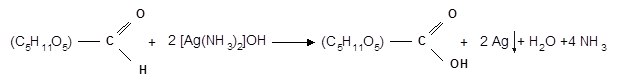
В 1869 г. А. А. Колли установил, что глюкоза реагирует с пятью молекулами уксусного ангидрида, образуя при этом пять сложноэфирных группировок, и поэтому является пятиатомным спиртом.
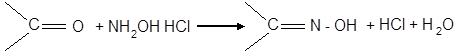
Фруктоза при восстановлении иодистым водородом также дает 2-иодгексан, что доказывает ее линейное строение. Наличие карбонильной группы можно доказать реакциями взаимодействия с синильной кислотой или с солянокислым гидроксиламином:
Месторасположение карбонильной группы в углеродной цепи доказывается тем, что окисление фруктозы происходит с разрывом углеродной цепи и образованием щавелевой и винной кислот:
|
|
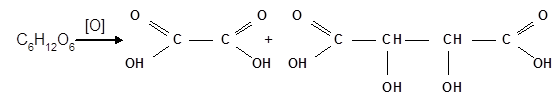
| щавелевая кислота | винная кислота |
Как и глюкоза, фруктоза реагирует с пятью молекулами уксусного ангидрида, образуя пять сложноэфирных группировок, следовательно, она содержит пять гидроксильных групп.
Таким образом, фруктоза представляет собой пятиатомный кетоспирт:
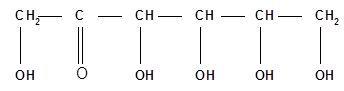
Это так называемые открытые, цепные формы моносахаридов (оксоформы).
2.2 Циклические формы моносахаридов
В растворах моносахаридов наряду с альдегидными или кетонными формами всегда содержатся циклические полуацетальные формы (оксиформы), причем содержание открытой формы мало (доли процента). В кристаллическом индивидуальном состоянии все моносахариды (кроме триоз) представляют собой внутренние полуацетали полиоксиальдегидов или полиоксикетонов. Структура полиацеталей аналогична структуре полуацеталей, возникающих при присоединении молекулы спирта к альдегиду:
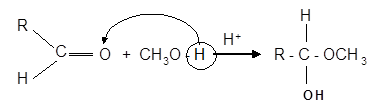
В случае моносахаридов эта реакция происходит внутримолекулярно с наиболее “удобно” расположенным гидроксилом. Обычно полуацетали неустойчивы, но у моносахаридов полуацетальная форма устойчива, так как образование циклической полуацетальной формы происходит внутримолекулярно. Циклические формы моносахаридов возникают в результате взаимодействия альдегидной (кетонной) группы с гидроксильной группой у пятого или у четвертого углеродного атома - кислород ОН-группы присоединяется к атому углерода карбонильной группы, а водород ОН-группы присоединяется к атому кислорода карбонильной группы. Образуются устойчивые циклические полуацетальные формы - пиранозная (шестичленный цикл) либо фуранозная (пятичленный цикл). Эти формы получили название от соответствующих гетероциклических соединений, шестичленные - от пирана (точнее тетрагидропирана), а пятичленные - от фурана (точнее тетрагидрофурана). Следует отметить, что гидроксил, образованный на месте бывшей карбонильной группы, называется полуацетальным или гликозидным и отличается по свойствам от спиртовых гидроксилов.
|
|
Для указания размера кольца в циклической форме моносахарида две последние буквы названия моносахарида (“оза”) заменяют окончанием “фураноза” в случае пятичленного кольца или “пираноза”- в случае шестичленного кольца, например, глюкопираноза, фруктофураноза, рибофураноза и т.д.
В циклической форме монозы нет альдегидной или кетонной группы, имеются только гидроксильные группы. Эти гидроксилы разные: один гидроксил полуацетальный появился в результате внутримолекулярного взаимодействия карбонильной и спиртовой групп, для сахаров этот гидроксил называют еще гликозидным; остальные гидроксилы спиртовые, при этом в глюкозе один из них у шестого атома углерода первичный, остальные - вторичные.
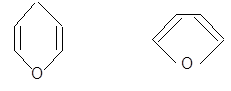
| пиран | фуран |