12.11.2021
Тема: «Относительная молекулярная масса.
Массовая доля химического элемента в соединении»
Цели урока: изучить различия между относительными атомной и молекулярными массами; изучить понятие массовой доли химического элемента и научиться ее рассчитывать; развить у учащихся умение делать несложные, логические построения на основе химических знаний; воспитать личностную рефлексию, то есть умение осмысливать свои действия и себя в проблемной исследовательской ситуации; воспитать самоорганизацию и самооценку учащихся при выполнении исследовательских заданий на уроке.
Теоретический материал
Актуализация знаний
Относительную атомную массу элемента обозначают Ar. В настоящее время за относительную атомную массу элемента принимают величину, показывающую, во сколько раз масса его атома больше 1/12 массы атома углерода. Значения относительных атомных масс химических элементов указаны в соответствующих клетках таблицы Д.И. Менделеева:
Ar(H)=1, Ar(O)=16, Ar(Fe)=56, Ar(K)=39, Ar(S)=32, Ar(Cl)=35,5.
Относительная молекулярная масса
Если вещество образовано несколькими элементами (одинаковыми или разными), то речь уже идет о молекулах и «Молекулярной относительной массе». Она складывается из атомных масс всех химических элементов образующих молекулу, умноженные на количество этих атомов. Обозначается Mr. Относительные атомная и молекулярная массы не имеют размерности.
Например:
Mr (O2) = Ar (O) ·2 = 16 · 2 = 32;
Mr (H2O) = Ar (H) · 2 + Ar (O) = 1· 2 +16 = 18;
Mr (H2SO4) = Ar (H) · 2 + Ar (S) + Ar (O) · 4 = 1· 2 + 32 + 16 · 4 = 98;
Mr(Ca3(РО4)2)=Ar(Ca) ·3+Ar(P) ·2+Ar(O) · 8 =40·3+31·2+16·8=310
Запомни: Значение атомных масс разных химических элементов складываются между собой. Если одинаковых атомов в молекуле несколько, от их численное значение атомных масс умножается на количество этих атомов.
|
|
Вычисление массовой доли химического элемента в соединении
По формуле вещества можно рассчитать массовую долю атомов каждого химического элемента, который входит в состав этого вещества, т. е. определить, какую часть от общей массы вещества составляет масса атомов данного элемента.
Массовая доля (w) атомов химического элемента в веществе показывает, какая часть относительной молекулярной (формульной) массы вещества приходится на атомы данного элемента.
Массовая доля атомов элемента А в сложном веществе АxBy рассчитывается по формуле:
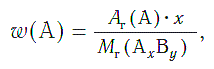
где w («дубль-вэ») — массовая доля элемента А;
Ar(А) — относительная атомная масса элемента А;
х, у — числа атомов элементов А и В в формуле вещества;
Mr(АхBy) — относительная молекулярная (формульная) масса вещества АхBy.
Массовые доли выражаются в долях единицы или в процентах.
Разбор тренировочных заданий
Задача 1.
Вычислите массовую долю водорода в формуле соляной кислоты HCl.
 Дано: Решение:
Дано: Решение:
 HCl 1.Вычисляем относительную молекулярную массу соединения.
HCl 1.Вычисляем относительную молекулярную массу соединения.
W(H)=? Mr(HCl)=1+35,5=36,5
W(Cl)=? 2. Вычислим массовую долю H
W(H)= 1\36,5=0.027 или 2,7 %
W(Cl)= 35,5\36,5=0,973 или 97,3%
Ответ: 0,973 или 97,3%
Задача 2.
Вычислите массовую долю водорода, серы и кислорода в сернистой кислоте, формула которой H2SO3

Домашнее задание
проработать конспект, выполнить задания:
Задание 1. Определите относительную молекулярную массу химических соединений: SO3, CH4, AlCl3, FeSO3, Na2S203, Al(OH)3.
Задание 2.
Вычислите массовую долю кальция, фосфора, кислорода в фосфоритной муке, формула которой Са3(PO4)2